
Hyun-Ji Bock et al., |
要約 |
| 腸内細菌叢は宿主の恒常性維持に重要な役割を果たしており、老化プロセスはその構成と機能に深く影響を及ぼします。蓄積されたエビデンスは、腸内細菌叢の変化が単に老化の結果であるだけでなく、加齢に伴う生理学的機能低下の積極的な要因でもあることを示唆しています。特に、加齢に依存した腸内細菌叢のディスバイオシスは、宿主の老化および老化関連疾患に寄与する重要な要因として浮上しています。本レビューでは、老化プロセスにおける腸内細菌叢の変化(例えば、α多様性の低下、有益な常在菌の枯渇、病原性細菌の増加)を体系的にまとめ、微生物の老化と宿主の老化の時空間的ダイナミクスおよび因果関係について考察します。腸内細菌叢が代謝疾患(例:肥満、2型糖尿病、心血管疾患)、免疫老化、神経変性疾患(例:アルツハイマー病、パーキンソン病)といった老化関連疾患に影響を及ぼす制御メカニズムについても解明します。最後に、腸内細菌叢を標的とした介入戦略(例:プロバイオティクス、プレバイオティクス、ポストバイオティクス)と先進的な研究戦略について考察します。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.加齢と腸内マイクロバイオームの変化 |
| 3.加齢に伴う代謝障害と腸内マイクロバイオーム |
| 4.免疫老化とマイクロバイオーム |
| 5.加齢に伴う神経変性疾患と腸内細菌叢 |
| 6.プロバイオティクス、プレバイオティクス、ポストバイオティクスによる抗老化介入 |
| 7.考察と結論 |
| 本文 |
| 1.はじめに |
| 世界的な高齢化の進行に伴い、老化の生物学的メカニズムの解明は、生物医学研究における重要な課題となっています。従来の老化理論は、ゲノム損傷、テロメア短縮、エピジェネティック変化といった細胞自律的なメカニズムに焦点を当ててきましたが、近年の研究では、腸内マイクロバイオームが老化プロセスに影響を与える重要な因子であることが示唆されています(1、2)。腸内マイクロバイオームは、短鎖脂肪酸や第二胆汁酸(SBA)などの微生物代謝産物を産生することで宿主の健康に貢献しており、これらの代謝産物はインスリン感受性、免疫恒常性、神経内分泌ネットワークを正に調節することが知られています(3)。しかしながら、腸内マイクロバイオームには加齢に伴う変化が観察されており、α多様性の低下、有益な細菌の減少、炎症誘発性病原菌の増加などが特徴として挙げられます。これらの変化は、短鎖脂肪酸と胆汁酸バランスの代謝調節異常を引き起こし、それによって代謝障害、免疫老化、アルツハイマー病やパーキンソン病などの神経変性疾患の進行を加速させる(4、5)。注目すべきは、腸内マイクロバイオームは宿主と共進化しており、生涯を通じて外部の影響(例えば、食事パターン、環境曝露、薬理学的介入)に非常に敏感である。これらのうち、食事は、栄養素の利用可能性、微生物の代謝基質、微生物間の競争への影響を通じて微生物組成を形成し、マイクロバイオームの構成と機能を調節する主要な要因と考えられている(6)。腸内マイクロバイオームと老化に関するレビューの数は増えているが、最近のメカニズムとトランスレーショナルな発見を統合したものはほとんどない。百歳以上の高齢者に関連する微生物の特徴、糞便微生物移植(FMT)に基づく因果関係の証拠、次世代プロバイオティクス/ポストバイオティクス戦略における臨床的進歩など、最近の研究成果は、まだ包括的に議論されていません。さらに、この分野が個別化されたマイクロバイオーム介入へと進むにつれて、基本的なマイクロバイオーム老化生物学と新たな治療応用を結びつける統合的なアプローチが喫緊に求められています。 |
| 本レビューでは、加齢過程における腸内マイクロバイオームの動的な変化を体系的にまとめ、微生物叢の異常が加齢関連疾患に寄与するメカニズムを解明し、加齢および加齢関連疾患の発症を軽減するためのマイクロバイオーム標的戦略の有望な展望を探ります。最新の発見、臨床応用への取り組み、個別化されたバイオティクスベースの介入の可能性に焦点を当てることで、本レビューは、これまでの研究とは一線を画す、最新かつ統合的な視点を提供することを目指します。 |
| 2.加齢と腸内マイクロバイオームの変化 |
| 腸内マイクロバイオームは、広大な内因性生態系として、出生時から宿主と共進化し、相互に有益な共生関係を築いています(1)。成人の腸内マイクロバイオームは、通常、細菌、真菌、ウイルス、バクテリオファージから構成されています。優勢な細菌門には、フィルミクテス門、バクテロイデス門、プロテオバクテリア門、アクチノバクテリア(放線菌)門、ベルコミクロビア門があり、フィルミクテス門とバクテロイデス門が微生物集団の大部分を占めています(7)。これらの腸内共生菌は、短鎖脂肪酸、亜硫酸水素ナトリウム(SBA)、必須ビタミン(ビタミンB群、ビタミンK2など)、その他の重要な栄養素といった主要な微生物代謝産物を合成することで、宿主の代謝、エネルギー恒常性、免疫安定性に大きく貢献しています(8)。しかし、多くの研究で、腸内細菌叢の構成と多様性は加齢とともに徐々に変化することが示されています(図1)。例えば、乳児期には放線菌門とプロテオバクテリア門が優勢で、ビフィドバクテリウム属が重要な属である。対照的に、成人の腸内細菌叢はフィルミクテス門とバクテロイデス門が優勢で、幼少期には存在しないか少ないフェカリバクテリウム属やブラウティア属などの属が存在する(9)。乳児が約3歳に成長するにつれて、腸内細菌叢の多様性は徐々に増加し、成人の腸内細菌叢の多様性に近づく(7)。成人期を通して腸内細菌叢は一般的に安定するが、加齢とともにその構成は大きく変化し、特に多様性が著しく低下する(1)。具体的には、グローバルなメタゲノムシーケンスデータのメタ解析では、高齢者は腸球菌、連鎖球菌、放線菌、ルミノコッカスなどの炎症促進性病原菌のレベルが高く、フェカリバクテリウム、ローズブリア、コプロコッカスなどの有益な短鎖脂肪酸産生菌のレベルが低いことが一貫して示されています(1、10)。これらの微生物の特徴は、不健康な老化表現型を特徴づけている可能性があります。興味深いことに、中国とイタリアの百歳以上の高齢者の腸内マイクロバイオームプロファイリングの研究では、若い人と比較してα多様性が高いことが明らかになり、年齢とともにα多様性が減少するという一般的な傾向と矛盾しています(11)。中国、韓国、日本、イタリアなどさまざまな集団において、百歳以上の高齢者は一貫してアッカーマンシアとクリステンセネラ科が豊富に存在しており、これらの細菌分類群が健康的な老化と長寿の潜在的な微生物マーカーとして機能する可能性があることを示唆しています(1、12)。ヒトでの知見と一致して、高齢マウスでは腸球菌や連鎖球菌などの病原性細菌の増加が観察され、その一方でビフィズス菌やアッケルマンシアなどの有益な細菌は減少します(13)。さらに、高齢マウスは若いマウスと比較して操作分類単位(OTU)の豊富さやα多様性指数(Chao1、Simpson、ACEなど)が有意に低く、門レベルの組成に変化が見られ、若いマウスではプロテオバクテリアがより豊富であるのに対し、高齢マウスでは放線菌とフソバクテリアが優勢になります(14)。ショウジョウバエでも同様のシフトが起こり、若いハエではアセトバクター・ペルシシとラクトバチルス・ブレビスが優勢ですが、高齢のハエではアセトバクター・マロラムとラクトバチルス・プランタルムが優勢になります(15)。興味深いことに、ショウジョウバエでは観察された操作分類単位の数が加齢とともに増加するが、これは加齢マウスで観察される傾向とは対照的である(14、15)。この相違は、ショウジョウバエの寿命が短いことと適応免疫系が欠如していることに起因する可能性があり、加齢に伴う免疫応答の調節異常が特定の共生生物の過剰増殖につながる可能性がある(16)。 |
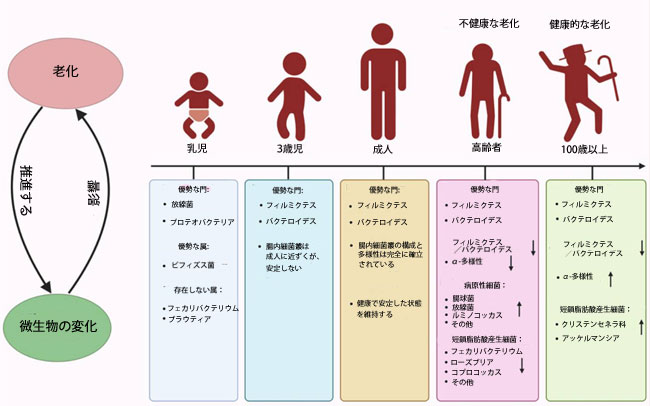 |
図1. 加齢と腸内細菌叢の変化。 加齢に伴い、腸内細菌叢は徐々に変化します。乳児期には放線菌門とプロテオバクテリア門が優勢で、腸内細菌叢は3歳頃までは成人のプロファイルとは異なり、比較的不安定な状態が続きます。成人では、フィルミクテス門とバクテロイデス門が優勢で、微生物群集は成人期を通じて安定する傾向があります。しかし、高齢者では、多様性の低下、有益な細菌の減少、病原菌の増加といった、不健康な加齢の特徴であるディスバイオシスが顕著になります。興味深いことに、百歳以上の高齢者は、多様性の増加と有益なアッケルマンシア属菌の増加を伴う、より安定した腸内細菌叢を示します。注目すべきは、加齢が腸内細菌叢の変化を促進する一方で、腸内細菌叢の変化が加齢プロセスに影響を与える可能性があるということです。ただし、正確な時間的順序と因果関係はまだ解明されていません。 |
| 腸内細菌叢の老化と宿主の老化の間の時空間的な順序と因果関係は依然として議論の的となっており、明確にすることは困難である(図 1)。いくつかの研究では、宿主の老化が腸内細菌叢の異常の主な原因であると示唆されている。老化に伴い、胃腸運動の低下と胃酸分泌の低下により、病原性細菌(例えば、大腸菌)にとって好ましい環境が作られ、乳酸菌などの有益な分類群が抑制される(17)。さらに、免疫細胞機能の低下と炎症性サイトカインの増加を特徴とする免疫老化が、腸内細菌叢の調節異常の重要な要因として浮上している(18、19)。例えば、老齢マウスの老化B細胞はIgA分泌が低下し、病原性細菌の増殖を促進し、微生物の恒常性を乱す(18)。ヒトとマウスの両方におけるT細胞の老化は、炎症環境下で正常な微生物群集を維持できないことが原因で、微生物多様性の低下とも関連している(19)。また、高齢マウスにおけるTNF-αレベルの上昇は、抗菌ペプチドの誘導を介して微生物のディスバイオシスを引き起こす可能性がある(20)。しかし、腸内微生物のディスバイオシスが宿主の老化加速に先行し、積極的に寄与する可能性があることを示唆する証拠が増えている。ショウジョウバエでは、加齢に伴う微生物の不均衡が腸管バリア機能不全の前に現れ、加齢に伴う死亡率の重要な要因となっている(16)。糞便微生物移植では、高齢のハエから無菌のレシピエントに腸内微生物叢を移植すると、ハエの死亡が加速することが示されており、高齢の微生物叢が原因的役割を果たしていることが示唆されている(15)。げっ歯類でも同様の知見が報告されており、高齢の微生物叢を若い無菌マウスに移植すると、全身性炎症が引き起こされる(21)。ヒトにおいても、アルツハイマー病(AD)やパーキンソン病(PD)の初期段階の患者は、認知症状の発症前であっても腸内微生物の特徴に大きな違いが見られることが臨床研究で示されており、腸内微生物叢の変化が神経変性の早期バイオマーカーとして機能する可能性が示唆されている(22、23)。 |
| 総合的に見ると、宿主の老化と腸内細菌叢の異常との因果関係はまだ完全には解明されていないものの、現在のエビデンスは双方向的な相互作用を示唆している。今後の研究では、宿主の老化に伴う腸内細菌叢の変化の時間的関係を明らかにするために、縦断研究、糞便微生物移植実験、および統合的なマルチオミクス解析(メタボロミクス、トランスクリプトミクス、プロテオミクスなど)を活用する必要がある。方向性に関わらず、腸内細菌叢が宿主の老化を調節する上で重要な役割を果たしており、治療介入の重要な標的となる可能性を秘めていることは明らかである。 |
| 3.加齢に伴う代謝障害と腸内マイクロバイオーム |
| 加齢が進むにつれて、代謝系の機能は徐々に低下し、肥満、2型糖尿病(T2DM)、心血管疾患などの代謝障害を引き起こします(24)。近年の研究では、腸内マイクロバイオームが、短鎖脂肪酸(酢酸、プロピオン酸、酪酸など)、亜硫酸水素塩(SBA)、トリメチルアミンN-オキシド(TMAO)、腸由来の神経内分泌因子や免疫因子などの微生物代謝産物の産生を通じて、代謝障害の調節に重要な役割を果たしていることが示されています(25)(図2)。げっ歯類を用いた研究では、フィルミクテス門/バクテロイデス門比の上昇が肥満と一貫して関連付けられています。さらに、若いドナーから糞便微生物移植(FMT)によって腸内細菌叢を移植すると、高齢のレシピエントマウスの体重が減少し、脂肪蓄積が抑制されました(26)。アラブ首長国連邦で行われた臨床研究でも、肥満の成人と痩せた成人の腸内細菌叢に大きな違いがあることが明らかになったが、地理的な場所や食文化がこれらの結果に影響を与えた可能性がある(27)。 |
 |
 |
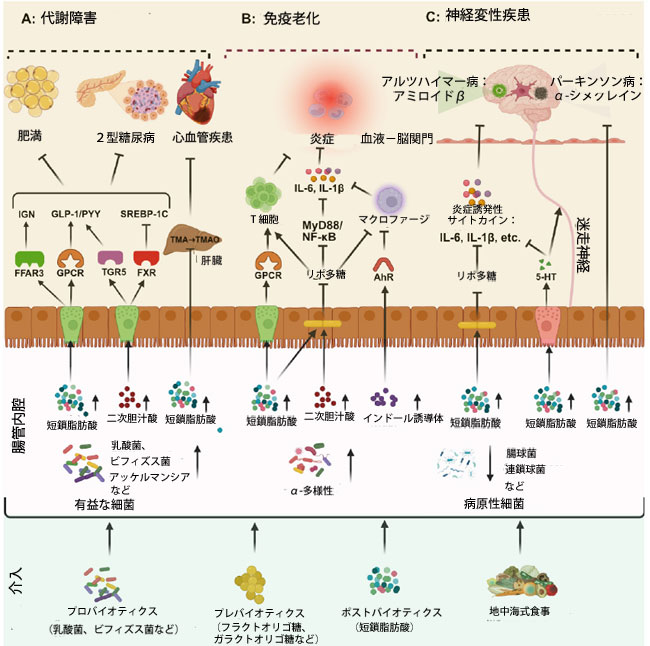
図2. 腸内細菌叢を標的とした介入による加齢関連疾患の緩和メカニズム。 腸内細菌叢は、代謝障害、免疫老化、神経変性疾患などの加齢関連疾患の発症と進行において極めて重要な役割を果たします。介入(プロバイオティクス、プレバイオティクス、ポストバイオティクス、地中海食など)は、腸内細菌叢を再構築し、短鎖脂肪酸、二次胆汁酸(SBA)、インドール誘導体などの微生物代謝産物の産生を促進することにより、これらの疾患を緩和することができます。 (A)(1)短鎖脂肪酸は、腸由来脂肪酸受容体FFAR3を活性化することにより腸内糖新生(IGN)を促進し、インスリン抵抗性を改善し、肥満および2型糖尿病(T2DM)を緩和します。 (2)短鎖脂肪酸は、腸由来のGタンパク質共役受容体GPCRの活性化を介してGLP-1とPYYの放出を刺激し、食欲を抑制したりインスリン分泌を促進したりして、肥満と2型糖尿病に対抗します。(3)二次胆汁酸は、腸由来の受容体TGR5の活性化を介してGLP-1/PYYの放出を促進することに加えて、腸由来のFXR受容体を活性化して脂肪生成因子SREBP-1Cの発現を阻害し、抗肥満および抗2型糖尿病効果を発揮します。(4)短鎖脂肪酸はトリメチルアミンレベルを低下させ、それによって肝臓のトリメチルアミンN-オキシド合成を阻害し、心血管疾患のリスクを低下させます。 (B)(1)短鎖脂肪酸は、腸由来のGPCRを活性化することによってT細胞の発達を促進し、加齢に伴う炎症のリスクを低下させます。 (2)短鎖脂肪酸と二次胆汁酸はともに腸管バリアを強化し、リポ多糖の血中への移行を抑制し、炎症反応(例えば、T細胞の活性化、マクロファージの抑制、MyD88/NF-κBを介した炎症性サイトカイン産生の抑制)を弱める。(3)インドール誘導体はマクロファージ上のアリール炭化水素受容体を活性化し、それによってマクロファージの活性と炎症性サイトカイン産生を調節し、累積的な炎症を軽減する。 (C)(1)短鎖脂肪酸はタイトジャンクションタンパク質の発現を増強し、腸管バリアの完全性を強化し、リポ多糖の漏出と炎症促進因子によるミクログリアの活性化を阻害し、それによってアミロイドβとα-シヌクレインの蓄積に対抗し、アルツハイマー病(AD)とパーキンソン病(PD)の病理を軽減する。 (2)短鎖脂肪酸は腸クロム親和性細胞を活性化することでセロトニン(5-HT)分泌を促進し、迷走神経を刺激して中枢神経系の炎症を抑制し、アルツハイマー病とパーキンソン病を軽減します。(3)短鎖脂肪酸は血液脳関門(BBB)を直接通過し、ミクログリアの活性化を阻害し、炎症性物質の蓄積を減らし、アルツハイマー病とパーキンソン病(を改善します。 |
| 腸内細菌叢が肥満に影響を与えるメカニズムは多様である。短鎖脂肪酸は腸由来のGタンパク質共役受容体(GPR41またはGPR43)を活性化し、ペプチドYY(PYY)やグルカゴン様ペプチド1(GLP1)などの満腹促進ホルモンの放出を誘発し、食欲を減少させる(28)。さらに、アッカーマンシア・ムシニフィラや短鎖脂肪酸などの特定の微生物や代謝産物は脂肪組織における脂肪酸酸化を促進し、肥満に対する保護メカニズムを提供する(29)。二次胆汁酸に関しては、デオキシコール酸(DCA)はTGR5受容体の活性化とそれに続くcAMP産生を介して脂肪分解を促進することにより、脂肪組織量を減少させ、高脂肪食(HFD)誘発性肥満を予防することが示されている(30、31)。さらに、デオキシコール酸とリトコール酸(LCA)は、ファルネソイドX受容体(FXR)の活性化を介してステロール調節エレメント結合タンパク質-1C(SREBP-1C、脂質合成の主要な転写調節因子)の発現を抑制することにより肝臓の脂質生成を阻害するが、コール酸などの一次胆汁酸に比べて効力は低い(32)。 |
| 2型糖尿病は、加齢に伴う代表的な代謝性疾患であり、インスリン抵抗性と膵臓β細胞の進行性機能障害を特徴とし、持続性高血糖として現れ、しばしば脂質異常症を伴います(33)。蓄積された証拠は、健康な人と比較して、2型糖尿病患者の腸内マイクロバイオームは多様性と構成の両方で変化を示し、特定の微生物の変化は研究によって異なる可能性があることを示していますが、一般的な傾向についてはコンセンサスが形成されつつあります。分類学的詳細は異なりますが、共通の特徴としては、αおよびβ多様性の低下、ファーミクテスの減少、バクテロイデスの増加が挙げられます。属レベルでは、病原性細菌(例:コプロコッカス、エシェリヒア、レンサ球菌)が増殖し、有益な属(例:ビフィズス菌、アッカーマンシア、ルミノコッカス、乳酸菌、プレボテラ)が減少します(33、34)。腸管バリア機能障害(一般に「リーキーガット」と呼ばれる)は、2型糖尿病の特徴である。この状態は、リポ多糖の全身循環への移行を促進し、NF-κB炎症経路を活性化し、その後インスリン抵抗性を誘発する(33)。アッカーマンシア・ムシニフィラや酪酸産生菌などの有益な微生物は、タイトジャンクションタンパク質を調節することで腸管バリア機能を維持し、2型糖尿病のリスクを低減する(35、36)。別の代謝調節因子である肝臓フラビン含有モノオキシゲナーゼ3(FMO3)は、インスリン抵抗性と高血糖を促進する。注目すべきことに、L.プランタルムとA.ムシニフィラを用いたプロバイオティクス介入は、マウスにおいてFMO3の発現を効果的に抑制し、インスリン感受性を改善した(29)。 2型糖尿病における代謝機能障害の主な原因である腸管糖新生(IGN)障害は、短鎖脂肪酸によって改善され、血糖値を下げることができる(37)。酪酸とプロピオン酸は、それぞれcAMPを介した経路と脂肪酸受容体3(FFAR3)に関連する腸脳神経回路を介して腸管糖新生を活性化し、インスリン感受性の改善やグルコース代謝の促進などの代謝上の利点をもたらす(37、38)。さらに、短鎖脂肪酸はグルコーストランスポーター4(GLUT4)の発現を促進することで末梢でのグルコース取り込みを増強することができる(39)。2型糖尿病における二次胆汁酸の代謝上の利点は、主にTGR5受容体の活性化を介して媒介され、腸管L細胞を刺激してGLP-1を分泌させ、それによってインスリン分泌を増強し、血糖値を低下させる(33、39)。また、トリプトファン由来の微生物代謝産物であるインドールは、異なるメカニズムを介してGLP-1の調節に関与していることが示唆されている(25)。 |
| 肥満や糖尿病以外にも、腸内細菌叢の異常は心血管代謝疾患の発症に寄与しており、特に腸内細菌代謝産物であるトリメチルアミンN-オキシドを介して、高血圧、動脈硬化、心不全との関連が指摘されている(40)。トリメチルアミンN-オキシドは、腸内細菌が食事中のコリンをトリメチルアミンに代謝し、それが肝臓でトリメチルアミンN-オキシドに酸化される際に生成される(41)。また、心血管疾患のある人ではトリメチルアミンN-オキシドレベルが上昇しており、腸球菌や大腸菌などのトリメチルアミンN-オキシド産生腸内細菌叢も有意に増加していることから、腸内細菌叢の異常が心血管疾患の発症に大きく寄与していることが示されている(25、40)。重要なことに、プロバイオティクスや短鎖脂肪酸などの介入は、腸内細菌叢を再構築して循環トリメチルアミンN-オキシドレベルを低下させることで心血管代謝障害を軽減できる有望な候補として浮上している(41)。 |
| 4.免疫老化とマイクロバイオーム |
| 加齢に伴い、免疫系の機能は徐々に低下し、この現象は免疫老化と呼ばれます。この過程は、獲得免疫応答の低下(例えば、ナイーブT細胞の減少や抗体産生の弱化)、感染症への感受性の増加、ワクチン効果の低下を特徴とします(42)。例えば、高齢者は重症インフルエンザのリスクが高く、インフルエンザワクチン接種に対する抗体反応が低下することがよくあります(43)。免疫老化には、慢性的な炎症、いわゆる「炎症性老化」の発症も伴います。これは、急性感染症がなくても、循環する炎症性サイトカインが上昇する状態です(42)。この慢性的な低度炎症は、蓄積された免疫細胞の機能不全と生涯にわたる抗原ストレスに起因すると考えられており、組織の老化や疾患感受性に寄与しています。腸内マイクロバイオームは、生涯を通じて免疫機能の形成と調節において極めて重要な役割を果たしており、加齢に伴うその変化は免疫老化に大きく寄与しています(43)。加齢に伴い、腸内細菌叢の構成と多様性は大きく変化し、免疫老化を悪化させる可能性がある(18)。高齢者集団では、有益な常在細菌(ビフィズス菌や酪酸産生菌などのフィルミクテス門)の減少と、それに伴う日和見病原菌や炎症誘発性微生物の増加が報告されている(44、45)。微生物の多様性は加齢とともに低下する傾向があり、健康な成人の腸で優勢な有益な嫌気性菌(例えば、クロストリジウム属クラスターXIVaに属するフェカリバクテリウム・プラウスニッツィーは減少する(46)。一方、加齢に伴い、腸内で病原性または炎症誘発性の可能性のある分類群(腸内細菌科などの特定のプロテオバクテリアを含む)が増加することが多い(46)。これらのディスバイオシス変化は、粘膜免疫の障害、全身性炎症、感染症に対する脆弱性の増大と関連付けられている(47)。前述のように、加齢に伴い腸内細菌叢は、主要な食物繊維発酵細菌の減少により、酢酸、プロピオン酸、酪酸などの短鎖脂肪酸の産生量が減少します(48)。これらの代謝産物は、腸管上皮の完全性の維持、炎症反応の調節、制御性T細胞(Treg細胞)活性のサポートにおいて重要な役割を果たします(49)。加齢に伴う短鎖脂肪酸産生細菌の減少は、炎症状態を悪化させ、炎症性老化プロセスに寄与することが示されています。例えば、酪酸やその他の短鎖脂肪酸は通常、粘膜免疫をサポートし、抗炎症作用を持つため、これらの減少は炎症に対する重要な制御制約を解除します(50)。短鎖脂肪酸はまた、免疫細胞や上皮細胞上のGタンパク質共役受容体(GPR41、GPR43など)のリガンドとしても機能し、制御性T細胞の発達を促進し、腸管バリア機能を強化します(49、50)。酪酸産生菌(フェカリバクテリウムやローズブリアなど)が減少するディスバイオシス(51、52)では、マクロファージがこれらの正のシグナルを受け取る機会が減る可能性がある。加齢に伴い、胸腺退縮によりナイーブT細胞の産生が自然に減少し、記憶T細胞への依存度が高まる。ディスバイオシスは、腸管バリアが障害されるとエンドトキシンリポ多糖などの微生物代謝産物が全身循環に移行し、自然免疫が継続的に活性化されることで、このプロセスをさらに悪化させる可能性がある(53)。この慢性的な活性化は免疫予備力を枯渇させ、T細胞の老化を加速させる。その結果、短鎖脂肪酸の少ない環境にある老化したマクロファージは、より炎症性ではあるが効果の低い状態にとどまる可能性がある(図2)。 |
| 免疫老化は、獲得免疫と自然免疫の両方に影響を与えます。特に自然免疫系、マクロファージと好中球は、加齢とともに機能が低下します。例えば、マウスでは、高齢個体のマクロファージは、いくつかの点で炎症反応と殺菌反応が低下しています(54)。老化したマクロファージは、刺激を受けた際にプロIL-1βの産生量が少なく、炎症活性化の鈍化を反映しています。ディスバイオシスは、自然免疫応答を調節する微生物由来分子の産生を減少させ、病原体の除去障害と炎症の増加につながります(55)。ディスバイオシスに関連したリポ多糖とペプチドグリカンの循環系への漏出は、マクロファージを常にプライミング状態に維持する可能性があります。これらの炎症刺激への持続的な曝露は、IL-1βの基礎レベルの上昇につながり、炎症性老化と組織損傷に寄与します(IL-1βは、加齢に伴う骨量減少、インスリン抵抗性などに関与しています)。この環境は組織に害を与え(虚弱や臓器機能低下の一因となる)、さらに「先天性免疫疲弊」の一形態を引き起こす可能性があり、過剰刺激の後、マクロファージや好中球の反応性が低下する可能性がある(56)。興味深いことに、マウスでは、腸内細菌叢を若い宿主から高齢の宿主に移植すると、免疫機能が若返り、全身性炎症が軽減されることが実験研究で示されており(57)、宿主の免疫応答の調節における腸内細菌叢の重要な役割が強調されている。本質的に、微生物のトリプトファン代謝物は、過剰に活性化した先天性応答のブレーキとして機能し、慢性炎症の予防に役立つ。特定の腸内細菌は、食事由来のトリプトファンをインドール誘導体(例:インドール-3-アルデヒド、インドールプロピオン酸)に代謝し、免疫細胞上のアリール炭化水素受容体(AhR)に結合することができる。先天性免疫細胞におけるアリール炭化水素受容体の活性化は、免疫調節効果をもたらす傾向がある。例えば、マクロファージにおけるアリール炭化水素受容体刺激は、リポ多糖に対するIL-6や他の炎症性サイトカインの産生を抑制することが示されている(58)。その結果、加齢に伴う腸内細菌叢の異常は免疫系を慢性的に刺激し、炎症性老化の一因となる可能性がある(59)(図2)。 |
| 5.加齢に伴う神経変性疾患と腸内細菌叢 |
| 腸内細菌は、神経機能に影響を与える神経活性物質として、短鎖脂肪酸、アセチルコリン、セロトニン(5-HT)など、様々なシグナル伝達分子を産生する一方、脳はストレスホルモンや自律神経を介して腸内生理機能や腸内細菌叢の組成を調節することができる(60)。この双方向のコミュニケーションは腸-脳軸(GBA)として知られ、腸内細菌叢、免疫系、中枢神経系(CNS)間の相互作用を伴い、正常な脳機能と行動の維持に重要な役割を果たしている。腸-脳軸の調節異常が、アルツハイマー病、パーキンソン病、その他の加齢に伴う認知機能障害などの神経変性疾患の発症に関与していることを示す証拠が増えており、脳の健康と疾患における腸内細菌叢の重要性が強調されている(61、62)。ディスバイオシスは、脳や末梢免疫系に到達する微生物分子を介して、神経炎症や神経病理を引き起こしたり悪化させたりする可能性があります。そのため、研究者たちは現在、加齢に伴うマイクロバイオームの変化が神経変性疾患の発症や進行にどのように寄与するかを調べています。ディスバイオシスを伴う加齢は、腸管透過性の増加、いわゆる「リーキーガット」を引き起こし、エンドトキシンリポ多糖などの細菌成分が全身循環に入ることを可能にします。リポ多糖は血液-脳関門を通過し、神経変性疾患の特徴である神経炎症を引き起こします(63)。例えば、高齢者で最も一般的な認知症であるアルツハイマー病は、慢性神経炎症とアミロイドβミスフォールディング病理を特徴としています。炎症性サイトカイン(例:IL-1β、IL-6)とリポ多糖のレベル上昇は、アミロイドβ凝集とタウ病理を促進することが示されています(64)。注目すべきことに、アルツハイマー病患者は抗炎症性または神経サポート性の微生物(例:乳酸菌、ビフィズス菌、プレボテラ菌)の減少と、ルミノコッカス、特定のプロテオバクテリア、および腸内細菌科などの炎症促進性属の増加を示すことが多い(65、66)。特定の腸内細菌は、宿主のアミロイドを模倣するアミロイド様タンパク質を産生し、脳内のアミロイドβのミスフォールディングと凝集を加速する可能性がある(63)。さらに、アルツハイマー病患者はF. プラウスニッツィーなどの短鎖脂肪酸産生細菌の減少も示している(67)。この微生物の変化は、宿主の神経化学と免疫環境に影響を与える可能性がある。たとえば、有益な微生物の喪失は、脳内で神経保護作用と抗炎症作用を持つ短鎖脂肪酸である酪酸の産生の減少につながる可能性がある。同時に、グラム陰性菌の過剰増殖は、循環血中のエンドトキシンリポ多糖のレベルを上昇させ、全身性炎症を引き起こし、血液脳関門を破壊する可能性がある。このような慢性炎症は、ミクログリア(脳の免疫細胞)を活性化し、脳内でのアミロイドβ凝集を促進することによって、アルツハイマー病の病態形成を促進すると考えられている。これを裏付けるように、アルツハイマー病マウスモデルでは、抗生物質による腸内細菌叢の破壊が神経炎症とアミロイド沈着を変化させることが示され、因果関係が強調されている(68)(図2)。 |
| もう一つの加齢に伴う神経変性疾患はパーキンソン病であり、脳の黒質のドーパミン作動性ニューロンの変性により主に運動制御に影響を及ぼします。パーキンソン病の特徴は、α-シヌクレイン(α-Syn)タンパク質のミスフォールディングと凝集によるレビー小体の形成です。興味深いことに、研究によると、パーキンソン病は部分的に腸管に起因している可能性がある。Braakの仮説では、ミスフォールディングしたα-シヌクレインが最初に腸管神経系に現れ、その後迷走神経を介して脳に移動する可能性があると提唱しています(69)。腸内細菌叢の異常はパーキンソン病と密接に関連しています。症例対照研究では、パーキンソン病患者は、健常対照群と比較して、特定の細菌(例えば、乳酸菌科、エンテロコッカス科、およびバルネシエラ科属など)の増加と抗炎症性細菌(特に、クロストリジウム・コッコイデスなどの短鎖脂肪酸産生クロストリジウム、プレボテラ科、およびバクテロイデス フラジリス)の減少という、著しいディスバイオシスを呈していることが示されています(70)。パーキンソン病における炎症促進性微生物の過剰存在は、リポ多糖やカーリ(細菌性アミロイドタンパク質)などの微生物産物への曝露の増加につながる可能性があります。腸内細菌由来のリポ多糖は、脳内のミクログリアを活性化し、ドーパミン作動性ニューロンの死を促進することが示されています(71)。α-シヌクレイン過剰発現(ASO)マウスを用いた研究では、腸内細菌叢がパーキンソン病の発症に大きく影響することが実証されました。 パーキンソン病の患者から糞便移植を受けたα-シヌクレイン過剰発現マウスは、健康なドナーから移植を受けたマウスと比較して運動症状が悪化した(70)。また、症例報告では、健康なドナーから糞便微生物移植を受けたパーキンソン病の患者が、脚の震えやその他のパーキンソン病の関連症状の一時的な改善を経験したとされている(72)。さらに、最近の疫学研究では、パーキンソン病の患者は短鎖脂肪酸産生細菌の持続的な欠乏を示すことが明らかになったが、短鎖脂肪酸はミクログリアの過剰活性化を防ぐなど、中枢神経系の炎症反応に有益な効果を発揮することが知られている(2)(図2)。 |
| 6.プロバイオティクス、プレバイオティクス、ポストバイオティクスによる抗老化介入 |
| プロバイオティクス、プレバイオティクス、ポストバイオティクスを用いて腸内マイクロバイオームを調節することは、健康的な老化を促進する有望な戦略として注目されています。これらの介入はそれぞれ異なるメカニズムで作用します。プロバイオティクスは有益な微生物を導入し、プレバイオティクスはそれらを養い、ポストバイオティクスはそれらの生物活性代謝産物を供給します。これらが相乗的に作用することで、微生物バランスの回復、代謝障害や免疫機能の向上、全身性炎症の軽減が促進され、健康寿命と長寿の向上に貢献します(図2)。 |
| 乳酸菌やビフィズス菌などのプロバイオティクスは、消化管通過に耐え、微生物バランスに良い影響を与える生きた微生物です。腸の健康維持に加えて、プロバイオティクスの補給は、腸内細菌叢を調節することで、2型糖尿病や心血管疾患などの代謝障害を改善し、インスリンシグナル伝達を強化し、血中コレステロール値を低下させることが報告されています(73)。高齢者では、L. ラムノサスやB. ロンガムなどの菌株が免疫応答を改善し、ワクチンの有効性を高め、感染リスクを低減することが示されています(74、75)。プロバイオティクス補給(例:L. ラムノサス GG、B. ブレーベ、またはL. カゼイ)は、STING/TBK1/NF–κB、IL−10R2/STAT3/SOCS3、およびTLR2/MyD88を含むいくつかのシグナル伝達経路を介して抗炎症性サイトカインの産生を増加させます(76-78)。プロバイオティクス(例:L. プランタルム、L. ラムノサス)は、タイトジャンクションタンパク質のアップレギュレーションにより腸管バリアを強化し、病原体の過剰増殖を防ぎ、クロストリジオイデス・ディフィシル大腸炎などの感染症のリスクを低下させるのに役立ちます(79、80)。 |
| イヌリン、フラクトオリゴ糖(FOS)、ガラクトオリゴ糖(GOS)などのプレバイオティクスは、消化されない食物繊維であり、特にビフィズス菌やF. プラウスニッツィーなどの短鎖脂肪酸産生菌の増殖を選択的に促進します(49、80、81)。短鎖脂肪酸、特に酪酸のレベルが上昇すると、腸管バリア機能が改善され、全身性炎症が軽減され、マクロファージの活性が高まります(61、82)。プレバイオティクスの摂取は、ヒトのグルコース耐性、脂質代謝、インスリン感受性、および免疫機能もサポートします(81、83)。果物、野菜、全粒穀物をベースとした天然繊維が豊富な食事は、炎症の軽減とより健康的な老化の軌跡に関連しています。 |
| ポストバイオティクスとは、短鎖脂肪酸、ペプチド、酵素、多糖類、細胞壁成分など、生存能力のない微生物細胞またはその代謝産物を指します(84、85)。プロバイオティクスとは異なり、ポストバイオティクスは感染のリスクがないため、虚弱な高齢者や免疫不全の高齢者に適しています(84)。ポストバイオティクスは、宿主の代謝と炎症を調節することで、代謝障害を軽減する上で大きな可能性を示しています。具体的には、エネルギー消費を増加させ、脂肪生成を抑制し、グルコース処理を改善すると同時に、脂質吸収と炎症経路にも作用し、肥満とインスリン抵抗性を改善します(86)。短鎖脂肪酸に加えて、デオキシコール酸やリトコール酸などの二次胆汁酸は、FXRおよびTGR5受容体を介して免疫応答を調節し、抗炎症性サイトカインIL-10の産生を促進し、NF-κBを介した炎症を抑制します(87)。加齢に伴うディスバイオシスは二次胆汁酸の産生を阻害し、免疫老化と炎症性老化に寄与する可能性があります。 |
| 免疫以外にも、これらの介入は腸-脳軸を介して神経変性疾患に有望である。プロバイオティクス株(ビフィズス菌、乳酸菌、アッケルマンシアなど)およびプロバイオティクスカクテルは、アルツハイマー病、パーキンソン病、筋萎縮性側索硬化症のモデルにおいて神経炎症の軽減と認知機能の改善に有望であることが示されている(88)。小規模な臨床および前臨床研究では、ビフィズス菌およびL.プランタルムの補給後に認知障害(MCI)および軽度アルツハイマー病に認知上の利点があることが示されている(89、90)。一方、9つのランダム化比較試験(患者663人)のメタ分析では、統一パーキンソン病評価尺度(UPDRS)運動スコアの改善、便秘、不安、うつ病の軽減など、運動症状の有意な改善が示されている(91)。さらに、食物繊維、ポリフェノール、発酵食品、不飽和脂肪酸が豊富な地中海食は、腸内細菌叢を調節し、短鎖脂肪酸などの有益な代謝物を増加させることで神経保護効果を発揮し、神経炎症や神経変性病理を軽減します(92)。二次胆汁酸も神経炎症やミクログリア活性に影響を与え、アルツハイマー病では二次胆汁酸プロファイルの変化が観察されています(93)(図2)。 |
| プロバイオティクスとプレバイオティクスを組み合わせたシンバイオティクス介入は、相乗効果をもたらす可能性があります。動物実験では、シンバイオティクス療法は、どちらか一方の成分単独よりも効果的に寿命を延ばしました(94)。人間の長寿に関する直接的な証拠は限られていますが、これらの戦略は炎症マーカー、代謝の健康、および免疫機能を改善し、これらすべてが健康寿命の延長に貢献します。特に、百歳以上の人は、炎症の軽減とともに、短鎖脂肪酸産生菌と乳酸菌が豊富な腸内マイクロバイオームプロファイルを特定しています(95)。臨床的には、バイオティクスベースの治療法は、加齢に伴う疾患の管理のために評価されています(96)。食物繊維が豊富で多様な食事は、有益な腸内細菌叢をサポートし、加齢に伴う結果を改善するための低コストで効果的なアプローチであり続けています(97)。キムチ、ヨーグルト、ケフィア、ザワークラウトなどの発酵食品は、プロバイオティクスとポストバイオティクスの便利な食品ベースの供給源となります(98)。将来的には、個々のマイクロバイオームプロファイルに基づいた、パーソナライズされたシンバイオティクス療法が開発される可能性がある。これらのマイクロバイオームに基づく戦略を、個々の栄養療法や治療法に戦略的に統合することで、代謝障害の軽減、免疫老化の遅延、認知機能の維持、そして健康寿命の促進といった、システムレベルでのアプローチが可能になるかもしれない。 |
| 7.考察と結論 |
| 腸内マイクロバイオームと加齢関連疾患との複雑な相互作用は、加齢研究における重要な分野として急速に注目を集めている。本レビューでは、多様性の低下、短鎖脂肪酸産生菌の減少、病原性細菌の過剰増殖など、加齢に伴う腸内マイクロバイオームの主要な変化を体系的に解明する。これらの変化は、代謝、免疫、神経内分泌経路を介して宿主の恒常性を阻害し、様々な加齢関連疾患の発症と進行に寄与する。 |
| プロバイオティクス、プレバイオティクス、ポストバイオティクスなどの腸内細菌叢を標的とした介入は、前臨床研究において老化プロセスを調節する可能性を示している(1)。これらの戦略は、免疫監視の強化、腸管バリアの強化、全身性炎症の軽減、神経認知機能のサポートなど、潜在的な利点をもたらす。さらに、糞便微生物移植などのヒトにおける新たなトランスレーショナル研究は、腸内細菌叢の構成と高齢者の代謝および認知機能の結果との関連性を示す予備的な因果関係の証拠を提供している。百歳以上の高齢者の研究では、短鎖脂肪酸産生細菌と抗炎症性代謝産物が豊富な独自の腸内微生物シグネチャーが一貫して明らかにされており、マイクロバイオームに基づく長寿メカニズムの可能性についての洞察を提供している。しかし、このような介入の臨床応用は、いくつかの課題によって依然として制限されている。まず、環境、遺伝的背景、食事、ライフスタイル、およびベースラインの微生物プロファイルによって影響を受ける腸内微生物組成の個人差は、単一の菌株または代謝産物を使用した「万人向け」のアプローチの有効性が限られていることを示唆しています。最近の研究では、食事パターン、多剤併用、および併存疾患がマイクロバイオーム老化研究における主要な交絡因子として作用し、因果関係の解釈を複雑にしていることも強調されています(2、92、99)。第二に、動物モデルでは若いドナーから高齢ドナーへの糞便微生物移植が加齢に伴う炎症や疾患を逆転させており(26)、高齢者を対象とした初期段階の臨床研究では加齢に伴うサルコペニアに対する有望な効果が報告されていますが(100)、既存のヒトデータのほとんどは相関関係にとどまり、メカニズム的な因果関係はまだ確立されていません。これらの課題に対処するには、管理された摂食試験、無菌動物モデル、遺伝子組み換え微生物、管理された摂食試験、および長期的なヒトコホート研究を統合し、微生物の影響を生活習慣や治療に関連する変数から切り離す必要がある。特に、遺伝子組み換えプロバイオティクスや新規ポストバイオティクス送達システムに関する安全性および規制上の問題にも対処しなければならない。 |
| これらの課題にもかかわらず、腸内マイクロバイオーム調節の治療的可能性は大きい。この分野が精密マイクロバイオーム医療へと移行するにつれて、今後の研究では以下の点を優先すべきである。(1) マルチオミクス技術(メタゲノミクス、メタボロミクス、シングルセルシーケンス、宿主トランスクリプトミクス)を統合して、予測可能な加齢関連微生物バイオマーカーとその動的な制御ネットワークを特定すること。(2) 個別化されたプロバイオティクスの組み合わせの設計を導くための、AI ベースの腸内マイクロバイオームプロファイリングなどの精密介入戦略を開発すること。(3) 有効性を高めるための新しい送達システム(例えば、短鎖脂肪酸のナノ粒子カプセル化や次世代の遺伝子操作プロバイオティクス)を探索すること。(4) 腸内マイクロバイオーム介入が高齢者の健康寿命と回復力に及ぼす長期的な影響を判断するために、大規模な縦断的コホート研究を実施すること。 |
| 結論として、腸内マイクロバイオームは、加齢生理のバイオセンサーとして、また治療介入の軸として機能します。百歳以上の高齢者の生物学、糞便微生物移植試験、そしてトランスレーショナルオミクスからの知見を取り入れることで、この分野は相関関係から因果関係、そして臨床応用へと発展していく態勢が整っています。マイクロバイオームに基づく介入を個別化された高齢者医療に戦略的に統合することは、老化を遅らせ、疾患負担を軽減し、健康的な加齢を促進するための有望なシステムレベルのアプローチとなります。 |
| 参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
| この文献は、BMB Rep. 2026 Jan 31;59(1):40–50. に掲載されたAging and the microbiome: implications for health and disease.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |