ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(アロニア:研究の最前線) |
アロニアベリーエキスの抗がん効果は、 大腸がんにおいてChk1とp53を介して媒介される |
Yoh Asahi , Caiming Xu , Keisuke Okuno , Akinobu Taketomi , Ajay Goel |
|
|
| 要約 |
| 背景:アロニアベリーエキス(ABE)は、その高いポリフェノール含有量から、大腸がん(CRC)を含む様々な悪性腫瘍に対して顕著な抗がん作用を示すことが近年報告されています。しかしながら、大腸がんにおけるアロニアベリーエキスの抗がん作用の分子メカニズムは未だ解明されておらず、がん治療における補完医療としての使用を検討する際には、この点を考慮することが重要です。 |
| 方法:大腸がん細胞におけるアロニアベリーエキス治療に関連する特異的な増殖シグナル伝達経路を同定するため、ゲノムワイドトランスクリプトームプロファイリング(訳者注:「ゲノムワイド・トランスクリプトーム・プロファイリング」とは、特定の条件下(疾患、薬物刺激、発育段階など)において、細胞内や組織内で発現しているすべてのRNA(トランスクリプトーム)をゲノム全体にわたって網羅的に測定・解析する手法です。)とパスウェイエンリッチメント解析(訳者注:パスウェイエンリッチメント解析(Pathway Enrichment Analysis)は、RNA-seqやマイクロアレイなどで得られた数千〜数万の遺伝子リストから、「特定の生物学的機能や代謝経路(パスウェイ)に共通して関わる遺伝子が、偶然以上に集まっているか」を統計的に判定する手法です。膨大な発現変動遺伝子のリストを、解釈しやすい「生命現象の単位」へと要約し、疾患のメカニズムや薬の作用機序を解明するために用いられます。)を実施しました。さらに、SW480(訳者注:SW480(またはSW-480)は、主に生物医学研究で使用されるヒト結腸腺がん(大腸がん)由来の細胞株です。1970年代に50歳の白人男性の原発巣から樹立され、がんの増殖、転移メカニズム、薬物耐性の研究において世界中で広く利用されています)およびHCT116 (訳者注:HCT116は、ヒト結腸癌(大腸がん)由来の上皮細胞様接着細胞株であり、がん研究、特にも分子メカニズム、薬剤耐性、および細胞増殖の解析において広く使用されるモデル細胞です。KRAS遺伝子変異を持ち、二倍体に近く安定したゲノムプロファイルを持つため、3D培養技術によるスフェロイド形成など、がん治療の基盤研究に利用されます。)大腸がん細胞株におけるアロニアベリーエキスの抗がん作用を調査するため、一連の体系的かつ包括的な細胞培養研究を実施しました。その後、これらの知見は患者由来3Dオルガノイド(PDO)モデル(訳者注:3Dオルガノイド(PDO:Patient-Derived Organoid)モデルとは、患者の生体組織(がん組織や正常組織)から直接作製された、3次元(3D)の「ミニ臓器」のことです。)において検証されました。 |
| 結果:トランスクリプトームプロファイリング解析により、p53(訳者注:p53は、細胞のDNA損傷やストレスを検知して細胞周期停止、修復、またはアポトーシス(自死)を誘導し、がん化を防ぐ最も重要ながん抑制遺伝子(タンパク質)です。17番染色体に位置し、その機能不全や変異は半数以上のヒトがんで見られ、「ゲノムの守護者」と称されます)シグナル伝達がアロニアベリーエキスの抗がん活性を媒介する主要な経路の一つであることが同定されました。公開データセットの解析により、p53の主要制御因子であるChk1(訳者注:Chk1(チェックポイントキナーゼ1)は、DNA損傷時に細胞周期(S期、G2/M期)を停止させ、修復を行うセリン/スレオニンプロテインキナーゼです。ATRによって活性化され、CDC25をリン酸化してCDK1を抑制することで分裂を止め、細胞の生存維持とゲノム安定性に不可欠な役割を果たします )が大腸がんにおけるアロニアベリーエキスの重要な標的の一つであることが明らかになりました。アロニアベリーエキス処理によりChk1およびp53の活性化が低下し、細胞周期停止(p = 0.003 – 0.014)およびDNA損傷の増強(p = 0.015 – 0.026)が誘導されました。さらに、これらの知見は3Dオルガノイド(PDO)モデルにおいても検証され、アロニアベリーエキス処理により濃度依存的に3Dオルガノイド(PDO)モデルが有意に減少し、サイズも小さくなりました(p = 0.045 - <0.001)。 |
| 結論:まず、p53シグナル伝達経路がアロニアベリーエキスの抗がん活性のメディエーターとしての役割を示すエビデンスを示し、大腸がんにおける安全かつ効果的な統合医療アプローチとしてアロニアベリーエキスを使用する根拠を示した。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.材料および方法 |
| 2.1.細胞培養および試薬 |
| 2.2.細胞生存率 |
| 2.3.遊走アッセイ |
| 2.4.コロニー形成アッセイ |
| 2.5.細胞浸潤アッセイ |
| 2.6.酸化ストレスおよびアポトーシスアッセイ |
| 2.7.RNA抽出、ゲノムワイドトランスクリプトームプロファイリング、および遺伝子セットエンリッチメント解析 |
| 2.8.リアルタイム定量逆転写PCR(RT-qPCR)アッセイ |
| 2.9タンパク質抽出およびウェスタンブロット法 |
| 2.10.DNA損傷および細胞周期アッセイ |
| 2.11.遺伝子発現データセットの解析 |
| 2.12.患者由来3D腫瘍オルガノイド(PDO) |
| 2.13.統計解析 |
| 3.結果 |
| 3.1.アロニアベリーエキスは、大腸がん細胞において、細胞増殖、遊走、クローン形成能、および浸潤を阻害することにより抗腫瘍効果を示した |
| 3.2.アロニアベリーエキス誘導による大腸がん細胞における活性酸素種(ROS)蓄積とアポトーシスの促進 |
| 3.3.トランスクリプトーム解析により、大腸がん細胞におけるアロニアベリーエキス処理後のp53シグナル伝達経路の関連性が明らかになった |
| 3.4.アロニアベリーエキスは大腸がん細胞におけるChk1のリン酸化を阻害した |
| 3.5.アロニアベリーエキスは大腸がん細胞において細胞周期停止を引き起こし、DNA損傷を増強した |
| 3.6.アロニアベリーエキスによる治療は、大腸がん患者由来3Dオルガノイド(PDO)モデルにおいて抗がん活性を示した |
| 4.考察 |
本文 |
| 1.はじめに |
| 大腸がんは、世界中でがん関連死亡の主要な原因であり、肺がんに次いで2番目に多い疾患です。2021年には、新規患者数が104,270人、死亡者数が52,980人と推定されています (Siegel et al., 2021; Sung et al., 2021)。大腸がん患者の死亡率の主な原因は、転移を伴う進行期に診断され、治癒を目指した手術が必ずしも可能ではないことです。手術の適応がない大腸がん患者には、全身性細胞傷害性療法がしばしば提供されます。大腸がんの管理における治療レジメンの改善は進んでいますが、薬剤耐性の獲得、毒性、そして過剰な費用のために、これらの治療の全体的な有効性は著しく損なわれています。最近では、多くの食事由来の天然化合物が、大腸がんを含む様々ながんにおける安全性、費用対効果、そして従来の治療法との相乗効果から、補完医療・代替医療アプローチとして研究上の関心が高まっています(Goel and Aggarwal, 2010; Goel et al., 2008b; Okuno et al., 2022)。生物学的観点から見ると、このような天然化合物は、強力な抗炎症作用と抗酸化作用を持つポリフェノールを豊富に含んでいることが多く、複数の増殖シグナル伝達経路に直接的または間接的に影響を及ぼす能力があるため、複数のシグナル伝達経路への効果から魅力的な補助抗がん剤となっています(Goel et al., 2008b; Okuno et al., 2022)。 |
| こうした天然化合物の中でも、多様なポリフェノールを豊富に含み、大腸がんを含む様々な悪性腫瘍の治療効果を相乗的に高める能力があることから、様々なベリー類が統合的・補完療法として注目を集めています(Pan et al., 2015; Wang et al., 2011; Wang et al., 2013)。 アロニアベリー(学名:Aronia melanocarpa)は、ブラックチョークベリーとも呼ばれ、北米原産の小さく濃い色のチェリーのような果実です。アロニアベリーには抗酸化作用、抗炎症作用、抗菌作用があり、様々な疾患の治療に有益です。実際、アロニアベリーは、いくつかのがんにおいて有望な抗がん作用を示しているベリー類でもあります。ポリフェノール含有量はベリーの種類によって異なるため(Del Rio et al., 2010)、その有効性は悪性腫瘍ごとに異なります(Bouyahya et al., 2022)。例えば、アロニアベリーエキスは、HT-29(訳者注:HT-29は、1964年に44歳の女性の原発性結腸腫瘍から樹立された、広く使用されているヒト結腸直腸腺癌の付着性細胞株です。成熟した腸細胞の特徴を持ち、癌研究、特に分化や化学療法薬の感受性、異種移植モデルに利用されています。 )大腸がん細胞における増殖阻害において、ビルベリーやブドウ種子エキスと比較して有意に強力な抗がん作用を示しました(Zhao et al., 2004)。さらに、Gaoらは最近、アロニアベリーエキスがブルーベリーやハスカップベリーのエキスと比較して、HepG2(訳者注:HepG2は、ヒトの肝細胞癌(または肝芽腫)由来の代表的な永久培養細胞株です。肝細胞の代謝・合成機能を維持しているため、薬物の肝毒性評価、代謝試験、癌研究、栄養学研究のモデルとして世界中で広く利用されています。)ヒト肝がん細胞において優れた抗酸化作用を発揮することを明らかにし、その研究結果を発表しました(Gao et al., 2018)。同様に、他の研究では、アロニアベリージュースがヒト大腸がん細胞HT-29およびCaco-2(訳者注:Caco-2(カコ・ツー)は、ヒトの大腸癌(結腸癌)由来の細胞株ですが、培養すると小腸の上皮細胞(腸管吸収細胞)に近い性質を持つようになるため、創薬研究において「腸からの薬の吸収しやすさ」を評価する世界的なデファクトスタンダード(標準モデル)として利用されています。)において細胞周期停止を引き起こすことが実証されています(Bermudez-Soto et al., 2007)。さらに、アロニアベリーエキスはHeLa細胞(ヒト子宮頸がん細胞)において細胞増殖を阻害し、活性酸素種(ROS)の産生を増加させることが明らかになっており(Rugina et al., 2012)、抗酸化活性が抗がん効果のもう一つの強力なメカニズムである可能性を示唆しています。近年、アロニアベリーエキスの潜在的な抗がん作用に関する文献は増えていますが、大腸がんにおけるアロニアベリーエキスの分子メカニズムについては、まだほとんど解明されていません。したがって、アロニアベリーエキスの抗がん作用の分子的基盤を解明することは、その潜在的な標的をより深く理解するために重要であり、大腸がん患者やその他の悪性腫瘍患者に対する統合医療アプローチとしてアロニアベリーエキスを使用するための、より具体的な根拠を与えるでしょう。 |
| 本研究では、大腸がん細胞株を用いて、細胞生存率、コロニー形成、遊走、細胞浸潤、酸化ストレス、アポトーシスなどの包括的かつ体系的な機能実験を実施し、患者由来3Dオルガノイドを用いてこれらの結果を検証することで、アロニアベリーエキスの抗がん効果を評価しました。さらに、p53シグナル伝達経路とアロニアベリーエキスの抗がん効果との関連性を明らかにするため、ゲノムワイドトランスクリプトームプロファイリングと遺伝子セットエンリッチメント解析を実施しました。これらの研究の結果、chk1およびp53経路が大腸がんにおけるアロニアベリーエキスの抗がん効果の媒介において重要な役割を果たしていることが明らかになりました。 |
| 2.材料および方法 |
| 2.1.細胞培養および試薬 |
| ヒト大腸がん細胞株(SW480およびHCT116)は、米国タイプカルチャーコレクション(ATCC;米国バージニア州マナサス)から入手した。大腸がん細胞株は、10%ウシ胎児血清(FBS;Gibco)および1%ペニシリン-ストレプトマイシン(Sigma Aldrich、米国ミズーリ州セントルイス)を添加したダルベッコ改変イーグル培地(DMEM;Gibco、カリフォルニア州カールスバッド)中で、37℃、5% CO2のインキュベーター内で培養した。接着細胞の回収には、0.05%トリプシン-0.03% EDTA(Invitrogen、米国カリフォルニア州カールスバッド)を用いた。細胞培養培地は2~3日ごとに補充した。 |
| アロニアベリーエキス(ABE;EuroPharma USA(ウィスコンシン州グリーンベイ)より提供)のストック溶液をジメチルスルホキシド(DMSO;Sigma Aldrich)に5 mg/mLの濃度で溶解し、-20℃で凍結保存した後、全ての実験に使用しました。 |
| 2.2.細胞生存率 |
| 大腸がん細胞株の細胞生存率を定量化するために、96ウェルフラットプレートに1ウェルあたり5×103個の細胞を播種し、18時間インキュベートして細胞株をプレート表面に接着させた。その後、細胞を様々な濃度のアロニアベリーエキスで処理した。アロニアベリーエキス処理48時間後、各ウェルにMTT溶液(5 mg/ml、Sigma Aldrich)20 μlを加え、さらに2時間インキュベートした後、培地を廃棄した。 細胞株をリン酸緩衝生理食塩水(PBS)で洗浄した後、各ウェルにDMSO 200 μlを加え、細胞株が完全に溶解するまでピペッティングした。マイクロプレートリーダー(Tecan Trading AG、Männedorf、スイス)を用いて、各ウェルの吸光度を435 nmで測定した。 |
| 2.3.遊走アッセイ |
| 大腸がん細胞株を遊走アッセイ用に6ウェル培養プレートで培養し、90%コンフルエントになるまで観察した。滅菌済みの200μlマイクロピペットチップを用いて細胞単層に傷をつけることで「創傷」を作製した。傷ついた細胞はリン酸緩衝生理食塩水で洗浄して除去した。その後、細胞を異なる濃度のアロニアベリーエキスで処理した。培養大腸がん細胞株の画像は、オリンパス倒立顕微鏡(倍率40倍)を用いて0時間および24時間後に撮影し、Image-J 1.53sソフトウェア(http://imagej.nih.gov/ij/index.html)を用いて解析し、創傷閉鎖率を算出した。すべての実験は3回繰り返して実施し、代表的な画像を提供した。 |
| 2.4.コロニー形成アッセイ |
| 異なる濃度のアロニアベリーエキス(IC25およびIC50)で48時間処理した大腸がん細胞株を用いて、コロニー形成アッセイを実施した。本アッセイでは、6ウェルプレートにおいて、前処理済みの細胞5×102個/ウェルを異なる濃度のアロニアベリーエキスで1週間インキュベートした。細胞は100%メタノールで30分間細胞培養プレートに固定し、1%クリスタルバイオレットで一晩染色した。コロニー面積はImage-J 1.53sソフトウェアを用いて算出した。 |
| 2.5.細胞浸潤アッセイ |
| 異なる濃度のアロニアベリーエキス(IC25およびIC50)(訳者注:IC50(半数阻害濃度)は、酵素や細胞などの生物学的活性を50%阻害するのに必要な薬物・化合物の濃度です。薬理学や創薬において、薬剤の強さや有効性を示す代表的な指標であり、値が低いほど強い阻害効果(高い活性)を持つことを意味します。)で48時間処理した大腸がん細胞株を用いて、細胞浸潤アッセイを実施した。本アッセイでは、8.0μm PETメンブレンを装着したマトリゲル浸潤チャンバー(Corning社、カリフォルニア州テハマ郡)に、1ウェルあたり1.0×105個の前処理済み細胞を播種した。48時間インキュベーション後、浸潤細胞を固定し、Diff-Quick染色法を用いて染色した。細胞株の画像は、オリンパス倒立顕微鏡(倍率40倍)で撮影し、細胞数を測定した。 |
| 2.6.酸化ストレスおよびアポトーシスアッセイ |
| 大腸がん細胞株を用いて、アロニアベリーエキス処理24時間後に酸化ストレスおよびアポトーシスアッセイを実施しました。酸化ストレスおよび細胞アポトーシスレベルは、Muse Cell Analyzer(Millipore Corp、マサチューセッツ州ビレリカ)と酸化ストレスキット、およびAnnexin V & Dead Cell Kitを用いて、製造元の指示に従って評価しました。 |
| 2.7.RNA抽出、ゲノムワイドトランスクリプトームプロファイリング、および遺伝子セットエンリッチメント解析 |
| RNAシーケンシング(RNA-seq)は、既報(Roy et al., 2022)に従って実施した。阻害濃度25(IC25)のアロニアベリーエキスまたはDMSOで24時間処理した後、miRNeasyキット(Qiagen、ドイツ、ヒルデン)を用いて各細胞株からtotal RNAを抽出した。抽出したRNAに対し、SureSelect XT HS2 mRNAライブラリ調製キット(Agilent、米国カリフォルニア州サンタクララ)を用いて、製造元の指示に従い、total RNA最大1μgを用いて次世代シーケンシング(NGS)ライブラリを構築した。各サンプルから1μgのRNAを用いて、TruSeq RNAサンプル調製キット(Illumina、米国カリフォルニア州サンディエゴ)を用いてリボソームRNA除去ライブラリを作成した。ライブラリ産物のサイズ分布と濃度は、Bioanalyzer DNA High Sensitivity Kit(Agilent Technologies、米国カリフォルニア州サンタクララ)を用いて測定し、ペアシーケンシング(両端150bp)により検証しました。解析にはHiSeq X-TENシステム(Illumina、米国カリフォルニア州サンディエゴ)を使用しました。RNA-seqのすべての手順は2回繰り返して実施しました。 |
| RNAシーケンシング(の解析では、アライメント前にTrim Galoreを使用してFastQファイルをトリミングし、アダプター配列と品質スコアが30未満の3'塩基を削除しました。トリミングされたリードはヒトゲノムバージョンGRCH38にマッピングされ、STARを使用してダウンロードしてアライメントファイルを生成しました。edgeRソフトウェアパッケージを使用して、差次的調節遺伝子を解析しました。アップレギュレーションおよびダウンレギュレーション遺伝子は、P値<0.05および|log2Foldchange|(|log2FC|)> 0.5の閾値によって選択されました。2つの細胞株間で共通する差次的調節遺伝子は、DAVIDオンラインツール(https://david.ncifcrf.gov/summary.jsp)[25]を介したGene Ontology(GO)およびKyoto Encyclopedia of Genes and Genomes(KEGG)遺伝子セットエンリッチメント解析に使用され、CRC細胞でABEの影響を受ける最も関連性の高いシグナル伝達経路が決定されました。 R でのパスウェイの視覚化にはパッケージ「ggplot2」を使用しました。 |
| 2.8.リアルタイム定量逆転写PCR(RT-qPCR)アッセイ |
| 様々な濃度のアロニアベリーエキスで24時間処理した大腸がん細胞株から全RNAを抽出した。RNAは、高容量逆転写キット(Thermo Fischer Scientific、マサチューセッツ州ウォルサム)を用いて相補DNA(cDNA)に逆転写された。qRT-PCRアッセイは、SensiFAST SYBR Lo-ROXキット(Bioline、英国ロンドン)およびQuantStudio 6/7 Flex RT-PCRシステム(Applied Biosystems、カリフォルニア州フォスターシティ)を用いて実施した。本研究で使用したプライマーは補足表S1に示す。Delta Ct値を用いて、β-カテニンをハウスキーピング遺伝子として遺伝子発現レベルの差を算出した。 |
| 2.9.タンパク質抽出およびウェスタンブロット法 |
| β-アクチン(1:1000、#58169; Cell Signaling Technology, Danvers, MA, USA)、p-Chk1(1:1000、#2348; Cell Signaling Technology)、Chk1(1:1000、#60277–1-Ig; Proteintech, Chicago, IL, USA)、p-p53(1:1000、#9286; Cell Signaling Technology)、p53(1:1000、#sc-126; Santa Cruz, CA, USA)に対する一次抗体、および二次抗体(#7074または#7076; Cell Signaling Technology)を用いてウェスタンブロット法を実施した。プロテアーゼ阻害剤カクテル(Thermo Fischer Scientific)を含むRIPA Lysis and Extraction Bufferを用いて、異なる濃度のアロニアベリーエキスで24時間処理した大腸がん細胞株から全タンパク質を抽出した。タンパク質は10% Mini-PROTEAN TGX™プレキャストゲル(BIO-RAD、米国カリフォルニア州ハーキュリーズ)で分離し、ニトロセルロース膜に転写した。膜は、0.1% Tween-20(Sigma-Aldrich)を含むトリス緩衝生理食塩水(Bio-Rad、米国カリフォルニア州ハーキュリーズ)中の5%ウシ血清アルブミン(Sigma-Aldrich)で室温(RT)で1時間ブロッキングした後、一次抗体(1:1000)で4℃で一晩インキュベートした。0.1% TBSTで3回洗浄した後、膜は二次抗体(1:2000)で室温で1時間インキュベートした。免疫ブロットは、ChemiDoc-MP Imagingシステム(バージョン5.2.1、Bio-Rad)を用いて、HRPベースの化学発光キット(Thermo Fisher Scientific)で可視化した。 β-アクチンを内部コントロールとして使用し、相対的なタンパク質レベルをImage-J 1.53s ソフトウェアで定量化しました。 |
| 2.10.DNA損傷および細胞周期アッセイ |
| 大腸がん細胞株におけるDNA損傷アッセイは、アロニアベリーエキス処理48時間後に免疫蛍光法およびフローサイトメトリーにより実施した。免疫蛍光法では、6cm平板プレートの各ウェルにスライドを1枚ずつ播種し、ウェルあたり5×105個の細胞を播種した。18時間インキュベーション後、細胞を異なる濃度のアロニアベリーエキスで処理した。細胞は4%パラホルムアルデヒドで固定し、0.5% Triton X-100で透過処理した。ブロッキングには5%ヤギ血清を含むPBSを用いた。細胞は一次抗体p-H2AX(1:1000、#05-636; Proteintech, Temecula, CA, USA)で一晩インキュベートし、0.1% PBSTで3回洗浄した。細胞を蛍光標識二次抗体(1:1000希釈)で1時間インキュベートし、3回洗浄した後、細胞核を染色した。細胞は、励起波長488 nm、蛍光波長496 nmの蛍光顕微鏡を用いて、マイクロプレートリーダー(Tecan Trading AG)で160倍の倍率で観察した。 |
| 細胞周期キットとH2A.X活性化デュアル検出キットは、製造元の指示に従って、Muse Cell Analyzer (Millipore Corp) によるフローサイトメトリー分析に使用されました。 |
| 2.11.遺伝子発現データセットの解析 |
| 本研究では、公開されている3つの遺伝子発現データセット(The Cancer Genome Atlas (TCGA; n = 327)、GSE104645 (n = 181)、およびGSE159216 (n = 171))から大腸がん症例679例を解析しました。TCGAデータは、カリフォルニア大学サンタクルーズ校のXena Browser (https://xenabrowser.net/) からダウンロードしました。GSE104645およびGSE159216データセットは、Gene Expression Omnibusデータベース (https://www.ncbi.nlm.nih.gov/geo/) からダウンロードしました。 |
| 2.12.患者由来3D腫瘍オルガノイド(PDO) |
| 大腸がん患者由来の3次元(3D)オルガノイドは、既報(Okuno et al., 2022; Ravindranathan et al., 2018; Sharma et al., 2020; Zhao et al., 2022a; Zhao et al., 2022b)に従って作製した。患者はヘルシンキ宣言に基づき匿名でコード化された。患者からは書面によるインフォームドコンセントが得られ、すべての実験はCity of Hopeの倫理委員会(IRB)の承認を得た。3次元(3D)オルガノイドは、上皮成長因子(STEMCELL Technologies)を含むIntestiCult™オルガノイド増殖培地(#06010、STEMCELL Technologies)を含む40μlのマトリゲル(Corning、米国カリフォルニア州テハマ郡)でドーム状に播種し、24ウェルプレートに播種した。ドーム周囲にIntestiCult™オルガノイド増殖培地750μlを添加した。3次元(3D)オルガノイドを異なる濃度のアロニアベリーエキスで48時間処理した。100μmを超える3次元(3D)オルガノイドを観察し、Image-J 1.53sソフトウェアを用いて3次元(3D)オルガノイドの数とサイズを計算した。 |
| 2.13.統計解析 |
| すべてのデータは平均値±標準偏差(SD)で表されます。データの正規性検定には、Shapiro–Wilk検定を用いました。異なる群間の連続値間の差を比較するための統計解析には、JMPソフトウェア(JMP Pro、バージョン16、SAS Institute Inc.、ノースカロライナ州キャリー)を用いて、両側スチューデントt検定を実施しました。p値は、3群間の比較においてHolm法を用いて調整しました。P < 0.05を統計的に有意としました。 |
| 3.結果 |
| 3.1.アロニアベリーエキスは、大腸がん細胞において、細胞増殖、遊走、クローン形成能、および浸潤を阻害することにより抗腫瘍効果を示した |
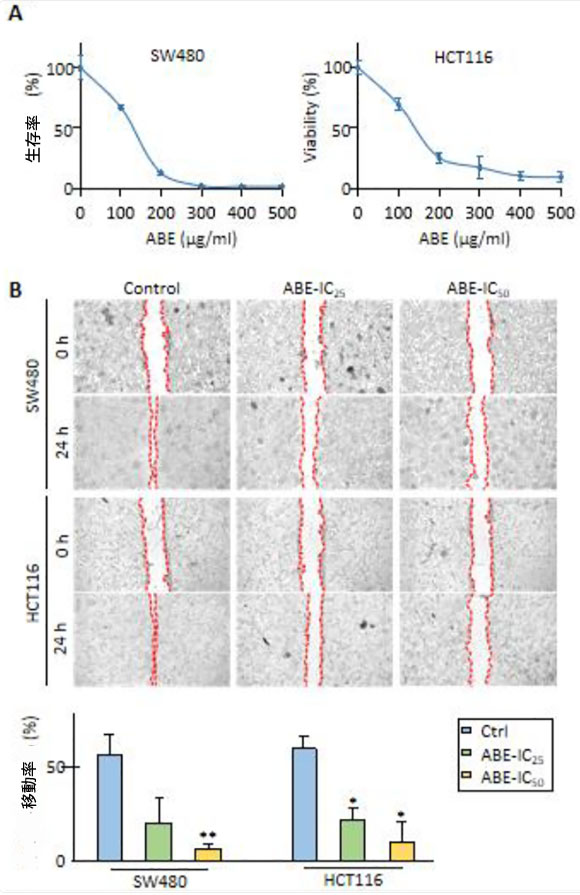
| 本研究の主目的は、大腸がん細胞株におけるアロニアベリーエキスの抗腫瘍効果を検討することである。2種類の異なる大腸がん細胞株、SW480(マイクロサテライト安定)およびHCT116(マイクロサテライト不安定)を用いて実験を行った(訳者注:マイクロサテライト(Microsatellite)は、DNA配列中の2〜6塩基の短い単位が数〜数十回繰り返される反復配列(STR)のこと。ゲノム全体に広く散在し、反復回数に個人差(多型)が出やすいため、DNA鑑定、血縁関係の調査、がんの診断(高頻度マイクロサテライト不安定性: MSI-High)などに利用される )。まず、大腸がん細胞株の細胞生存率に対するアロニアベリーエキスの影響を検討するため、MTTアッセイ(訳者注:MTTアッセイは、細胞のミトコンドリア内にある還元酵素(デヒドロゲナーゼ)が、黄色のテトラゾリウム塩(MTT)を紫色の不溶性ホルマザン結晶へ還元する反応を利用した、生細胞の生存率や増殖率を測定する比色定量法です)を実施した。その結果、用量依存的にアロニアベリーエキスの抗増殖効果が認められ、両大腸がん細胞株において増殖抑制および細胞生存率の阻害が示された。 SW480細胞における1/4および1/2最大阻害濃度(IC25およびIC50)は、それぞれ80.0 μg/mLおよび130.0 μg/mL、HCT116細胞では80.0 μg/mLおよび140.0 μg/mLであった(図1A)。したがって、以降の実験では、IC25およびIC50濃度をそれぞれ80.0 μg/mLおよび140.0 μg/mLとした。 |
 |
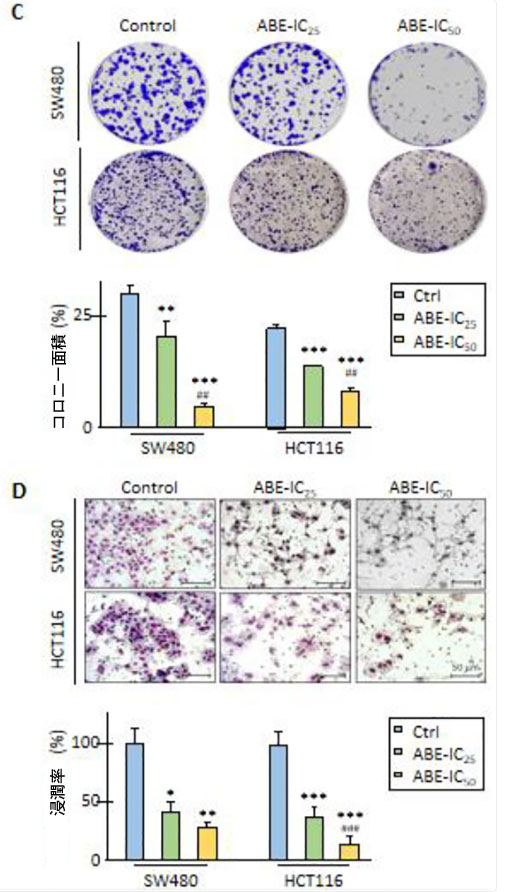 |
図1:大腸がん細胞におけるアロニアベリーエキスの抗がん効果。 (A)折れ線グラフは、異なる濃度のアロニアベリーエキスで48時間処理した後のSW480細胞株とHCT116細胞株の細胞生存率を測定したMTTアッセイの結果を示しています。アロニアベリーエキスは用量依存的に両方の大腸がん細胞株の細胞生存率を抑制しました。 (B)アロニアベリーエキスで24時間処理した後の遊走アッセイ。IC50濃度のアロニアベリーエキス処理は、両方の大腸がん細胞株の細胞遊走を阻害しました。 (C)アロニアベリーエキス処理後のコロニー形成アッセイ。 IC25およびIC50濃度を使用したアロニアベリーエキス処理は、用量依存的に両方の大腸がん細胞株のクローン形成を著しく阻害しました。 (D)アロニアベリーエキスで48時間処理した後の大腸がん細胞を用いた浸潤アッセイ。IC25およびIC50用量を使用したアロニアベリーエキス処理は、両方の大腸がん細胞株の浸潤能力を阻害しました。さらに、アロニアベリーエキスの抗浸潤効果はHCT116細胞において用量依存的でした。 エラーバーは平均±SDです。(*; 対照群と比較してP値 < 0.05、**; 対照群と比較してP値 < 0.01、***; 対照群と比較してP値 < 0.001、##; ABE-IC25と比較してP値 < 0.01、###; ABE-IC25と比較してP値 < 0.001)。 ABE:アロニアベリーエキス:CRC、結腸直腸がん。 |
| 次に、両大腸がん細胞におけるアロニアベリーエキスの抗遊走作用を評価するために遊走アッセイを行った。大腸がん細胞の移動率は、対照群と比較してIC50濃度のアロニアベリーエキス処理により有意に抑制され、SW480細胞では57%から7%(p < 0.01)、HCT116細胞株では61%から11%(p < 0.05、図1B)であった。コロニー形成アッセイも実施し、その結果、アロニアベリーエキスは用量依存的に大腸がん細胞のクローン形成を有意に阻害することが明らかになった(IC25 vs. IC50でp < 0.01)。コロニー面積が30%であった対照群と比較して、SW480細胞では、IC25濃度でアロニアベリーエキスは全体のコロニー面積を20%(p < 0.01)、IC50濃度でわずか5%(p < 0.001)まで減少させた。同様に、HCT116細胞株において、アロニアベリーエキスはIC25濃度でコロニー総面積を22%から14%に減少させ(p < 0.001)、IC50濃度で8%に減少させた(p < 0.001、図1C)。最後に、アロニアベリーエキスの抗浸潤効果を細胞浸潤アッセイで検証した。IC25およびIC50濃度における相対浸潤率は、SW480細胞株では42%および28%(p < 0.05 – 0.01)、HCT116細胞株では37%および14%(p < 0.001)であり、これらの大腸がん細胞株においても用量依存的な変化が認められた(IC25 vs. IC50でp < 0.001、図1D)。これらのデータは、多様なゲノム背景を持つ大腸がん細胞株において、アロニアベリーエキスが抗がん剤として高い可能性を有することを示唆している。 |
| 3.2.アロニアベリーエキス誘導による大腸がん細胞における活性酸素種(ROS)蓄積とアポトーシスの促進 |
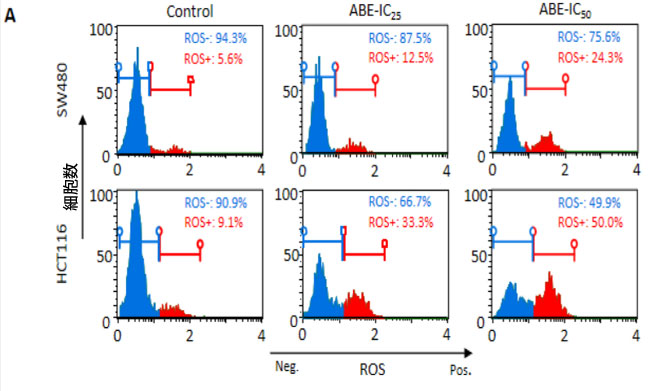
| 大腸がん細胞におけるアロニアベリーエキスの抗がん効果の根底にあるメカニズムをさらに理解するため、酸化ストレスキットを用いて活性酸素種(ROS)蓄積への影響を検討した。結果はMuse Cell Analyzerで解析した。SW480細胞において、IC50濃度のアロニアベリーエキス処理は、大腸がん細胞における活性酸素種蓄積を対照群の6%と比較して21%に有意に増加させた(p < 0.05)。同様に、HCT116細胞において、IC25およびIC50濃度の両方で、大腸がん細胞における活性酸素種蓄積を対照群の11%と比較して36%に有意に増加させた(p < 0.05;図2A) |
 |
 |
 |
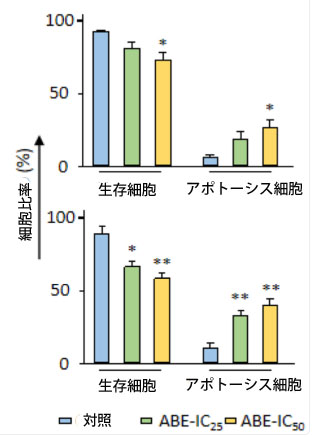 |
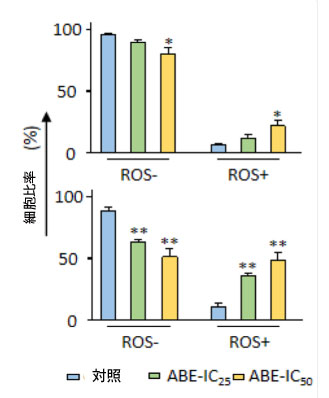
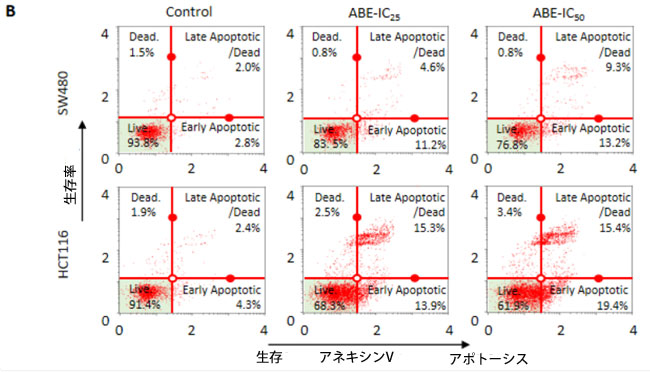
図2:アロニアベリーエキスは大腸がん細胞で活性酸素種の蓄積を誘発し、アポトーシスを促進します。 (A)アロニアベリーエキスで24時間処理した後のSW480細胞とHCT116細胞における活性酸素種分布の代表的なヒストグラム。値は棒グラフでROS-(陰性)細胞とROS+(陽性)細胞の割合として表されます。IC50レベルのアロニアベリーエキス濃度はSW480細胞で活性酸素種蓄積を誘発し、IC25濃度以上の高用量はHCT116細胞で活性酸素蓄積を誘発しました。 (B)アロニアベリーエキスで24時間処理した後のSW480細胞株とHCT116細胞株でのアネキシンV結合アッセイでアポトーシスを起こしている細胞の代表的なヒストグラム。値は棒グラフで生存細胞とアポトーシス細胞の割合(初期アポトーシス細胞と後期アポトーシス細胞の合計)として表されます。 アロニアベリーエキスは、SW480細胞においてIC50濃度で、HCT116細胞においてIC25濃度でアポトーシスを増強した。(*;対照群と比較してP値<0.05、**;対照群と比較してP値<0.01)。 ABE:アロニアベリー抽出物、CRC:大腸がん、ROS:活性酸素種。 |
| 次に、大腸がん細胞株におけるアロニアベリーエキスのアポトーシス誘導率に対する影響を評価するため、アネキシンV結合アッセイを実施した。アロニアベリーエキスはSW480およびHCT116の両方で有意にアポトーシスを誘導した。SW480では、アポトーシス誘導率はIC50濃度で22%に有意に増加したのに対し、対照群では7%であった(p < 0.05)。同様に、HCT116細胞では、アポトーシス誘導率はIC25用量で32%(p < 0.01)、IC50濃度で39%(p < 0.01)に有意に増加したのに対し、対照群では10%であった(図2B)。これらのデータを総合すると、アロニアベリーエキスの抗がん効果は大腸がん細胞における活性酸素種蓄積と細胞アポトーシスの増加に関連していることが示された。 |
| 3.3.トランスクリプトーム解析により、大腸がん細胞におけるアロニアベリーエキス処理後のp53シグナル伝達経路の関連性が明らかになった |
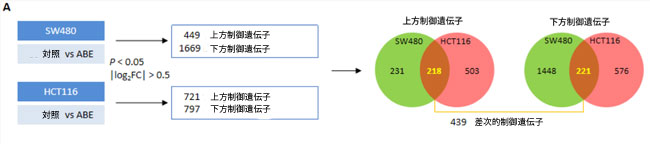
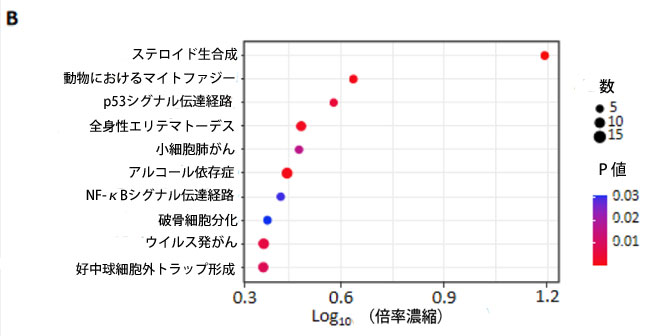
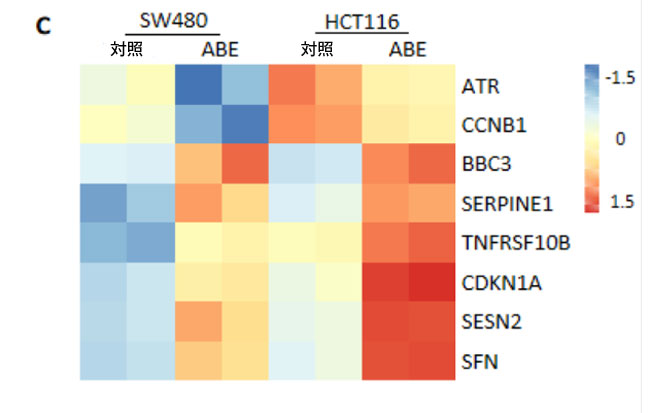
| 大腸がん細胞におけるアロニアベリーエキスの抗がん効果に関連する分子経路を同定するために、アロニアベリーエキス処理および未処理のSW480細胞株およびHCT116細胞株において、RNAシーケンシングを用いた包括的なゲノムワイドトランスクリプトーム解析を実施した。アロニアベリーエキス処理群と対照群を比較することにより、各細胞株において|log2FC| > 0.5およびP < 0.05に基づいて、アップレギュレーションおよびダウンレギュレーションされた遺伝子を抽出した。両細胞株において共通して異なる制御を受ける439個の遺伝子が検出され、これらは共通してアップレギュレーションおよびダウンレギュレーションされた遺伝子の集合体として定義した(図3A)。これらの差次的調節遺伝子のGOおよびKEGGエンリッチメントパスウェイ解析を実施したところ、上位10のエンリッチメントされたKEGGパスウェイの中で、p53シグナル伝達経路が最も顕著であり(図3B)、8つの共通の差次的調節遺伝子(図3C)が明らかになった。さらに重要なのは、p53シグナル伝達経路が大腸がんを含むさまざまな悪性腫瘍の進行に重要な役割を果たしていることを考えると、これは特に興味深いことだった(Hernandez BorreroおよびEl-Deiry、2021)。その後のp53経路関連遺伝子のqRT-PCRアッセイでは、ATR、CCNB1、SESN2、SFNを含むこれらの差次的調節遺伝子のほぼ半数が、ゲノムワイドトランスクリプトーム解析の結果と統計的有意性をもって一致していることが確認された(p < 0.05 – 0.001、図3D)。総合的に、p53 シグナル伝達経路は、大腸がん細胞における アロニアベリーエキスの抗がん効果のメカニズムに関連する候補経路として特定されました。 |
 |
 |
 |
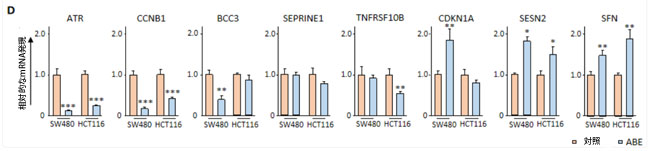 |
図3:P53シグナル伝達経路は大腸がん細胞におけるアロニアベリーエキスの抗発がん効果と相関している。 (A)アロニアベリーエキス処理群および対照群の大腸がん細胞のゲノムワイドトランスクリプトーム解析に従って、差次的調節を受ける遺伝子を選択する手順を示す図。SW480細胞またはHCT116細胞でアロニアベリーエキス処理と対照との間でLog2 FC > ±0.5およびP < 0.05の差があった場合、その遺伝子はアップレギュレーションまたはダウンレギュレーションを受けていると定義した。両方の細胞株でアップレギュレーションまたはダウンレギュレーションを受けた439個の遺伝子は、2つの細胞株間で共通の差次的調節を受ける遺伝子と定義した。 (B)アロニアベリーエキス処理した大腸がん細胞における共通の差次的調節を受ける遺伝子のKEGGパスウェイエンリッチメント解析の散布図。パスウェイは、遺伝子数> 5で倍数エンリッチメント> 2.0およびP < 0.05でエンリッチメントを受けているとみなした。上位10のエンリッチメントを受けたパスウェイが図にプロットされている。 (C) p53シグナル伝達経路において共通して差次的に制御される遺伝子の発現を示すヒートマップ。 (D) SW480細胞およびHCT116細胞におけるp53シグナル伝達経路において共通して差次的に制御される遺伝子のqRT-PCR解析。β-アクチンmRNA発現を内部対照として用いた。平均値(列)±SDが示されている(*;P値<0.05、**;P値<0.01、***;P値<0.001、対照群 vs. ABE)。 ABE:アロニアベリー抽出物、CRC:大腸がん、KEGG:京都遺伝子ゲノム百科事典。 |
| 3.4.アロニアベリーエキスは大腸がん細胞におけるChk1のリン酸化を阻害した |
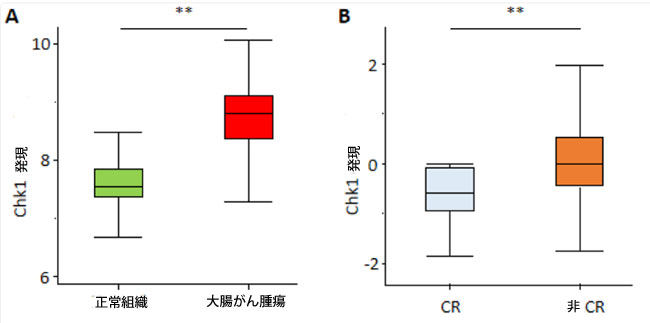
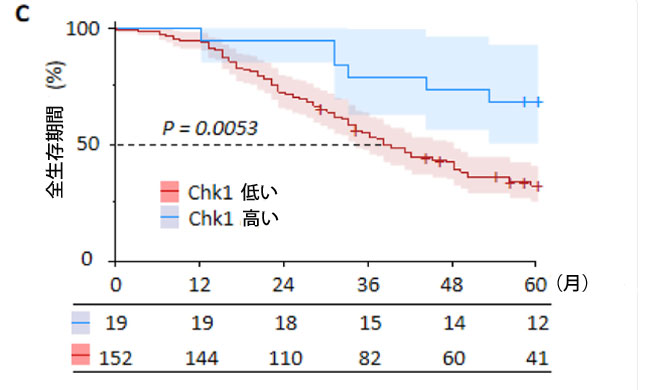
| チェックポイントキナーゼ1(Chk1)は、がんにおいてp53を調節する重要な制御因子であり、p53依存的に抗がん効果を発揮する(Rizzotto et al., 2021; Shieh et al., 2000)。一方、Chk1はp53非依存的にがん細胞の生存を阻害することも報告されており、がん治療への潜在的な道筋を示している(McNeely et al., 2014)。まず、3つの公開データセットにおける大腸がん症例の遺伝子発現プロファイリングデータを解析することにより、Chk1 mRNAの特性を調査した。 TCGA公開データセット(症例数:腫瘍/正常=286/41)の大腸がん症例を解析したところ、Chk1の発現は正常組織と比較して大腸がん腫瘍で有意に高いことがわかった(Chk1発現:8.7 vs. 7.6、p < 0.01;図4A)。別の公開データセット(GSE104645)には、全身化学療法による完全奏効(CR)達成に関する情報を含む大腸がん症例181例が含まれていた(症例数:CR/非CR=8/173)。このデータセットの解析により、CR症例では非CR症例と比較してChk1の発現が有意に低いことが明らかになった(Chk1発現:−0.6 vs. 0.1、p = 0.01;図4B)。さらに、ステージIV大腸がん症例(症例数:Chk1発現高/低 = 152/19)の生存情報を含むGSE159216データセットの解析では、Chk1発現高症例はChk1発現低症例と比較して全生存率(OS)が有意に不良であることが明らかになった(p < 0.01、図4C)。 |
 |
 |
 |
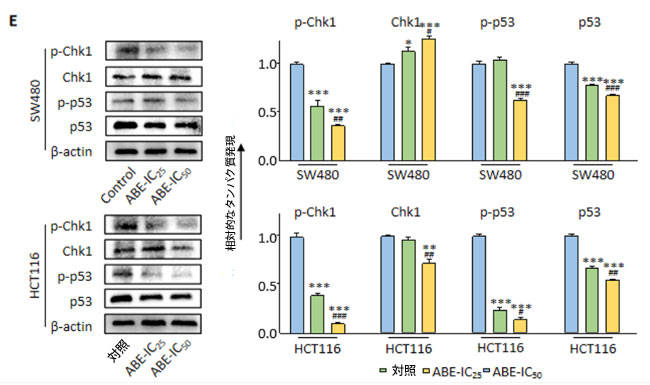 |
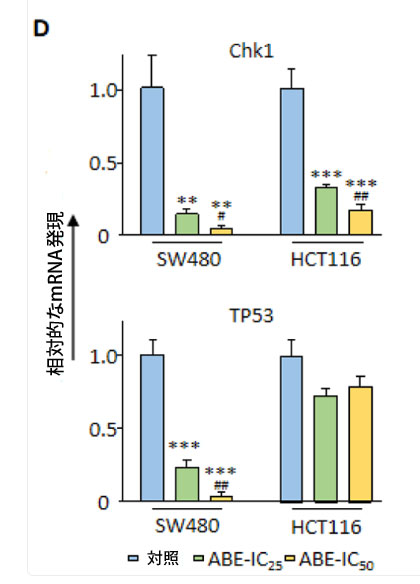
図4:アロニアベリーエキスは大腸がん細胞中のChk1発現を阻害し、大腸がんの全身療法の潜在的ターゲットとなる。 (A)TCGAデータセットの大腸がん症例におけるChk1の発現。Chk1の発現は、正常組織と比較して腫瘍で上方制御されていた。 (B)GSE104645の大腸がん症例におけるChk1の発現。大腸がんの全身療法後、CR(完全奏効)症例と比較して、非CR(非完全奏効)症例のChk1発現が高かった。 (C)GSE GSE159216の大腸がん症例におけるChk1の発現。高いChk1発現を示すステージIVの大腸がんは、不良な生存転帰と関連していた。 (D)異なる濃度のアロニアベリーエキスで24時間処理した後のSW480細胞とHCT116細胞におけるChk1とTP53のqRT-PCR分析。β-アクチンmRNA発現を内部対照として使用し、遺伝子の相対的発現を計算した。 (E) SW480細胞およびHCT116細胞を異なる濃度のアロニアベリーエキスで24時間処理した後、p53シグナル伝達経路関連タンパク質(ATR、p-ATR、ATM、p-ATM、p53、p-p53)およびβ-アクチンのウェスタンブロット法で測定した。β-アクチンタンパク質は内部標準として用いた。平均値(列)±SDを示す(*;対照群に対するP値<0.05、**;対照群に対するP値<0.01、***;対照群に対するP値<0.001、#;ABE-IC25に対するP値<0.05、##;ABE-IC25に対するP値<0.01、###;ABE-IC25に対するP値<0.001)。 ABE:アロニアベリー抽出物、CRC:大腸がん、Chk1:チェックポイントキナーゼ1、CR:完全奏効。 |
| 大腸がん患者におけるChk1の影響を評価した後、Chk1およびTP53遺伝子のqRT-PCRアッセイを実施し、これらの遺伝子がアロニアベリーエキスの抗がん効果を調整する潜在的な要因としての役割を同定しました。実際、SW480(対照 vs. ABE IC25 vs. ABE IC50、1.00 vs. 0.14 vs. 0.04; p < 0.05 – 0.01)およびHCT116(対照 vs. ABE IC25 vs. ABE IC50、1.00 vs. 0.32 vs. 0.16; p < 0.01 – 0.001)の両方において、アロニアベリーエキスが用量依存的にChk1の発現を有意に低下させることが観察されました(図4D)。同様に、HCT116細胞では有意な変化は観察されなかったが、アロニアアベリーエキス処理後のSW480ではTP53遺伝子の発現も低下した(対照 vs. ABE IC25 vs. ABE IC50、1.00 vs. 0.23 vs. 0.03、p < 0.01 – 0.001、図4D)。 |
| Chk1およびp53のリン酸化型、リン酸化Chk1(p-Chk1)およびリン酸化p53(p-p53)も、Chk1およびp53タンパク質発現解析に含めました。β-アクチンで標準化した後、p-Chk1はSW480(相対p-Chk1発現:対照 vs. ABE IC25 vs. ABE IC50、1.00 vs. 0.57 vs. 0.36; p < 0.001 – 0.01)およびHCT116(対照 vs. ABE IC25 vs. ABE IC50、1.00 vs. 0.39 vs. 0.10; p < 0.001)の両方において、用量依存的にアロニアベリーエキスによって有意にダウンレギュレーションされることが明らかになりました(図4E)。 HCT116細胞では、アロニアベリーエキス処理後、p-p53の発現も用量依存的にダウンレギュレーションされた(対照群 vs. ABE IC25 vs. ABE IC50、それぞれ1.00 vs. 0.23 vs. 0.13、p < 0.001)。IC50濃度のアロニアベリーエキスは、SW480細胞においてp-p53の発現を有意にダウンレギュレーションした(対照群 vs. ABE IC50、それぞれ1.00 vs. 0.62、p < 0.01 – 0.001、図4E)。これらを総合すると、アロニアベリーエキスは大腸がん細胞において、大腸がんの全身療法の有力な候補遺伝子であるChk1の発現をダウンレギュレーションした。さらに、アロニアベリーエキスはp-Chk1およびp-p53の発現をダウンレギュレーションしており、このことがこの悪性腫瘍におけるアロニアベリーエキスの抗がんメカニズムを部分的に説明している。 |
| 3.5.アロニアベリーエキスは大腸がん細胞において細胞周期停止を引き起こし、DNA損傷を増強した |
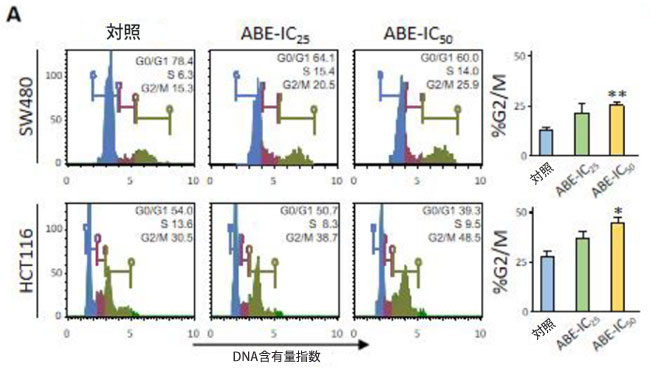
| Chk1とp53がアロニアベリーエキスの抗がん効果の潜在的メディエーターとしての役割を担っていることを踏まえ、次に細胞周期アッセイを実施し、アロニアベリーエキスが細胞周期ダイナミクスに及ぼす影響を検討した。興味深いことに、IC50濃度のアロニアベリーエキスをSW480細胞(p < 0.01)とHCT116細胞(p < 0.05)の両方で処理した後、G2/M期で停止した細胞の割合が増加することが観察され、その抗がん効果のメカニズムの一つが大腸がん細胞における細胞周期停止の誘導によるものであることが示唆された(図5A)。 |
 |
 |
 |
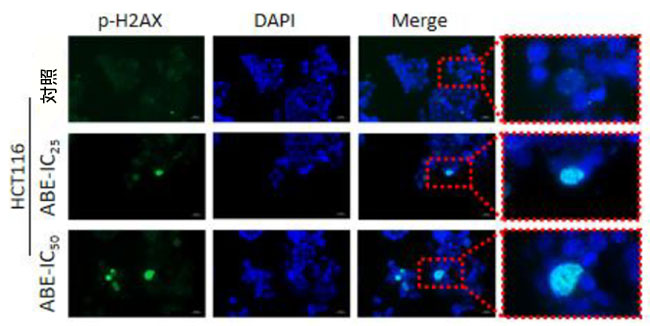 |
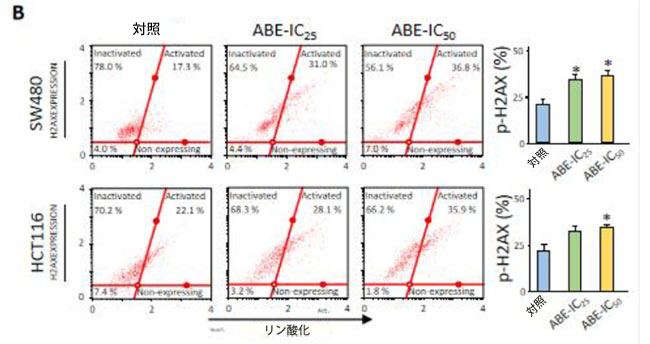
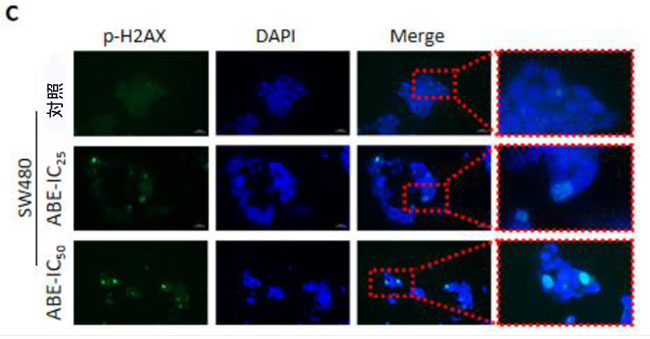
図5:大腸がん細胞におけるG2/M期でのアロニアベリーエキスによる細胞周期停止とDNA損傷の増強。 (A)アロニアベリーエキス処理後の両細胞株におけるG2/M期(訳者注:G2/M期(G2/M phase)とは、細胞が分裂する直前の「最終準備段階」から「分裂実行」までの期間を指します)での細胞周期停止を示す代表的なヒストグラム。 (B)異なる濃度のアロニアベリーエキスで48時間処理した後のSW480細胞とHCT116細胞におけるDNA損傷を表すp-H2AXの代表的なヒストグラム。値はp-H2AX発現細胞の割合として表される。 (C)アロニアベリーエキス処理後の両大腸がん細胞における核内での発現が増強されたp-H2AXの免疫蛍光アッセイの代表的な画像。平均(列)± SDが示されている(*; P値<0.05 vs.コントロール、**; P値<0.01 vs.コントロール)。 ABE:アロニアベリー抽出物、H2AX:H2AヒストンファミリーメンバーX、p-:リン酸化-。 |
| 次に、大腸がん細胞におけるDNA損傷を解析するため、リン酸化H2AヒストンファミリーメンバーX(p-H2AX)の発現を解析しました(Fujii, 2019; Hopp et al., 2017; Takahashi et al., 2011)。まず、Muse Cell Analyzerを用いたフローサイトメトリーアッセイによりp-H2AXの発現を解析しました。SW480では、IC25およびIC50の両用量でアロニアベリーエキス処理後にp-H2AXの発現が有意に増加しました(p-H2AX(%):対照 vs. ABE IC25 vs. ABE IC50、20 vs. 34 vs. 36、p < 0.05)。同様に、IC50 濃度の アロニアベリーエキスは、HCT116 細胞で p-H2AX の発現を有意に促進しました (p-H2AX (%): コントロール vs. ABE IC50、22 vs. 34、p < 0.05、図 5B)。これら 2 つの p-H2HX 分析の結果は、大腸がん細胞の DNA 損傷が アロニアベリーエキスによる処理によって促進されたことを示唆しています。同時に、DNA 損傷に反応して核細胞で上方制御された p-H2AX を視覚化するために、免疫蛍光分析を実施しました (Bhardwaj et al., 2012; Mah et al., 2010)。p-H2AX の免疫蛍光分析により、未処理コントロール群では p-H2AX の発現が弱く、アロニアベリーエキス処理後の核 大腸がん細胞では p-H2AX の発現が促進されたことが明らかになりました (図 5C)。総合的に、我々のデータは、アロニアベリーエキスが細胞周期停止を誘導し、大腸がん細胞の DNA 損傷を促進することを示しています。 |
| 3.6.アロニアベリーエキスによる治療は、大腸がん患者由来3Dオルガノイド(PDO)モデルにおいて抗がん活性を示した |
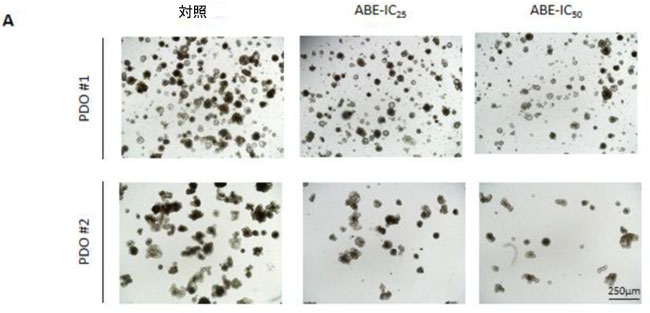
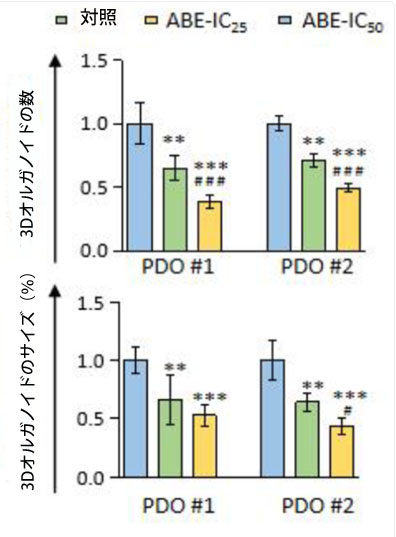
| アロニアベリーエキスの抗がん効果は、我々の細胞培養に基づく知見を検証するために、以前に大腸がん症例から作製された3Dオルガノイド(PDO)モデルにおいても評価された(Okuno et al., 2022)。PDO #1では、IC25およびIC50の用量でアロニアベリーエキスを治療することにより、PDOの形成が有意に阻害された(PDO数:対照 vs. ABE IC25 vs. ABE IC50、それぞれ107 vs. 70 vs. 41; p < 0.01 – 0.001; 図6A)。 PDO #2では、IC50濃度のABE処理によりPDO形成が有意に阻害されました(PDO数:コントロール vs. ABE IC25 vs. ABE IC50、43 vs. 31 vs. 21、p < 0.01 – 0.001、図6A)。同様に、PDO #1および#2では、IC25およびIC50の用量でABE処理することにより、3Dオルガノイド(PDO)モデルの増殖が有意に阻害されました(PDO#1の%サイズ:コントロール vs. ABE IC25 vs. ABE IC50、1.0 vs. 0.66 vs. 0.53、p < 0.01 – 0.001、PDO#2の%サイズ:コントロール vs. ABE IC25 vs. ABE IC50、1.0 vs. 0.66 vs. 0.44、p < 0.01 – 0.001、図6A)。全体的に、アロニアベリーエキス は 3Dオルガノイド(PDO)モデルで抗がん活性を発揮し、3D 培養実験で細胞培養に基づく発見をうまく検証しました。 |
 |
 |
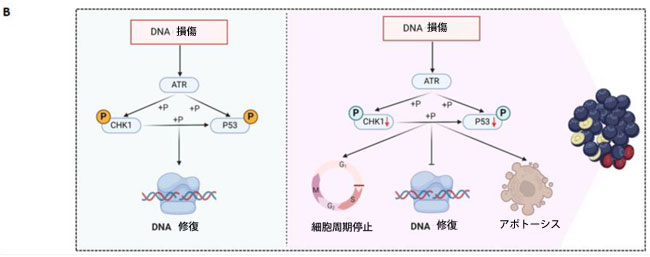 |
図6:アロニアベリーエキスは大腸がん患者由来3Dオルガノイド(PDO)モデルにおいて抗がん活性を効果的に増強し、大腸がん細胞に対するアロニアベリーエキスの効果を示す概略図。 (A)異なる濃度のアロニアベリーエキスで48時間処理した後の3Dオルガノイド(PDO)モデルの代表画像。3Dオルガノイド(PDO)モデル数とサイズの平均(列)± SDが示されている(*;対照に対してP値<0.05、**;対照に対してP値<0.01、***;対照に対してP値<0.001)。 (B)大腸がんにおけるChk1およびp53によるDNA損傷の制御を介したアロニアベリーエキスの抗がん効果の模式図。 ABE、アロニアベリー抽出物、Chk1、チェックポイントキナーゼ1、PDO、患者由来3Dオルガノイド。 |
| 4.考察 |
| 近年の抗がん剤の開発により、大腸がん患者の生存率は大幅に改善しました(Van Cutsem et al., 2016)。しかしながら、多くの患者は従来の治療レジメンに対して化学療法抵抗性を呈し、過度の毒性を経験することが多く、治療成績と生活の質を向上させるための抗がん剤のさらなる開発の必要性が浮き彫りになっています。天然食物由来化合物は、費用対効果、毒性の低減、そして複数の経路を標的とすることができることから、様々ながんに対する有望な補完療法・代替療法としてますます注目を集めています(Goel and Aggarwal, 2010; Goel et al., 2008a; Goel et al., 2008b; Pan et al., 2015; Wang et al., 2011; Wang et al., 2013)。この点において、我々はポリフェノールを豊富に含み、強力な抗がん作用を持つアロニアベリーエキスに注目しました。本研究では、多様なゲノム背景を持つ大腸がん細胞株を用いて、包括的かつ体系的な一連の研究を実施しました。その後、これらの知見を3Dオルガノイドで検証し、アロニアベリーエキスの抗がん効果とメカニズムを評価しました。 |
| アロニアベリーエキスの細胞生存率に対する抗がん作用は、膵臓がん(Thani et al., 2014)、肝細胞がん(Gao et al., 2018)、白血病(Sharif et al., 2012)、子宮頸がん(Rugina et al., 2012)、大腸がん(Bermudez-Soto et al., 2007; Malik et al., 2003; Zhao et al., 2004)における最近のいくつかの研究で報告されています。しかし、これらの研究のほとんどは主に探索的なものであり、アロニアベリーエキスの抗がん作用の具体的なメカニズムを深く掘り下げてはいません。本研究では、アロニアベリーエキスが大腸がん細胞株において細胞生存率、遊走性、クローン形成性、および浸潤を阻害することを実証しました。さらに重要なことに、以前の研究では、がん細胞における過剰な 活性酸素種蓄積がアポトーシスを含む細胞死につながる可能性があることが示唆されています (Wang et al., 2021)。本研究では、大腸がん細胞における 活性酸素種蓄積を促進しアポトーシスを誘導するアロニアベリーエキスの有効性を実証しましたが、これは以前の報告 (Rugina et al., 2012; Wei et al., 2020) でなされたいくつかの示唆と一致しています。抗酸化物質の活性酸素種蓄積とがん細胞死に対する逆説的な効果は、以前の研究で頻繁に報告されています (Kalyanaraman et al., 2018; Xu et al., 2023)。この効果は、本研究で アロニアベリーエキスによって誘導された活性酸素種の蓄積とそれに続く細胞死を部分的に説明しています。本研究で初めて大腸がん細胞を対象に実施したゲノムワイドなトランスクリプトーム解析により、p53 シグナル伝達経路など、アロニアベリーエキス の抗がん活性に関連する主要な成長シグナル伝達経路を特定することができました。これまでの報告では、p53 シグナル伝達経路に関連する特定の遺伝子に対するアロニアベリーエキスの効果に焦点が当てられていませんでしたが、私たちは qRT-PCR アッセイを使用して、p53 シグナル伝達カスケード内の主要な差別的制御遺伝子を検証しました (図 6B)。 |
| p53シグナル伝達経路がKEGGで上位10のエンリッチド経路の1つであることを確認した後、p53の重要な制御因子としてのChk1の役割(Hu et al., 2021)と、抗がん療法の標的候補としてのChk1の可能性(da Costa et al., 2023)を検討しました。Chk1は、S期内およびG2/M期の細胞周期停止を引き起こすSer/Thrタンパク質キナーゼであり(Neizer-Ashun and Bhattacharya, 2021)、DNA損傷に応答してリン酸化を介して活性化されます(Han et al., 2016)。Chk1は、p53活性の制御と、細胞周期の重要な制御因子であるサイクリン依存性キナーゼ(CDK)のリン酸化阻害を介して、細胞周期のダイナミクスを制御することができます(McNeely et al., 2014)。 TCGAデータセットの解析から、大腸がんを含む様々な悪性腫瘍においてChk1の過剰発現が報告されていることが明らかになりました(Madoz-Gurpide et al., 2007)。さらに、公開データセットGSE104645およびGSE159216におけるChk1の追加評価により、Chk1が大腸がんおよびいくつかの悪性腫瘍において腫瘍の増殖を促進することが確認され、Chk1と抗がん剤耐性(Bartucci et al., 2012; Cavelier et al., 2009; Lee et al., 2011; Perego et al., 2003)および腫瘍の進行との関連性が明らかになりました。本研究では、変異p53を持つSW480と野生型p53を持つHCT116の両方の大腸がん細胞株において、アロニアベリーエキスによってp-Chk1がp-p53とともにダウンレギュレーションされ、G2/M期での細胞周期停止とp-H2AX発現で評価したDNA損傷の増強をもたらしたことが示唆された。 |
| 本研究にはいくつかの強みがあります。第一に、大腸がん細胞におけるアロニアベリーエキスの抗がん効果を解析し、その抗がん効果に関与する特定の遺伝子と経路を同定するために、ゲノムワイドなトランスクリプトーム解析を実施しました。これらの取り組みの結果、様々な経路、特にp53シグナル伝達経路の顕著な増加が観察されました。p53シグナル伝達経路の主要な制御因子をさらに解析した結果、Chk1とp53の両方がアロニアベリーエキスによってダウンレギュレーションされ、DNA損傷を増強することが明らかになりました。第二に、抗がん効果を確認するために、2つの異なる治療濃度(IC25とIC50)を使用しました。第三に、アロニアベリーエキスの抗がん効果は3Dオルガノイドモデルにおいて検証されました。 |
| 本研究にはいくつかの限界があることを承知しております。第一に、アロニアベリーエキスの効果は動物モデルで評価されていません。第二に、正常細胞におけるアロニアベリーエキスの潜在的毒性を直接評価したわけではありません。しかしながら、これまでの研究では、アロニアベリーエキスを低濃度で使用した場合、非腫瘍形成性結腸細胞に有害な影響はないと報告されており(Zhao et al., 2004)、小動物モデル(Gajić et al., 2020)や臨床患者(Kędzierska et al., 2013)におけるアロニアベリーエキスの影響を評価した後でも、重篤な有害作用は報告されていません。さらに、本研究では陽性対照薬を含めなかったため、アロニアベリーエキスと臨床で使用されている薬剤との比較が可能であった可能性があります。さらに、ポリフェノールは既存の全身療法との併用により抗腫瘍効果が向上することが示されているにもかかわらず(Kaviani et al., 2023)、本研究ではアロニアベリーエキスを単独療法としてのみ評価しました。今後の研究では、現在の治療法との適合性や潜在的な相乗効果を判断する必要があります。 |
| 結論として、これらの知見は、大腸がんにおいてアロニアベリーエキスを安全かつ費用対効果が高く、多標的を標的とした補完・統合的治療法として用いるための更なるエビデンスを提供するものである。既存の全身療法との併用を含め、大腸がんの予防と治療におけるアロニアベリーエキスの可能性については、さらなる研究が必要である。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、Phytomedicine. 2024 Sep 19;135:156086. に掲載されたThe anticancer effects of Aronia berry extract are mediated by Chk1 and p53 in colorectal cancer.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


