ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
プロバイオティクスとポストバイオティクスを活用した 乳がん介入のための腸内細菌叢を中心としたアプローチ |
A S Arya, A Mythili |
|
|
| 要約 |
がんは世界中で主要な死因の一つであり、中でも乳がんは最も多く診断されるがんであり、女性の死亡率に大きな影響を与えます。早期初潮から閉経遅延までエストロゲンなどのホルモンに曝露された女性は、乳がんのリスクが高まる可能性があります。腸内細菌叢と乳がんとの関連性は、新たな研究分野です。腸内細菌叢のディスバイオシス(腸内細菌叢の乱れ)につながるあらゆる要因は、乳がんの潜在的な原因となる可能性があります。同時に、プロバイオティクス、ポストバイオティクス、次世代プロバイオティクス(NGP)は、腸内細菌叢を調節し、免疫応答を増強する可能性から、がん治療における有望なサプリメントとして注目されています。したがって、これらのバイオ医薬品は、免疫療法や腫瘍微小環境の調節に関するより深い知見をもたらします。ディスバイオシスを予防し、健康な腸内細菌叢を維持する能力は、乳がんの治療に役立ちます。これらの薬剤は有望ではあるものの、その作用機序、安全性、そしてヒトにおける臨床効果を完全に理解するには、より包括的な研究が必要です。本レビューでは、腸内細菌叢ががんの進行と制御に及ぼす影響を検証することにより、乳がん治療の強化におけるバイオ医薬品の重要な役割を明らかにし、この分野における継続的な研究の必要性を強調しています。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.マイクロバイオータ |
| 3.腸内細菌叢 |
| 4.乳腺微生物叢 |
| 5.乳汁微生物叢 |
| 6.プロバイオティクスとポストバイオティクスの作用機序 |
| 7.マイクロバイオームに基づく治療法 |
| 8.プロバイオティクスのがんにおける役割 |
| 9.腸内細菌叢と乳がん:プロバイオティクス介入 |
| 10.宿主の免疫調節に関与するプロバイオティクスとポストバイオティクス分子 |
| 11.現在の臨床的エビデンスと課題 |
| 12.プロバイオティクスとポストバイオティクスの将来展望と結論 |
本文 |
| 1.はじめに |
| 世界がん観測所(GLOBOCAN)は、2020年までにインドで130万人の新規がん症例と約85万人のがん関連死亡が報告されたと報告しています。乳がんは新規がん症例の13.5%、死亡率の10.6%を占めています[1]。報告によると、現在の傾向が続けば、2040年までに年間死亡者数は100万人に達する可能性があります[2]。先進国と発展途上国の両方で乳がん罹患率が上昇していることは懸念すべき事態であり、既存の限界を克服するための、より効果的な新しい抗がん治療の緊急の必要性が浮き彫りになっています。乳がんは多様な疾患であり、様々なサブタイプが存在します[3, 4]。乳がんは他のがんと同様に、複数の因子の影響を受ける多因子疾患です。これらの因子には、年齢、性別、月経開始(初潮)の早さ、閉経の遅さ、乳がんの既往歴または家族歴などの遺伝的および環境的要素が含まれます[3, 5]。微生物叢はがんの進行と制御に影響を与える主要な要因であるため、多くの研究者が微生物叢と人間の健康との複雑な関係の関連性を強調しています。腸内細菌叢の乱れはさまざまな疾患につながる可能性があるため、腸内細菌叢を適切にバランスさせることが不可欠です。腸内細菌叢とその関連代謝物は、乳がんを含むさまざまな種類のがんの抑制に強い影響を与える可能性があります[6]。これらの微生物の相対的な存在量はがんの種類によって異なり、治療結果の改善に役立ちます[3]。細菌の存在量は、がんにおける細菌の転写ランドスケープに焦点を当てたBICデータベースを使用して分析されました。この分析により、BRCA(乳がん浸潤性がん)およびOV(卵巣がん)に関連する細菌の多様性が他のがんの種類と比較して有意に高いことが明らかになり、同じものが図1に示されています。そのため、治療アプローチにおけるこの微生物叢の役割を調査する必要性が高まっています[7]。乳がんはホルモンとの関連性が強く、そのため内分泌療法が主な治療法となっています。しかし、医療現場では治療抵抗性が新たな懸念事項となっており、適切な対処が求められています[8]。治療に対する患者の無反応は、しばしばがんの再発や出現につながります。様々な治療法に対する患者ごとの反応を理解することは、より困難になっています[9]。腸内細菌叢の構成は個人差があり、これらの微生物が様々な治療法に影響を与える上で重要な役割を果たしていることは明らかです。そのため、プロバイオティクスやポストバイオティクスなどを用いてこれらの微生物を標的とすることは、効果的な治療介入のための有望な方法となる可能性があります[10]。 |
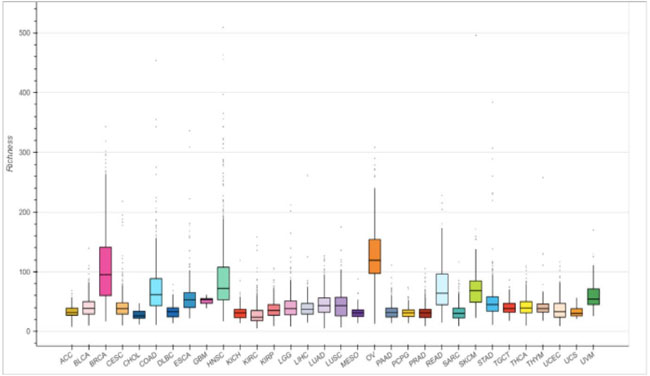 |
図1. がん検体で検出された細菌多様性の箱ひげ図。これは、がん種ごとの細菌多様性の豊富さを視覚的に分析したものである[7] |
| FAO / WHOはプロバイオティクスを、適切な量を投与すると宿主に健康上の利益をもたらす生きた微生物と定義しています[11]。世界のプロバイオティクス市場は2021年に581.7億米ドルと評価されました。受容と需要の増加により、2030年までに年平均成長率(CAGR)7.5%で成長すると予測されています[12]。プロバイオティクスは腸内の善玉菌の数を増やすのに効果的で、それによって個人の健康を全体的に高めます[13]。経口投与されると、プロバイオティクスは腸に到達し、そこで微生物バランスの維持や全体的な健康の増進などの有益な効果を発揮します[14]。それらは免疫調節、抗がん、抗糖尿病、抗肥満作用において重要な役割を果たし、さまざまな疾患の治療に役立ちます[15]。プロバイオティクスは、マイコトキシンの生体内変換、ビタミンK、リボフラビン、葉酸の合成、そして生体外物質やその他の環境汚染物質の解毒にも関与しています[16]。また、様々な代謝産物や短鎖脂肪酸などの関連化合物の生成にも関与しています。さらに、有益な微生物の増殖を促進し、感染性細菌の増殖を抑制することで、宿主の健康増進にも寄与します[13, 17]。いくつかの研究では、プロバイオティクスが乳糖耐性、過敏症反応、さらには腸の炎症の抑制にも応用できる可能性が示唆されています[18]。 |
| 近年の科学の進歩に伴い、ポストバイオティクスも広く受け入れられるようになりました。ポストバイオティクスには、加熱殺菌した微生物とその代謝成分が含まれることが多く、これらはヒトの健康に何らかの利益をもたらします[19–21]。国際プロバイオティクス・ポストバイオティクス科学協会(ISAPP)は、ポストバイオティクスを「宿主に健康上の利益をもたらす無生物微生物および/またはその成分の調製物」と定義しました。ポストバイオティクスという用語は、「生物に関連する」という意味の「biotic」と、「後」という意味の「post」という2つの言葉に由来しています。つまり、ポストバイオティクスという用語は「死後の世界」と解釈できるのです[21]。 |
| ポストバイオティクスは、ラクトバチルス、ビフィドバクテリウム、ストレプトコッカス、ユーバクテリウム、フェカリバクテリウム、サッカロミセスなどの特定の細菌または真菌種によって産生される天然由来の分子です[22]。ポストバイオティクスは、その元素組成に基づいて様々なクラスに分類されます。これらのグループには、脂質(プロピオン酸および酪酸)、有機酸(乳酸、酢酸、プロピオン酸、3-フェニル乳酸)、分泌タンパク質/ペプチド(ラクトセピン、p40分子)、炭水化物(テイコ酸、ガラクトースを豊富に含む多糖類)、バクテリオシン(アシドフィリン、ビフィジン、ロイテリン)、ビタミンおよび補酵素(ビタミンB群、リボフラビン、アスコルビン酸)、ペプチドグリカン由来のムロペプチドやリポテイコ酸などの複合分子が含まれます[23, 24]。ポストバイオティクスの潜在的な供給源は、プロバイオティクスの細胞外成分または細胞内成分のいずれかです。これらには、細胞外多糖類、テイコ酸、さらには線毛、線毛、鞭毛といった表面に突出する糸状構造が含まれる場合があります[23]。ポストバイオティクスは、生理学的、調節的、代謝的、行動的反応に影響を及ぼすことで、宿主微生物叢に大きな影響を与える可能性があります。その有益な作用としては、病原体の抑制、抗炎症作用、免疫調節作用などが挙げられます。さらに、抗菌作用および抗酸化作用を持つことでもよく知られています[24]。 |
| 2.マイクロバイオータ |
| マイクロバイオータとは、口腔、腸管、その他の関連部位など、特定の環境に関連する生きた微生物を指します[25]。かつては十分に研究されておらず、人体の暗黒物質と考えられていましたが、近年のマイクロバイオーム研究とマルチオミクスの進歩により、ヒトの健康におけるマイクロバイオータの計り知れない役割についての知見が深まりました。これらのマイクロバイオータは、臓器系全体とその環境への影響から「臓器」と呼ばれることが多く、また、膨大なゲノムデータ(人体全体のゲノム構成を上回る数)を有することから「人体の第二のゲノム」と呼ばれることもあります[26]。MetaHitとヒトマイクロバイオームプロジェクトのデータを組み合わせた研究により、ヒトに関連する微生物種は約2,172種存在することが明らかになっています。マイクロバイオータに関連してよく使われる用語として「マイクロバイオーム」があります。マイクロバイオームとは、環境中に生息するすべての生物のゲノムの集合体、ならびに生物的・非生物的構成要素を指す広義の用語である [27]。この微生物の平衡が崩れると、ディスバイオーシスと呼ばれる状態に至る可能性がある。現代生活においては、健康、環境要因、および抗生物質などの他の非生物的要因も細菌組成に影響を及ぼし、ディスバイオーシスの一因となる可能性がある [28]。プロバイオティクス、プレバイオティクス、およびプロバイオティクスとプレバイオティクスの組み合わせを使用することで、この状態を克服することもできる [29, 30]。マイクロバイオータを調節する様々な方法とそれらがヒトの健康に及ぼす関連する影響を図 2 に示している。これらの微生物に関連する特定の代謝物は、直接的または間接的に、さまざまなシグナル伝達経路の修正または調節に関与する可能性がある [31]。 |
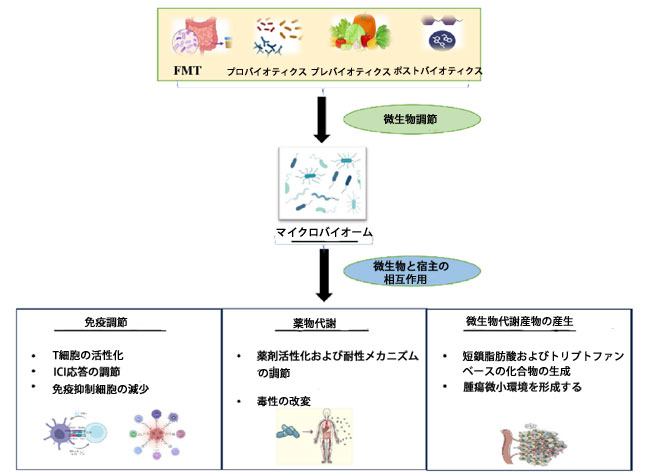 |
| 図2.微生物叢の調節とヒトの健康における関連性の図解 |
| 3.腸内細菌叢 |
| 腸内細菌叢とは、細菌、真菌、寄生虫、古細菌など、ヒトの腸内に生息する微生物群全体を指す広義の用語です。また、ある程度ウイルスも含まれる場合があります[32]。腸内マイクロバイオームは、腸内細菌叢の機能的および遺伝的プロファイルとして定義できます[33]。平均的な人の生涯において、約60トンの食物粒子と数百万の微生物がヒトの消化管を通過します[34]。また、いくつかの研究では、細菌数とヒト細胞数の比率が10:1であることが示されている[35]。 |
| 腸内細菌叢とヒト宿主の間には、共生関係、すなわち片利共生関係が存在します。これらの微生物の構成は地域によって異なり、大腸にはその集団の大部分が集中しています。これらの微生物のほとんどは嫌気性です[36]。腸内細菌叢は、腸管の完全性の維持、病原体からの防御、免疫バランスの調整など、宿主にさまざまな恩恵をもたらします[25, 34, 37, 38]。腸内細菌叢は、腸管バリアの正常な機能をサポートし、抗炎症作用も発揮します[33]。また、ビタミンや短鎖脂肪酸などの特定の物質の合成など、不可欠な機能も担っています。これらの機能に加えて、宿主の免疫システムを強化し、体内の微生物叢を維持します[39]。腸内細菌叢のコロニー形成は通常、妊娠中に始まり、生涯を通じて進化していきます。宿主因子(遺伝的要因)と外的因子(食事、習慣、衛生状態、薬物、喫煙/アルコール摂取)が腸内細菌叢の構成を主に左右します。確立された腸内細菌叢を免疫反応から守るため、消化管は物理的因子(上皮細胞と粘液)、生化学的因子(二次代謝物と酵素)、そして免疫学的因子からなる多因子性かつ動的な腸管バリアを形成しています[40]。 |
| 腸内微生物叢は、宿主の恒常性と健康維持に大きな役割を果たしています。これらの微生物は、短鎖脂肪酸(SCFA)、胆汁酸(BA)、分岐鎖アミノ酸(BCAA)、トリメチルアミンN-オキシド、トリプトファン、ビタミン、神経伝達物質、その他の抗菌ペプチドなど、様々な化合物の産生と代謝に関与しています[41]。腸内微生物叢の構成の変化が、がん、心血管疾患、炎症性腸疾患、精神神経疾患、2型糖尿病、肥満、さらには喘息など、様々な疾患に関与していることを示唆するエビデンスもあります[42]。特定のプロバイオティクスによる腸内微生物叢の調節は、様々な疾患の治療に有効であり、ラクトバチルス・ラムノサスのプロバイオティクス投与は、高脂血症のマウスモデルにおいて有効であることが示されています。プロバイオティクスは腸内細菌叢の構成を維持・変化させる上で不可欠な役割を果たしており、潜在的な治療の進歩が期待されています[43, 44]。 |
| 4.乳腺微生物叢 |
| 乳腺微生物叢とは、乳腺および母乳に生息する微生物を指します。この微生物叢は、プロテオバクテリア門とフィルミクテス門から構成されることが多いです[45]。乳房組織はかつて無菌であると考えられていましたが、その後の研究により、乳房組織にも腸管に類似した微生物群が多数生息していることが明らかになりました[46]。乳房組織における微生物叢の蓄積は、授乳、性交、腸管からの細菌の移行など、様々な経路によって確立されることが多いです[47]。乳房組織に関連する細菌群の中には、腸内細菌科や表皮ブドウ球菌などの病原性のものもあれば、ラクトコッカス・ラクチス、ラクトバチルス属、ストレプトコッカス・サーモフィルスなどのプロバイオティクス系のものもあります[48]。これらの病原菌およびプロバイオティクス菌は、免疫調節、予防、さらには腫瘍の進行など、さまざまな方法で宿主の健康に影響を与える可能性があります [49]。最近の研究によると、正常な乳房組織に生息する微生物は乳がんの発生率と関連していることが明らかになっていますが、微生物の組成は正常な乳房組織とがん組織の両方で異なります [49]。妊娠後期から授乳期にかけてのヒトの乳房組織の生理的で湿潤した解剖学的特徴は、微生物の定着、増殖などの機会を高めます。これらの条件は、微生物の生存に必要な栄養因子やその他の非生物的因子を満たすのに適しています。これらの要因に加えて、乳房組織の確立された管系は、ブドウ球菌などの微生物の微生物バイオフィルムの形成に有利です。正常な乳房組織の細菌組成は、乳がん組織のそれとは異なります [45]。健常組織では放線菌が豊富、プロテオバクテリアが減少することが多く、その逆もまた同様です[50]。研究では、腫瘍組織ではシュードモナス科や腸内細菌科などの科が優勢であることが結論付けられています。正常健常組織と乳がん組織の比較に加え、微生物群集の構成はがんのサブタイプによっても異なります[51]。したがって、これらの知見は乳がんに対するプロバイオティクス療法に効果的に活用できる可能性があります[52]。 |
| 5.乳汁微生物叢 |
| 母乳微生物叢と乳房組織微生物叢はしばしば関連しています。母乳微生物叢は新生児の常在菌の大部分を占めています[53]。母乳微生物叢(HMM)は、多様な微生物群と、幅広い栄養・生理活性分子で構成されています[54]。研究では、細菌、真菌、ウイルスなど、様々な微生物が母乳微生物叢に関与していることが示されています。母乳微生物叢を構成する重要な微生物群には、フィルミクテス属、ビフィドバクテリウム属、ラクトバチルス属、プロテオバクテリア属、放線菌属などがあります[54]。母乳微生物叢の構成は、授乳、母体のBMI(ボディマス指数)、年齢、食事、分娩中の抗生物質やプレバイオティクスの使用、分娩方法など、様々な要因の影響を受けることが多い[55]。培養法では、連鎖球菌、コリネバクテリウム、クチバクテリウムの様々な種を含む、母乳に関連する微生物の非常に多くの集団が存在することが実証されています[52]。 |
| 乳中の微生物叢の発生源として、主に2つの経路として、逆行性経路と腸乳管経路がある。逆行性経路では、乳児は乳汁を吸う際に乳管を通り、皮膚や唾液を介して乳児から母親へと微生物が移動する。これは、乳児の口腔由来のベイヨネラ、レプトトリキア、プレボテラなどの特定の細菌群や、膣由来のラクトバチルス(多くの場合、出産時に乳児が獲得)などの特定の細菌群が母乳中に存在することで証明されることが多い[55]。乳腺や母乳への細菌侵入のもう1つの経路は、腸乳管経路である。この経路では、母親の消化管から乳腺への免疫細胞を介した細菌の移行が起こり、そこで細菌が定着する[56]。 |
| 6.プロバイオティクスとポストバイオティクスの作用機序 |
| プロバイオティクスとポストバイオティクスは、受容体、栄養素、および空間を競合させることで病原体を排除し、感染リスクを低減するなど、いくつかのメカニズムを通じて免疫調節に重要な役割を果たすことが知られています[57]。また、pHを低下させ、バクテリオシンやバクテリオシン様産物を含む様々な代謝物を産生することで、腸管の完全性を維持します[18]。腸管コロニー形成と粘膜接着は、微生物叢の恒常性維持に役立つプロバイオティクスの潜在的な特性です[58]。腸絨毛および腸管上皮細胞に存在する特定のプロバイオティクスである乳酸菌群は、病原体の接着を阻害することで感染リスクを低減することが知られています[59, 60]。プロバイオティクスはまた、短鎖脂肪酸、有機酸、過酸化水素、リゾチーム、プロテアーゼ、バクテリオシンなどの化合物を産生することで、特定の抗菌活性を示します[61, 62]。プロバイオティクスは腸管杯細胞によるムチン産生を刺激し、腸管バリアを強化する[59]。例えば、ラクトバチルスによる乳酸産生はpHの低下と関連しており、またグラム陰性細菌に直接結合してその増殖を阻害する可能性がある[60]。 |
| このように、プロバイオティクスは腸内細菌叢とその代謝産物のバランスを維持し、恒常性を維持することが知られています。人体生態系に関連する常在微生物は、大腸菌やウェルシュ菌などの特定の腐敗菌の抑制にも大きく貢献している可能性があります。これらの腐敗菌は、アゾ還元酵素、ニトロ還元酵素、β-グルクロニダーゼなどの特定の分子を分泌します[63]。これらの分子は、がんの進行と増殖を促進することに関与しています。プロバイオティクスの潜在的な供給源である発酵乳製品を定期的に摂取することは、これらの腐敗菌の個体数を減少させる上で重要な役割を果たします[64]。 |
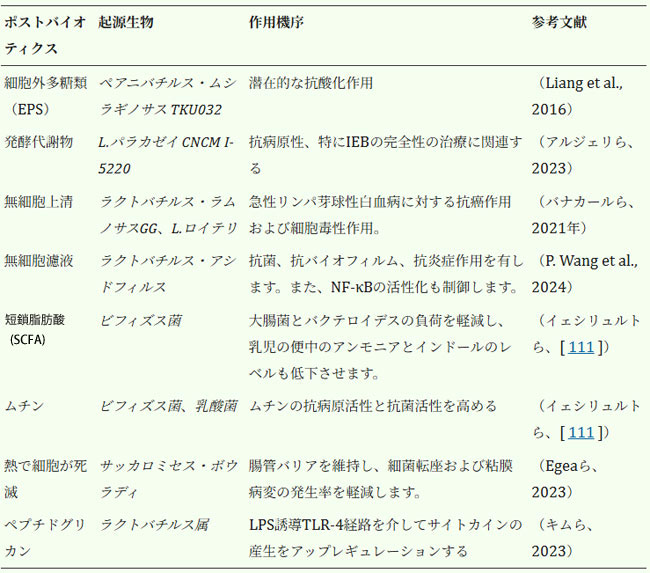
| プロバイオティクス菌の抗発がん活性は、潜在的発がん物質の結合と分解にも関連している可能性がある。多くの試験管内研究では、特定のプロバイオティクスがヘテロ環芳香族アミン(HAA)、ニトロソアミン、マイコトキシン、多環芳香族炭化水素(PAH)、フタル酸エステル(PAE)などの変異原性化合物の結合または代謝において重要な役割を果たすことが明らかになっている[65]。ポストバイオティクスはまた、プロバイオティクスの潜在的な健康効果やその他の治療効果を模倣することを目的としている。確立された分子構造と保存安定性により、ポストバイオティクスは様々な健康効果を持つことが証明されている。これらの特性は、標的組織に対する局所効果の持続期間を延長する。プロバイオティクスと比較して、これらの無生物分子は、生きた微生物の投与に関連するリスクを低減する[22]。最近の研究では、腸内細菌叢と乳房内細菌叢のディスバイオシスが乳がんの発症に潜在的に影響を及ぼすことが明らかになっている。これらの腸内細菌叢は、エストロゲンなどのさまざまなステロイドホルモンの代謝に関連しています。エストロゲンは乳がんのリスク増加に不可欠な役割を果たしており、したがって、乳がんの発生率を調節しています。ポストバイオティクスは宿主の免疫システムとネイティブマイクロバイオームの調節に大きな影響を与えるため、強力な抗がん特性を示します[66]。ポストバイオティクス、その原料生物、および免疫調節のメカニズムのリストを表1に示します。ポストバイオティクスは、隣接する細胞を殺すことなく標的部位にアポトーシスを誘導できるため、科学界から大きな関心を集めています。ポストバイオティクスは内因性経路と外因性経路の両方を介してアポトーシスを誘導することができ、これは多くの場合、Bad、Bax、カスパーゼ8、カスパーゼ9、カスパーゼ3などの発現を上昇させることによって達成されますが、Bcl-2の抑制にも関連しています[67]。 |
| 表1.ポストバイオティクスのリストとヒトの健康における作用機序 |
 |
| 7.マイクロバイオームに基づく治療法 |
| 抗生物質の使用は数世紀にわたって劇的に増加してきたため、抗生物質に対する耐性も出現しています。抗生物質に対するこの反応性は、現在、これらの化学療法の有効性に疑問を投げかけています。また、抗生物質は、腸内細菌叢の乱れ(ディスバイオシス)の出現の潜在的な原因でもあります。有益な細菌とそのコンソーシアムもまた、より良い治療的意義を求めて研究されています[68]。近年、ヒトの健康におけるマイクロバイオームに関する知識と科学的エビデンスの進歩は、微生物の腸内細菌叢の乱れ、ひいては様々な疾患に対処するための特異的な治療法の開発に徐々に近づいています[68]。現在のマイクロバイオームに基づく治療戦略には、糞便マイクロバイオーム移植(FMT)、プロバイオティクス、ポストバイオティクスが含まれることがよくあります。前述のように、正常組織と腫瘍組織では微生物組成が異なります。したがって、各治療法の有効性は、個人間のマイクロバイオームのばらつきや宿主とマイクロバイオームの相互作用など、様々な根本的要因によって変化する可能性があります[69]。図3は、マイクロバイオームに基づく治療法の概要と、正常な腸内細菌叢を回復させることでディスバイオシスの症例をコントロールする上でのそれらの効果を示しています。マイクロバイオームは、自然免疫系と獲得免疫系の両方に影響を及ぼすことで、個人の免疫反応を変化させる可能性があり、免疫療法の重要性が高まっています。したがって、個々の微生物プロファイルに関する知識を活用した個別化マイクロバイオーム療法の開発は、従来の方法と比較して効果的である可能性があります[69]。 |
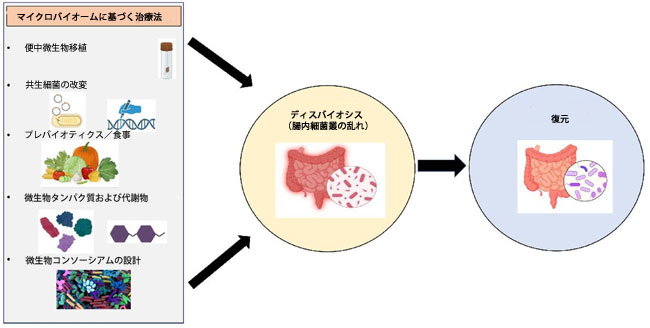 |
| 図3.腸内微生物バランスの回復におけるマイクロバイオームに基づく治療戦略の概要 |
| 糞便マイクロバイオーム移植は、有望で広く使用されているマイクロバイオームベースの治療法の1つであり、健康な個人の糞便を患者の消化管に投与して健康な微生物組成を再構築することがよくあります[70]。 バイオ医薬品もマイクロバイオームベースの治療法に不可欠な要素です。 これらを適切に投与することも効果的な治療法と考えられており、免疫調節と腸の完全性の維持に効果的に貢献する可能性があります[71]。 比較微生物叢解析を用いて特定された次世代プロバイオティクスも、消化管免疫とがん患者の免疫療法の有効性を高めることにより、宿主生物に特定の健康上の利点をもたらすことが期待されています[72]。 これらは、新しいバイオ治療戦略の新興分野に効果的に貢献する可能性があります[73]。 腸内微生物の遺伝子操作を介したCRISPR(訳者注:CRISPR(クリスパー)は、細菌の獲得免疫システムを応用した画期的なゲノム編集技術です。ガイドRNAが標的となるDNA配列を認識し、Cas9などの酵素がその部分を切断して、遺伝子の「削除・挿入・置換」を高精度かつ低コストに行います。医療、農業、基礎研究など広範囲で急速に普及しています)や塩基編集などのマイクロバイオーム編集治療法の出現により、広範な微生物移植と比較して、より優れた治療特異性が達成されています[74]。これらに加えて、既存の微生物群集を変化させ、治療効果を高めるために、改変されたマイクロバイオームや微生物コンソーシアムも投与されます。腸内細菌叢はしばしば第二のヒトゲノムと呼ばれ、腫瘍形成を促進する微小環境を効果的に形成する可能性があり、個別化治療の潜在的な標的となる可能性があります[69]。 |
| 8.プロバイオティクスのがんにおける役割 |
| 「オンコバイオーム」とは、ヒトマイクロバイオームとがんの深い相互作用を研究する分野です[75]。ヒトの宿主の体もマイクロバイオームに影響を与えるため、マイクロバイオームの変化はディスバイオシス(腸内細菌叢の乱れ)を引き起こし、多くのがんの発生につながる可能性があります[46]。 |
| プロバイオティクス微生物は、多くの治療用途があることが知られています。これらは、土着の微生物叢の影響により、消化管と関連していることが多いです[76]。大腸がん患者の腸内には、バクテロイデス、プレボテラなど、様々な菌株が定着しており、これらの菌株は、特定の発がん物質や、ヘテロ環アミン、胆汁酸塩などの腫瘍形成化合物の産生に関与していることが知られています。一部のプロバイオティクス細菌は、特定の免疫調節作用や抗がん作用を持つことが知られています。これらのプロバイオティクス化合物は、特定の発がん性化合物の生物学的修復を助けるだけでなく、細胞死や進行の調節に関与する短鎖脂肪酸などの特定の代謝産物の産生にも関与しています[63]。乳酸菌の代表的なクラスであるラクトバチルス属とビフィドバクテリウム属は、α-グルクロニダーゼ、アゾレダクターゼ、ニトロレダクターゼの酵素活性を変化させる能力により、効果的な抗がん作用を持つことが知られています。これらの酵素活性は、大腸がんの発生と進行に不可欠な役割を果たしています[77]。プロバイオティクスががんの進行抑制に関与していることは高く評価されています。表2は、いくつかのプロバイオティクス菌とそのがん抑制メカニズムを示しています。 |
| 表2.プロバイオティクスの一覧とがんにおける作用機序 |
 |
 |
 |
| これらはまた、IL-2やIL-12などのサイトカイン、抗酸化物質(SOD、CAT、GSH)、血管新生阻害因子、ムチン、ディフェンシン、IgAなどの産生と上方制御にも関与しています。また、サイトカイン応答やチロシンキナーゼ阻害にも何らかの形で関与しています。宿主体内の免疫調節は、様々な抗炎症分子の分泌によって行われ、Th細胞の応答と制御に影響を及ぼす一方で、がんの増殖は細胞分化を制御し、アポトーシスを促進することで維持されます[78]。いくつかの研究では、特定のラクチカゼイバチルス・ラムノサスGGとビフィドバクテリウム・ラクチス Bb12をオリゴフルクトース強化イヌリンとともに12週間投与すると、腸内微生物叢に影響を及ぼし、クロストリジウム・パーフリンゲンスのレベルが低下し、毒性代謝物の産生の減少、免疫応答の強化、その他の抗がん効果を通じてがんリスクが低下する可能性があることが明らかになっています[76]。 |
| 9.腸内細菌叢と乳がん:プロバイオティクス介入 |
| 乳がんは、世界中の女性に関連する悪性腫瘍の中で、最も顕著な悪性腫瘍の一つです(WHO, 2021)。乳がんは多因子疾患であるため、その発症と進行は、内的要因と外的要因の両方の影響を受けることが多いです。また、遺伝的要因、ホルモン要因、環境要因、生活習慣要因も影響します[79]。乳がんの主な組織学的型は腺がんで、主に乳管(75%)と小葉上皮(15%)に発生します。乳管がんは、原発巣内に限局するものから、基底膜を越えて転移し、乳腺実質細胞に深刻な影響を及ぼすものまで、幅広い病型があります[80]。乳がんには、トリプルネガティブ乳がん(TNBC)、乳腺パジェット病、化生がん、HER2陽性乳がん(訳者注:HER2(ハーツー)は細胞増殖に関与するタンパク質で、乳がん細胞表面に過剰発現すると増殖が促進される「HER2陽性乳がん」を引き起こします。乳がん全体の15〜20%を占め、増殖が早く再発リスクが高い特性がありますが、抗HER2薬(ハーセプチン等)による分子標的療法が有効です)など、他にも幅広い種類があります。これらの発がん性変化に加えて、乳房細胞はしこりや嚢胞形成につながる変化を起こしやすい傾向があります[79]。 |
| 腸内細菌叢が乳がんの発生と発達に及ぼす影響は、過去10年間で大きな注目を集めています。これは、免疫調節、様々な細菌代謝物の放出、エストロゲンレベルの変化など、様々な方法を介して起こります[81]。血中エストロゲン濃度の上昇は、乳がんのリスクを高める可能性があります[82]。微生物のβ-グルクロニダーゼによるエストロゲンの生体内変換能力は、乳がんに影響を与えます[83]。エストロゲンは抱合および処理された後、腸管に入り、多くの場合、β-グルクロニダーゼによって脱抱合され、糞便中に排泄されるため、リスクが低下します[82]。短鎖脂肪酸やナイシンなどのバクテリオシンなどの細菌代謝物も、乳がんに対して抗がん作用を持つ可能性があります[6]。植物性エストロゲン、リトコール酸(LCA)、カダベリンなどの特定の生理活性化合物が、乳がんの発生率と進行を抑制するという証拠もあります[84]。様々な発酵食品から得られるラクトバチルスやビフィズス菌などの腸内細菌は、様々な健康効果を持つことが知られており、効果的なプロバイオティクスと言えるでしょう。図4は、ディスバイオシスを引き起こす様々な外的要因と、バイオ医薬品がヒトの健康に及ぼす影響を示しています。適切な菌株の入手可能性、それらの生存率、そして適切な投与量を考慮する必要がある一方で、プロバイオティクスの新たなニーズが生まれています。最近のいくつかの研究では、がんとプロバイオティクス細菌の間にかなりの相関関係があることが明らかになっています[85]。 |
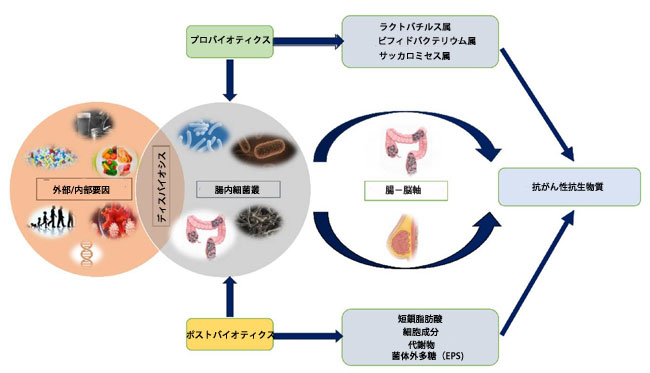 |
| 図4.プロバイオティクス、ポストバイオティクス、腸内細菌叢の相互作用と、腸-乳軸への影響におけるそれらの重要な役割および抗発がん活性の模式図 |
| プロバイオティクスは、免疫調節作用と常在菌への潜在的な作用により、乳がんに対する大きな抗がん効果を発揮します[86]。最近の研究では、プロバイオティクスの日常摂取量と乳がん発症率の間に負の相関関係があることが示されています。ラクトバチルス・アシドフィルスを経口投与したところ、対照群と比較して生存期間が有意に延長することが示されました。これらの結果は、この菌が免疫応答を調節する能力を持っていることを示しています[87]。プロバイオティクスの乳がんへの影響は、いくつかのin vitro細胞実験によっても裏付けられており、これらの菌が乳がん細胞に対してアポトーシス誘導活性または細胞傷害活性を示す証拠が断片的に示されています[88]。これらのin vitro研究に加えて、様々な動物モデルを用いた複数の研究も実施されており、乳がんの進行予防と抑制におけるプロバイオティクスの明らかな役割に関する重要な知見が得られています。図5は、プロバイオティクス投与による乳がん腫瘤の抑制率を示しています。さらに、これらの微生物は化学療法の副作用を軽減する働きもある[89]。 |
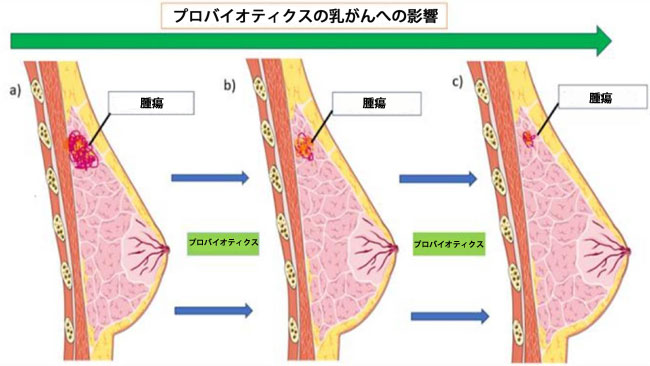 |
| 図5. プロバイオティクス投与による腫瘍の抑制 - 乳がんの進行に対するプロバイオティクスの効果を3つのステージ(a、b、c)に分けて示した図。各ステージ間でプロバイオティクスを投与した結果、ステージaからステージcにかけて腫瘍の大きさが顕著に縮小した。これは、プロバイオティクスが乳がんの非侵襲的治療選択肢となる可能性を示唆している。 |
| プロバイオティクスは微生物の恒常性を維持することで、腸内細菌叢の乱れを防ぎます。これは通常、善玉菌の個体数を増やすか、競合排除によって病原菌を排除することで起こります [90]。プロバイオティクス菌の重要なグループの一つであるラクトバチルスは、様々な健康効果を示しています。特定の病原菌の増殖を抑制することで、胃腸バリア機能を効果的に改善する可能性があります [43]。L.ラムノサス GGやラクトバチルス・カゼイなどのラクトバチルス属菌は、腸内疾患の恒常性を回復させることも知られており、特定の免疫疾患の治療にも利用できる可能性があります [91, 92]。ラクトバチルス以外にも、B. シュードロンガムやB. アドレセンティスなどのビフィドバクテリウム属菌も腸内細菌叢を変化させることが知られています [93]。また、特定の免疫調節活性にも関与しています [94]。プロバイオティクスのビフィズス菌は、腸内細菌叢の代謝活性と構成を高める働きがあることがわかっています [42]。大腸菌も、腸内細菌叢の構成を維持する効果のあるプロバイオティクス菌です。大腸菌の一種である 大腸菌ニスレ1917 は、さまざまな病原菌の付着や侵入を防ぐ保護バリアとして機能するヒト β-ディフェンシン 2 の産生を刺激することがわかっています [95]。最近の研究では、これらの菌株がサルモネラ菌、赤痢菌、カンジダ菌に対して潜在的な効果があることが明らかになっています [96]。グラム陽性菌のプロバイオティクス菌であるエンテロコッカスは、抗腫瘍剤や抗がん剤として重要な生理学的、機能的意味合いを持っており、免疫系を調整する可能性さえあります [97]。サッカロミセスもまた、非病原性のプロバイオティクス酵母であり、プロバイオティクス食品の製造に広く利用されています。中でも、S. セレビシエとサッカロミセス・ボウラディは、プロバイオティクスをベースとした治療に広く利用されています。これらの菌株は、免疫防御と短鎖脂肪酸の産生を促進することで、炎症を予防する潜在的な効果も示しています[98, 99]。 |
| 10.宿主の免疫調節に関与するプロバイオティクスとポストバイオティクス分子 |
| プロバイオティクスは免疫系の調節因子として働き、過剰な炎症と防御反応のバランスをとります。これらの微生物と免疫系との相互作用は主に腸管を介して起こり、腸管では上皮細胞と結合するか、輸送されて樹状細胞やマクロファージなどの免疫細胞と相互作用します。この相互作用はTリンパ球とBリンパ球の活性化につながり、体の免疫反応を形成します。プロバイオティクスは、宿主細胞内の遺伝子活性とシグナル伝達に影響を及ぼすことで免疫調節効果を発揮します[100, 101]。 |
| 最近の研究では、プロバイオティクスが体液性、細胞性、その他の免疫応答を誘発する役割が報告されています [44]。また、抗炎症、抗アレルギー、抗がん特性も示します。プロバイオティクスは、IgA産生、サイトカイン、抗菌物質などの産生を促進することで免疫調節を行い、腸管上皮の健康を調整します。また、腸管バリアのタイトジャンクション(訳者注:タイトジャンクション(密着結合)は、隣接する上皮細胞間を強固に接着し、細胞の隙間をシールして物質の透過を制御するバリア装置。皮膚や腸管、腎臓などで、異物の侵入や水分の蒸散を防ぎ、細胞極性を維持する重要な役割を担い、クローディンやオクルディンなどのタンパク質で構成される)を強化することで病原体の侵入を防ぎます。プロバイオティクスの抗原断片は、上皮細胞膜とパイエル板のM細胞に結合する可能性があります。この特性は、プロバイオティクスの免疫調節効果も高めます [102]。プロバイオティクスは、腸管バリアの完全性を改善し、粘膜上皮に結合して病原細菌の影響を防ぎ、それらの相互作用の機会を減らすことで免疫応答を改善します [103]。ラクトバチルス属のプロバイオティクスを対象としたいくつかの研究では、腸管上皮細胞に対するプロバイオティクスの効果について報告されています。インターロイキン10(IL-10)およびインターロイキン12(IL-12)を産生する末梢単核細胞を刺激する大きな能力が示されている[101]。L. プランタルム WCFS1を含む様々な種を対象とした様々な比較ゲノムハイブリダイゼーション研究や免疫応答研究により、LamBDCAクオラムセンシングシステム、N-アセチルグルコサミン/ガラクトサミンホスホトランスフェラーゼシステム、バクテリオシン生合成の構成要素、および輸送経路をコードする複数の遺伝子が同定された。これらの遺伝子に関連する変異は、サイトカイン産生の調節に影響を与える可能性があります[104]。 |
| 遺伝子工学的アプローチはプロバイオティクスの制御を促進する。最近の研究では、リポテイコ酸の産生を助けるホスホグリセロールトランスフェラーゼ遺伝子を除去すると、樹状細胞におけるIL-12およびTNFレベルが低下し、IL-10産生が増加することが実証されている。したがって、CD4 + T細胞の活性化を誘導する能力が低下する[105]。これらの遺伝子に加えて、特定のプロバイオティクス成分も免疫応答を制御することが知られている。ビフィドバクテリウム・アニマリス亜種ラクティスBB-12が放出するプロバイオティクスタンパク質のMALDI-TOF解析により、74種類の異なるタンパク質が明らかになり、そのうち18種類は宿主上皮細胞または細胞外マトリックスタンパク質と相互作用することができる。これらのタンパク質は、プロバイオティクス種のプラスミノーゲンへの結合、線毛形成、コラーゲンへの接着、そして免疫調節応答の誘導といった特性を高める[106]。他のいくつかの研究でも、ラクトバチルス・ラムノサスGGが様々なタンパク質を産生することが示されており、その中にはp40も含まれ、大腸炎における腸管上皮細胞のアポトーシスとバリア機能の破綻を抑制することが示されています。p40は、自然免疫とTh1免疫応答の調節においても重要な役割を果たしています[107]。 |
| プロバイオティクスは、微生物を認識し反応する役割を担うToll様受容体を活性化することで、宿主の免疫系を調整する上で重要な役割を果たします。この活性化は免疫細胞をサポートし、健康でバランスの取れた免疫系の構築に貢献します[108]。また、制御性樹状細胞を刺激することで免疫系に影響を与え、制御性T細胞(Treg)の発達と増殖を促進します。制御性T細胞は過剰な免疫反応を抑制し、炎症を軽減するのに役立ちます。プロバイオティクスの菌株や投与量によって、効果は異なります。例えば、ラクトバチルス・ラムノサスを高用量で摂取すると強い炎症を引き起こす可能性がありますが、ビフィドバクテリウム・ブレーベなどの菌株は制御性T細胞を増加させ、アレルギーに対する保護効果をもたらすことが分かっています。特定のプロバイオティクスは、制御性T細胞の数に直接影響を与えるのではなく、好ましい環境を作り出すことで間接的に制御性T細胞をサポートすることは注目に値します[109]。全体として、これらの知見は、プロバイオティクスが免疫応答を調節することにより、炎症性疾患の治療薬として使用できる可能性を示唆している[38]。図6は、プロバイオティクス、ポストバイオティクス、プレバイオティクスの相互関係を示している。 |
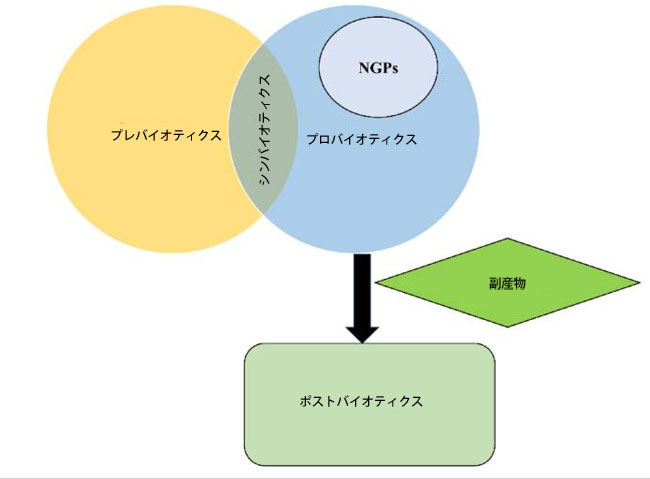 |
| 図6. ヒト腸内細菌叢におけるプロバイオティクス、プレバイオティクス、シンバイオティクス、ポストバイオティクスの相互作用 |
| ポストバイオティクスの概念は、不活化微生物の免疫調節効果に関する断片的な証拠から始まりました[110]。いくつかの臨床試験では、潜在的なポストバイオティクスの免疫防御および免疫調節作用が抗ウイルス活性を持つことも証明されています。ポストバイオティクスは、炎症性サイトカインの産生を抑制し、抗炎症性サイトカインの産生を促進するとと11.もに、TLR(訳者注:TLR(Toll様受容体:Toll-like receptor)は、マクロファージや樹状細胞などの自然免疫細胞の表面や内部に存在し、細菌やウイルスなどの病原体に固有の分子構造(PAMPs)を認識するセンサータンパク質です。これらは有害な微生物の侵入をいち早く検知し、免疫系を活性化させて炎症性サイトカインを産生させる、生体防御の初期反応における必須の役割を果たします)の発現を刺激します。これらは、自然免疫応答と獲得免疫応答の両方に関与することが知られています。ラクトバチルス属(L.アシドフィルス、L. カゼイ、L. ラムノサス)が産生するペプチドグリカンは、リポ多糖誘導性TLR-4経路を介して炎症性サイトカインを放出する能力を高めることが知られています[111]。パラプロバイオティクスという用語に続いて、パラサイコバイオティクスも登場しました[60]。 |
| 11.現在の臨床的エビデンスと課題 |
| 前臨床研究では、バイオ医薬品が腸内細菌叢に及ぼす潜在的な治療作用について支持的な結果が得られていますが、ヒトを対象とした堅牢な臨床試験データは依然として限られています。腸内細菌叢、プロバイオティクス、乳がんの関係性を検討した臨床試験はごくわずかです。微生物組成の個人差は、個別化免疫応答や腫瘍バイオマーカーにおいても懸念事項です。clinicaltrials.gov (https://clinicaltrials.gov/) (訳者注:ClinicalTrials.govは、世界中の人間を対象とした臨床試験(治験)の登録および結果を公開している、世界最大級のデータベースです)で「乳がん」「プロバイオティクス」「腸内マイクロバイオーム」というキーワードで検索したところ、2件の研究が見つかりました。一方、「プロバイオティクス」と「乳がん」というキーワードで検索したところ、20件の研究が見つかりました。一方、「ポストバイオティクス」と「乳がん」というキーワードで検索したところ、そのような記録はありませんでした。一方、WHO国際臨床試験登録プラットフォーム(ICTRP)(https://trialsearch.who.int/)を「プロバイオティクス」「腸内細菌叢」「乳がん」というキーワードで検索しても結果は得られず、「プロバイオティクス」と「乳がん」のみで検索すると19件の記録が見つかりました。これらの結果は、乳がん治療におけるこれらのバイオ医薬品の治療可能性を検討するための、明確に定義された大規模臨床試験の限界を浮き彫りにしています。 |
| 12.プロバイオティクスとポストバイオティクスの将来展望と結論 |
| 従来型薬剤に対する抗生物質耐性の台頭により、プロバイオティクス、ポストバイオティクス、そして次世代プロバイオティクスは、従来の治療法に代わる効果的な選択肢として、科学界にとって重要な関心領域となっています。個々のマイクロバイオータの特性は、個々人に合わせた治療法の有効性を高め、特に女性の死亡原因の上位にある乳がんなどの疾患において、治療効果を向上させる可能性があります。腸内マイクロバイオータとプロバイオティクス株に関する研究の進歩、そしてゲノミクスの進歩は、個別化医療への道を開きつつあり、大きな注目を集めています。しかしながら、特定の酸素感受性微生物の生存能力を維持することは、今後の研究で取り組むべき課題を提示しています。計算生物学と合成生物学の台頭は、遺伝子工学による新規プロバイオティクスの開発や、新たな標的プロバイオティクスコンソーシアムの開発に、さらに活用される可能性があります。ポストバイオティクスはプロバイオティクスと同様の利点を提供しますが、非生存性であるため、より高い安定性と安全性を備えています。現在進行中の研究は、生産、投与量、安全性の最適化に加え、乳房組織由来の微生物叢を治療用途に活用することを目指しています。結論として、プロバイオティクス、ポストバイオティクス、そして次世代プロバイオティクスは、免疫調節、がん免疫学、そしてがん治療における有望な最先端領域です。プロバイオティクスとポストバイオティクスがホリスティックヘルスに及ぼす影響はがん治療の枠を超え、腸内微生物叢の調和を維持し、免疫機能と全体的な健康状態の向上に貢献します。プロバイオティクスの投与は腸内微生物叢の調整にも役割を果たし、ポストバイオティクスの産生は全体的な健康状態に影響を与えます。したがって、プロバイオティクスとポストバイオティクスの併用投与は、乳がん治療における効果的な治療法として注目されています。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、Discov Oncol. 2026 Jan 5;17:220に掲載されたGut microbiota centered approaches for breast cancer intervention leveraging probiotics and postbiotics.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


