ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(ヨーグルト、ビフィズス菌:研究の最前線) |
ビフィズス菌と脳の相互作用を制御する:アルツハイマー病の潜在的治療戦略 |
Liting Peng et al., |
|
|
| 要約 |
アルツハイマー病(AD)は高齢者に多くみられる認知症であり、典型的には認知障害(CI)と記憶喪失の症状として現れます。病理学的には、アミロイドβ(Aβ)沈着とタウリン酸化の異常な上昇を特徴とします。急速な高齢化の進展に伴い、多くの科学者がアルツハイマー病の発症メカニズムと潜在的な治療法に焦点を当てて研究を行っています。残念ながら、現在までに非常に効果的な治療法は見つかっていません。興味深いことに、複数の研究でアルツハイマー病患者の腸内細菌叢の変化が明らかにされており、これがアルツハイマー病の病態解明の新たな道筋となる可能性を示唆しています。消化管における重要なプロバイオティクスであるビフィズス菌は、腸内細菌叢のバランス維持に重要な役割を果たしています。特筆すべきことに、アルツハイマー病患者の腸内においてはビフィズス菌の顕著な欠乏が観察されており、腸内細菌叢と脳の連携を介したビフィズス菌のアルツハイマー病への影響について、更なる研究の可能性を示唆しています。しかしながら、ビフィズス菌がアルツハイマー病を緩和するメカニズムに関する現在の研究は限られており、更なる研究が必要です。本レビューでは、アルツハイマー病患者におけるビフィズス菌の変化とその根底にあるメカニズムを検証し、アルツハイマー病治療戦略としての可能性を評価することを目的としています。 |
| 目次(クリックして記事にアクセスできます) |
| 1. はじめに |
| 2. ビフィズス菌とアルツハイマー病 |
| 2.1. 高齢化社会におけるビフィズス菌の減少 |
| 2.2. ビフィズス菌の補給はアルツハイマー病患者の腸内細菌叢を再構築する可能性がある |
| 3. ビフィズス菌が脳-腸軸を介してアルツハイマー病を改善するメカニズム |
| 3.1. ビフィズス菌は神経炎症抑制によりアルツハイマー病を改善した |
| 3.2. ビフィズス菌は短鎖脂肪酸を増加させることでアルツハイマー病を改善する |
| 3.3. ビフィズス菌は脳由来神経栄養因子を増加させることでアルツハイマー病を改善した |
| 3.4. ビフィズス菌は神経伝達物質の放出を調節することでアルツハイマー病を改善した |
| 3.4.1. セロトニン(5-HT) |
| 3.4.2. γ-アミノ酪酸(GABA) |
| 4. 限界 |
| 5. 結論と今後の展望 |
本文 |
| 1.はじめに |
| アルツハイマー病の治療は、症状管理のためのコリンエステラーゼ阻害薬、アミロイドβ(Aβ)プラークおよびp-タウに対するモノクローナル抗体など、その中核となる神経病理学的特徴を標的とした戦略によって大きく左右されます(1-6)。しかし、これらのアプローチによる疾患進行の阻止または回復における臨床的有効性は、主にアルツハイマー病の病因が多因子性であることと、単一標的治療の失敗により、依然として著しく限られています(7, 8)。この重大なギャップは、神経変性を媒介する新たな経路の探究が緊急に必要であることを浮き彫りにしています。アルツハイマー病研究における注目すべき現象として、腸-脳軸の認識の高まりが挙げられます。腸-脳軸は、高度に動的な腸内細菌叢を、脳の恒常性と神経炎症に重要かつ調整可能な影響を与える因子として位置付けています(9, 10)。 |
| ヒトの消化管は複雑で密度の高い微生物生態系であり、約 10~100 兆個の常在微生物細胞で構成されています (9)。興味深いことに、腸内細菌叢は神経伝達物質、神経調節物質、およびアミノ酸由来のさまざまな代謝物を分泌できます (11, 12)。こうした状況において、アルツハイマー病患者の腸内細菌叢の不均衡を一貫して報告するエビデンスが蓄積されており、微生物組成の変化と神経変性プロセスの間には強い関連があることが示唆されています (13)。重要な点は、腸内の重要なプロバイオティクス属であるビフィズス菌の減少が、アルツハイマー病における重要な微生物特性の 1 つになっていることです (14, 15)。ビフィズス菌の存在量は加齢とともに急激に減少し、これがアルツハイマー病の主要な非遺伝的リスク要因であるため、この発見は特に重要です (14, 16, 17)。さらに、ビフィズス菌は、病原菌の競合的排除、腸粘膜バリアの強化、有益な短鎖脂肪酸(SCFA)の主要産生など、不可欠な役割を果たしています(18~20)。加齢に伴うビフィズス菌の減少、アルツハイマー病患者における顕著な減少、そして特に全身性炎症と代謝の健康状態を調節する上での重要な機能という相乗効果から、重要かつ時宜を得た仮説が浮かび上がります。ビフィズス菌の減少は、単にアルツハイマー病の結果であるだけでなく、腸-脳軸を介してアルツハイマー病の病因に積極的に寄与している可能性があるのです。 |
| そのため、ビフィズス菌をプロバイオティクスとして利用し、アルツハイマー病病態を改善する治療効果が期待されています(21)。最新の研究では、その有益な効果は、複数の相互に関連したメカニズムによってもたらされることが示唆されています。具体的には、微生物の安定性を回復させることで炎症誘発性分子の循環プールを減少させること(22–24)、腸管上皮の完全性を強化して細菌性エンドトキシン(リポ多糖など)の転座を防ぎ、末梢炎症および神経炎症を緩和すること(25–27)、そして短鎖脂肪酸などの代謝産物を利用してミクログリア機能、神経栄養因子発現(BDNFなど)、および神経伝達物質系を直接調節すること(24, 28–32)などが挙げられます。本レビューは、アルツハイマー病に関連するビフィズス菌の変化に関する最新のメカニズム解明と、ビフィズス菌補給がアルツハイマー病介入のための新たな標的戦略であることを裏付けるエビデンスを批判的に統合することを目的としています。 |
| 2. ビフィズス菌とアルツハイマー病 |
| 2.1. 高齢化社会におけるビフィズス菌の減少 |
| 腸内細菌叢は、食事や睡眠不足など、私たちの日常生活に非常に敏感です(33)。腸内フローラの恒常性の維持は、身体全体の健康状態と密接に関連しています。興味深いことに、加齢プロセスが腸内細菌叢の構成に大きな影響を与えることが明らかになりつつあり、研究が進展しています(34, 35)。加齢は認知症の発症において極めて重要な要因ですが、微生物、加齢、認知症の複雑な相互作用は依然として解明されていません。これら3つの概念の関連性は、まだ完全に解明されていません。この関係性を理解することで、認知機能に対するそれらの総合的な影響についての理解が深まり、加齢に伴う神経機能低下を軽減するための戦略につながる可能性があります。 |
| 乳児の腸内細菌叢には大きな個人差があり、経膣分娩(36)や母乳育児(37)など、複数の経路を通じて母親の腸内細菌叢に類似した微生物群集を獲得します。ヒトの腸内細菌叢の多様性は加齢とともに増加します。ある日本の研究では、参加者を乳児、成人、高齢者の3つの年齢層に分類し、各年齢層における腸内細菌叢の変化を調査しました(2)。この研究では、乳児層では放線菌の相対的存在量が高く、成人層ではクロストリジウムの相対的存在量が増加し、高齢者層ではバクテロイデス属、ベータプロテオバクテリア属、デルタプロテオバクテリア属の有病率が有意に高いことが明らかになりました(図1)。 |
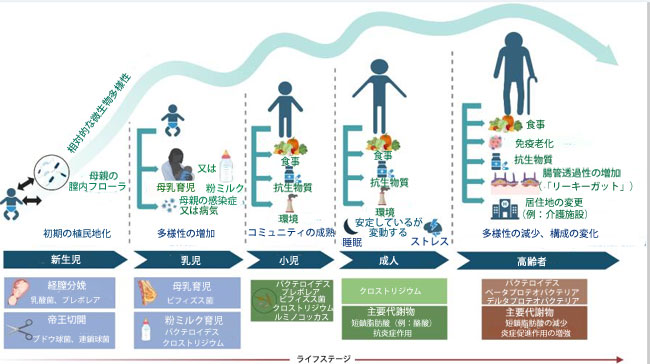 |
| 図1. 人間の腸内細菌叢の構成は、加齢やライフスタイルの変化など、さまざまな要因によって動的に変化します。(画像はBioRender.comを使用して作成しました。) |
| しかし、腸内細菌叢の変化は、日常生活や食事などの他の要因による影響を排除することはできない。そのため、年齢が腸内細菌叢の変化に影響を与える独立した要因であるかどうかは現時点では不明であり、さらなる研究が必要である。Parker Aらは、腸内細菌叢の変化によって、腸、眼、脳のバイオマーカーを調整できることを発見した (34)。若いマウスから高齢マウスに腸内細菌叢を移植すると、レシピエントの微生物組成が変化し、ビフィズス菌アニマリス、ユーバクテリウム属、アッカーマンシア・ムシニフィラ、クロストリジウム・コクリータムなどの分類群の相対的存在量が大幅に増加する。同時に、網膜における炎症性補体タンパク質C3の発現を減少させ、リポ多糖結合タンパク質(LBP)の血清濃度を低下させることで、炎症を軽減する (34)。逆に、高齢マウスの糞便細菌叢を若齢マウスに移すと、ミクログリアの活性化が促進される一方で、中枢神経系(CNS)の炎症が悪化する(34)。近年、ミクログリアの過剰活性化は神経炎症の重要な誘発因子であり、認知機能障害の重要な原因であることが指摘されている(38)。対照的に、若齢マウスの糞便細菌叢を変化させることで、これらの有害な影響が逆転した。これは、腸内細菌叢の構成が加齢とともに変化し、それによって老化と認知機能の低下が促進されることを示唆する間接的な証拠となる可能性がある。したがって、高齢者の腸内におけるビフィズス菌の著しい減少をアルツハイマー病の新たな治療標的として利用できる可能性については、さらなる研究が必要である(35)。 |
| 2.2. ビフィズス菌の補給はアルツハイマー病患者の腸内細菌叢を再構築する可能性がある |
| アルツハイマー病患者は、アミロイドβ沈着とタウタンパク質の過リン酸化を特徴とする典型的な病態生理学的特徴に加え、認知機能障害(CI)や記憶障害などの臨床症状を示す。しかしながら、アルツハイマー病患者の腸内細菌叢には、マイコバクテリウム・アビウムの相対的存在量の増加、ビフィズス菌およびファーミクテスの相対的存在量の減少など、乱れがあることを示唆するエビデンスが増えつつある(29, 39, 40)。これまでの研究では、特定の細菌叢がアルツハイマー病に治療効果を発揮することは確立されておらず、この分野における重大なギャップが浮き彫りになっている。しかしながら、科学者たちはプロバイオティクスの補給によって細菌叢の不均衡を改善し、最終的にアルツハイマー病を軽減しようと試みている。 |
| プロバイオティクスのこの治療効果は、アルツハイマー病患者に限らず、健康的な老化という幅広い文脈にも及びます。Shi Sらは、ビフィドバクテリウム ロンガム BB68S(BB68S、5×1010 CFU/サシェ)を8週間毎日経口投与したところ、介入後のRBANSスコア(訳者注:RBANS(アールバンズ)は、即時記憶、遅延記憶、言語、注意、視空間・構成の5つの認知領域(12の下位項目)を短時間で評価する神経心理学検査です。健常~軽度認知障害(MCI)~中等度認知症の脳機能を評価でき、平均100、標準偏差15の指標得点で算出されます)合計が18.89ポイント上昇し(p<0.0001)、健康な高齢者の認知機能が著しく改善したことを実証しました。また、即時記憶、視空間認知能力/構成能力、注意力、遅延記憶に有意な改善が見られました(41)。同時に、ビフィドバクテリウム ロンガム BB68S投与により、ラクノスピラ属やビフィドバクテリウム属などの有益な細菌種の相対的存在量が上昇し、コリンセラ属やパラバクテロイデス属などの認知障害に関連する分類群の有病率が低下しました(41)。研究結果は、プロバイオティクスの補給が認知障害を軽減する可能性があることを示唆していますが、さらなる検証が必要です。この研究の主な限界としては、(42) 末梢系および腸内細菌叢の代謝物の分析が不足しているため、どの代謝物が治療効果の源であるかが不明瞭であること (43)、認知機能は大幅に改善したものの、特定の認知領域および腸内細菌叢の変化は有意ではなかったこと (44)、8週間の研究ではこれらの結果を観察するには不十分な可能性があるため、より長期的な研究が必要であること (45)、介入期間中の参加者の食事は厳密に管理されていなかったため、食事の変化が腸内細菌叢に与える影響を排除できないことなどが挙げられます。今後の研究では、厳格な食事管理など、より厳密に設計された研究が必要です。 |
| さらに、腸内細菌叢の調整による認知機能への効果は、プロバイオティクスとプレバイオティクスを組み合わせたシンバイオティクス的アプローチによってさらに高められる可能性がある(46)。ランダム化二重盲検プラセボ対照試験では、ビフィドバクテリウム・アニマリス亜種ラクティスGCL2505とイヌリンを含むシンバイオティクスサプリメントを12週間摂取させたところ、高齢者の参加者において、注意力、認知柔軟性、実行機能など、全体的な認知機能が有意に改善したことが示された(47)。この介入により、糞便中のビフィドバクテリウム数が顕著に増加し、いくつかの炎症マーカーが正に調整されたことから、腸内環境の改善と炎症の緩和によって認知機能の改善が促進されたことが示唆される(臨床的に関連性の高い実験については表1を参照)。 |
| 表1.ビフィズス菌によるアルツハイマー病改善に関する部分的な知見(試験研究) |
 |
 |
 |
 |
AD(アルツハイマー病)、MCI(軽度認知障害) |
| これらの研究は、ビフィズス菌サプリメントが認知機能を向上させるというエビデンスを示しています(41, 46)。しかし、重要な疑問が残ります。これらの腸内細菌はどのようにして脳に深い影響を与えるのでしょうか?ビフィズス菌が腸-脳相関を制御するメカニズムは、解明が始まったばかりです。これらの経路を解明することは、プロバイオティクス療法をアルツハイマー病に対する標的臨床介入に繋げるために不可欠です。 |
| 3. ビフィズス菌が脳-腸軸を介してアルツハイマー病を改善するメカニズム |
| 神経系と腸管の間にはコミュニケーションが存在することを示唆するエビデンスが増えており、微生物-腸-脳軸は神経変性疾患の研究において極めて重要な概念として浮上しています。このコミュニケーションは、主に免疫関連、神経系、内分泌系、代謝系のシグナル伝達経路を介して行われます(54)。したがって、腸内細菌叢の恒常性の維持は、脳機能を最適に保つために不可欠です。広く利用されているプロバイオティクスであるビフィズス菌は、治療目的で腸内フローラ環境を調整するために、単独で、または他のプロバイオティクスと併用して投与されることが多く、現在、腸疾患、糖尿病(55)、肝疾患(56)の治療に広く利用されています。 アルツハイマー病患者の腸内細菌叢内のビフィズス菌のレベルが低下しているという観察を踏まえ、研究者は、ビフィズス菌の補給が単独または他の戦略と組み合わせてアルツハイマー病の潜在的な治療法になる可能性があるという仮説を立てました。 |
| 3.1. ビフィズス菌は神経炎症抑制によりアルツハイマー病を改善した |
| 神経炎症はアルツハイマー病の主要な病理学的特徴であり、その起源はしばしば腸管に遡る(57)。腸内細菌叢と腸管免疫系の共生関係の破綻は、炎症性サイトカインの放出と腸管透過性亢進を特徴とする炎症プロセスを悪化させる可能性があり、しばしば「リーキーガット」(図2)と呼ばれる(58)。重要なことに、この炎症は腸-脳軸に沿って広がり、脳内の神経炎症につながる(39)。一方で、腸内細菌叢の乱れはミクログリアを異常に活性化し、ケモカインの放出を促して神経炎症を誘発する(59, 60)。他方では、リポ多糖の産生を促進し、腸の炎症につながる(61)。高齢者のように腸管および血液-脳関門(BBB)に障害のある集団では、リポ多糖は脳に移行しやすくなります(62)。特に、アルツハイマー病患者の血漿中リポ多糖濃度は健常者と比較して有意に高く、アルツハイマー病患者の軽度の慢性炎症状態に寄与しています(63)。脳に到達したリポ多糖はミクログリアと相互作用し、Toll様受容体(TLR)を活性化させ、強力な神経炎症反応を引き起こします(39)。 |
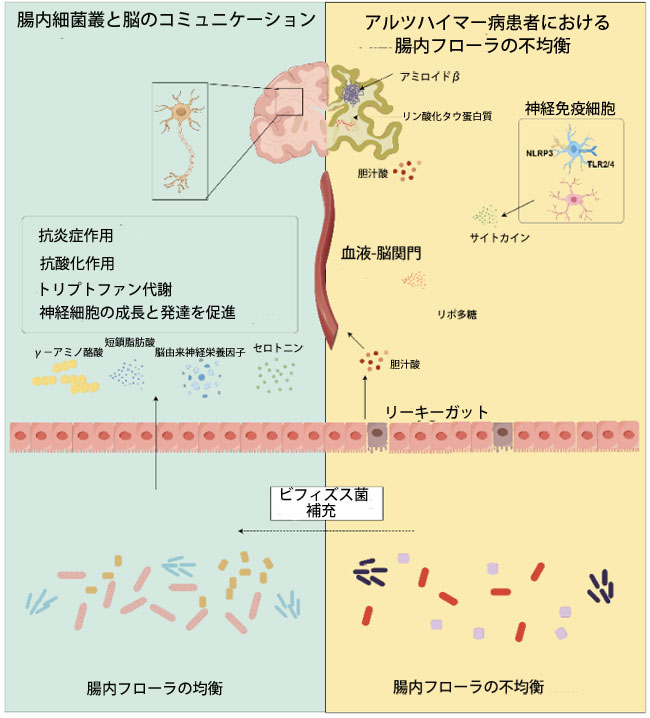 |
図2. ビフィズス菌を補給することで、ガンマアミノ酪酸、短鎖脂肪酸、脳由来神経栄養因子、セロトニンの生成を促進し、神経炎症を軽減し、ニューロンの成長と発達を促進し、アルツハイマー病を改善します。(画像はFigdrawを使用して作成)。 NLRP3(NOD様受容体3)、TLR2/4(Toll様受容体2/4)。 |
| 複数の研究により、ビフィズス菌(単一菌株または複合製剤)の投与は、結腸組織におけるTNF-αやIL-1βなどの炎症誘発因子の発現を有意に減少させ、NF-κB+CD11c+炎症誘発性免疫細胞の浸潤を減少させることが示されています(64–66)。これは、ビフィズス菌が局所的な腸の炎症を効果的に緩和することを示しています。さらに、腸管バリアの修復と腸内細菌叢の組成の最適化により、ビフィズス菌による治療は血中および糞便中のリポ多糖濃度を有意に低下させます(64, 66)。これは、腸管由来の全身性炎症、すなわち代謝性エンドトキシン血症を効果的に抑制することを意味します。この末梢炎症シグナルの減少は、その後中枢神経系にも波及します。複数の関連モデルにおいて、ビフィズス菌による介入は、認知機能に重要な脳領域である海馬におけるTNF-α、IL-1β、IL-6などの主要な炎症誘発因子の発現を有意に減少させ、同時にNF-κBシグナル伝達経路の活性化を阻害しました(64–66)。この神経炎症性微小環境の直接的な緩和は、ビフィズス菌がアルツハイマー病の進行を緩和する重要なメカニズムであると考えられます。 |
| 3.2. ビフィズス菌は短鎖脂肪酸を増加させることでアルツハイマー病を改善する |
| 短鎖脂肪酸は、腸内細菌叢による食物繊維の発酵によって生成される主要な代謝産物です。中でも、酢酸、プロピオン酸、酪酸は最も広く研究されており、機能的に重要な成分です。これらは「腸内細菌叢と宿主」間の重要なコミュニケーション分子とみなされており、神経栄養因子の調節において中心的な役割を果たしています(67)。重要な酸産生菌であるビフィズス菌は、短鎖脂肪酸の生成を促進することで、腸-脳軸機能に正の影響を与えます(68)。これらの短鎖脂肪酸は、血液-脳関門を通過して中枢神経系に直接作用するだけでなく、末梢経路を介して間接的に脳機能と行動を制御することができます(67)。例えば、Fernandoらは、短鎖脂肪酸が腸-脳軸機能にどのように作用するかについて報告しています。ビフィドバクテリウム・ブレーベ、ビフィドバクテリウム・ロンガム、ラクトバチルス・ラムノサスの複合製剤を補給すると、腸内の短鎖脂肪酸の総量が大幅に増加し、ビフィドバクテリウムが短鎖脂肪酸の生成を促進する上で重要な役割を果たしていることが分かりました(69)。 |
| ビフィズス菌は主にブドウ糖代謝によって酢酸と乳酸を産生し、酢酸が主な最終産物である (17)。短鎖脂肪酸がアルツハイマー病を改善するメカニズムには複数の経路が関与している。まず、腸管バリア機能の維持において、酢酸は結腸上皮細胞の重要なエネルギー源として、細胞の正常な増殖と機能をサポートし、それによって腸粘膜の完全性を確保する (70)。さらに重要なことに、酢酸はタイトジャンクション(TJ)タンパク質(クローディン、オクルディン、ZO-1など)の発現と安定性をアップレギュレーションし、腸管透過性(いわゆる「リーキーガット」)を低下させる。これにより、エンドトキシン(リボ多糖など)などの有害物質が血流に入るのを効果的に防ぎ、リポ多糖によって引き起こされる全身性および中枢神経系の炎症を緩和し、間接的な神経保護を達成する (71)。 |
| 第二に、短鎖脂肪酸、特に酪酸は強力な直接的な神経保護作用を示す(72)。ビフィズス菌は酪酸を直接生成しないものの、その代謝産物である酢酸と乳酸は、他の酪酸産生細菌(クロストリジウムやユーバクテリウムなど)の基質として機能し、「クロスフィーディング」機構を通じて間接的に酪酸の生成を促進する(図3)(73)。 |
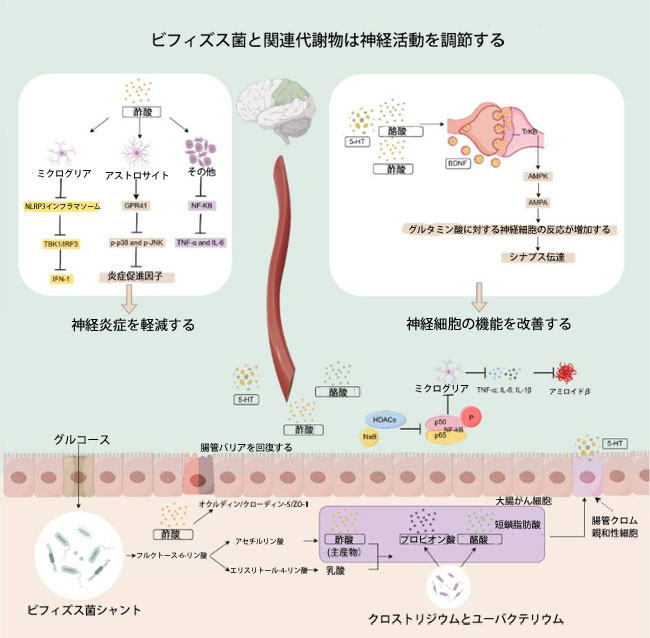 |
図3. ビフィズス菌とその関連代謝物がアルツハイマー病を改善するメカニズム。 ビフィズス菌が産生する短鎖脂肪酸の主成分は酢酸です。酢酸と乳酸は、他の微生物群(クロストリジウム属やユーバクテリウム属)の代謝基質として働き、プロピオン酸と酪酸を生成します。酪酸は、腸管クロム親和性細胞におけるセロトニンの産生を促進します。これらの代謝物は、炎症性因子の放出を抑制し、アミロイドβの産生を減少させ、神経機能を高めることでアルツハイマー病を改善します。(画像はFigdrawを使用して作成) GABA(ガンマアミノ酪酸)、SCFA(短鎖脂肪酸)、BDNF(脳由来神経栄養因子)、5-HT (セロトニン)、Aβ(アミロイドβ)、BA(胆汁酸)、LPS(リポ多糖)、 |
| この相乗的な酸産生プロセスは宿主の健康にとって極めて重要です。アルツハイマー病マウスモデルにおいて、酪酸ナトリウム(NaB)の介入はシナプス可塑性を著しく向上させただけでなく、脳内の炎症性サイトカイン(TNF-α、IL-6、IL-1β)のレベルを直接的に低下させ、ミクログリアの過剰活性化を抑制し、アミロイドβの沈着を予防しました(74)。その分子メカニズムはGPR109A(訳者注:GPR109A(HCA2)は、ナイアシン(ビタミンB3)や腸内細菌が生成する酪酸をリガンドとするGタンパク質共役受容体です。主に結腸、脂肪組織、免疫細胞に発現し、抗炎症作用や脂質代謝改善、がん抑制(特に大腸がん)に寄与する機能分子です)受容体への結合に関与しており、GPR109A受容体はPPAR-γ(訳者注:PPARγ(ペルオキシソーム増殖因子活性化受容体γ)は、主に脂肪組織に存在し、脂肪細胞の分化や脂質・糖代謝を調節する核内受容体(転写因子)です。インスリン感受性を改善する役割を持ち、チアゾリジン系薬剤(ピオグリタゾンなど)の標的として糖尿病治療において重要な分子です)の発現をアップレギュレーションし、TLR4/NF-κBシグナル伝達経路の活性化を阻害します。このプロセスはミクログリアにおけるM1/M2極性不均衡を修正し、最終的にはマウスの認知障害を改善する可能性があります(75)。酪酸に加えて、酢酸もミクログリア上のGPR41(訳者注:GPR41(別名:FFAR3)は、主に腸内細菌が産生する短鎖脂肪酸(特にプロピオン酸)をリガンドとするGタンパク質共役受容体です。交感神経節や腸管内分泌細胞に発現し、エネルギー消費の増大、食欲抑制ホルモン(PYY)の分泌促進、血糖値の調節など、腸-脳連関を通じた代謝恒常性の維持に重要な役割を果たします)などの受容体を活性化することで抗神経炎症作用を発揮し、p38 MAPK、JNK、NF-κBなどの炎症誘発性シグナル伝達経路を阻害します(76–78)。上記の研究は、短鎖脂肪酸および関連塩、特に酪酸と酪酸分子がアルツハイマー病の改善に大きな可能性を秘めていることを実証しています。 |
| 要約すると、現在のエビデンスは、ビフィズス菌が短鎖脂肪酸の生成と組成を調節することで多面的な機能を発揮できることを強く示唆しています。これらの機能には、腸管バリアの強化、全身性抗炎症作用、そして神経炎症の抑制、アミロイドβ蓄積の減少、シナプス機能の改善といった直接的な神経保護作用が含まれます。したがって、ビフィドバクテリウム-短鎖脂肪酸経路を標的とすることは、アルツハイマー病への介入における非常に有望な治療戦略であり、それに関連する分子メカニズムは重要な理論的根拠となります(79–85)。 |
| 3.3. ビフィズス菌は脳由来神経栄養因子を増加させることでアルツハイマー病を改善した |
| 脳由来神経栄養因子(BDNF)は、ニューロンの生存、成長、機能に不可欠な重要なタンパク質である(86)。脳由来神経栄養因子が神経新生とシナプス可塑性を促進することは、学習と記憶の生物学的基盤を構成する。アルツハイマー病患者の脳内脳由来神経栄養因子レベルは、疾患の重症度と負の相関関係にあることを示す確固たる証拠がある(87, 88)。近年、腸-脳軸を介した脳由来神経栄養因子を介した脳機能の調節は、神経変性疾患に対するプロバイオティクス介入の重要な候補メカニズムとして浮上している(89)。ビフィズス菌自体は脳由来神経栄養因子を産生しないが、複数の研究で宿主の脳内で脳由来神経栄養因子レベルを有意に上昇させる能力があることが実証されている(90)。 |
| ビフィズス菌が脳由来神経栄養因子をアップレギュレーションするメカニズムは多面的です。分子シグナル伝達レベルでは、脳由来神経栄養因子は受容体TrkBを活性化し、長期増強(LTP)、樹状突起棘の成長と成熟、成体海馬神経新生といった中核脳機能を調節します(91, 92)。エピジェネティックレベルでは、ビフィズス菌はヒストン修飾に影響を及ぼすことで脳由来神経栄養因子の発現を促進します。例えば、ビフィドバクテリウム・ビフィダムBGN4とビフィドバクテリウム・ロンガムBORIは、ヒストンH3リジン9(H3K9me3)のトリメチル化を増加させることで脳由来神経栄養因子の発現を効果的に促進し、マウスの加齢に伴う認知障害を改善することが示されています(93)。 |
| しかし、これらのメカニズムの根底にあるより深い上流の調節は、腸内細菌叢の乱れによって引き起こされる神経炎症の抑制と密接に関連しているようです。腸内細菌叢の乱れ、特に老化モデルやアルツハイマー病モデルでは、プロテオバクテリアなどの炎症誘発性細菌の増加と、それに伴うリポ多糖産生の上昇が起こります(64)。リポ多糖は複数のメカニズムを通じて血液-脳関門を損傷し、敗血症関連脳症(SAE)などのさまざまな脳疾患の発症を促進します(44)。リポ多糖が血液-脳関門を破壊する主な方法は、炎症を誘発し、内皮細胞に直接作用することです。リポ多糖はToll様受容体4(TLR4)に結合してNF-κBの発現を刺激します(94)。活性化されたNF-κB経路は、その後、オクルディンなどのタイトジャクションタンパク質の発現を低下させることで血液-脳関門の透過性を高めます(95, 96)。このバリアの損傷により、循環しているリポ多糖や有害化学物質が中枢神経系に侵入しやすくなり(44)、結果として中枢神経系機能障害を引き起こします。活性化NF-κBは、TNF-αやIL-1βなどの炎症性サイトカインの放出を誘導するだけでなく、脳由来神経栄養因子の発現を抑制し、アミロイドβ産生経路における重要な酵素であるβセクレターゼとγセクレターゼの発現を亢進させます(97, 98)。これにより、「炎症-アミロイドーシス-脳由来神経栄養因子抑制」という悪循環が生じ、最終的に認知機能障害につながります(99)。 |
| このような背景から、ビフィズス菌の治療効果を直接示す研究が数多く発表されています。例えば、ビフィドバクテリウム・アドレセンティスNK98とラクトバチルス・ロイテリNK33の併用療法は、海馬における脳由来神経栄養因子発現を亢進させるだけでなく、NF-κBシグナル伝達経路を相乗的に阻害し、神経炎症を軽減することが示されました(100)。同様に、ビフィドバクテリウム・ブレーベCCFM1025などの菌株を用いた治療は、シナプス可塑性を高め、脳由来神経栄養因子およびシナプス後肥厚部タンパク質95(PSD-95)を含む主要なシナプスタンパク質のレベルを上昇させることが示されています(20)。さらに最近の研究では、このプロセスの詳細なメカニズムがさらに解明されています。例えば、ビフィドバクテリウム・ロンガムNK46は、単独またはラクトバチルス・ムコサエNK41(NKc)との併用において、リポ多糖産生腸内細菌の増殖を効果的に抑制し、血中リポ多糖濃度を低下させることで、前述の炎症カスケードをその発生源から阻害しました(64)。生体内研究では、NK46またはNKcの経口投与が、アルツハイマー病および高齢マウスモデルの海馬におけるNF-κBの活性化を有意に阻害することが確認されました(64, 101)。これはBDNFの抑制を緩和し、海馬における脳由来神経栄養因子発現と脳由来神経栄養因子陽性ニューロン数の顕著な増加をもたらし、認知障害の改善を伴いました(64, 99)。 |
| 注目すべきことに、ビフィズス菌の効能は他の病理学的プロセスとの関連にも及んでいます。例えば、歯周病原菌であるポルフィロモナス・ジンジバリスによって誘発される認知機能障害モデルにおいて、ビフィドバクテリウム・ビフィダムNK391とラクトバチルス・ペントーサスNK357の組み合わせは、NF-κB経路を阻害することで、海馬脳由来神経栄養因子およびN-メチル-D-アスパラギン酸受容体(NMDAR)の抑制レベルを同様に回復させました(66)。 |
| 結論として、ビフィズス菌は多層的なメカニズムネットワークを通じて脳由来神経栄養因子をアップレギュレーションします。エピジェネティックな修飾を介して脳由来神経栄養因子遺伝子発現を直接促進するだけでなく(93)、より重要な点として、腸内細菌叢の再構築、リポ多糖の産生と吸収の阻害、NF-κBを介した神経炎症の抑制によって、脳由来神経栄養因子発現の抑制を緩和します。このプロセスは、アミロイドβ病変の緩和やシナプス機能の維持(64、66、91~93、99、102)といった他の機能と密接に関連しており、アルツハイマー病改善のための強固な理論的根拠となります。 |
| 3.4. ビフィズス菌は神経伝達物質の放出を調節することでアルツハイマー病を改善した |
| 神経伝達物質は、神経細胞間コミュニケーションの基本的な媒介物質として機能し、正常な脳機能の維持に不可欠である(103, 104)。これらの分子は神経シグナル伝達を促進するだけでなく、認知プロセス、感情反応、行動結果の調節においても極めて重要な役割を果たしている(105)。本節の目的は、ビフィズス菌がセロトニン(5-HT)やγ-アミノ酪酸(GABA)などの主要な神経伝達物質を調節し、アルツハイマー病に対する潜在的な治療効果を発揮するメカニズムを明らかにすることである(図2)。 |
| 3.4.1. セロトニン(5-HT) |
| 中枢神経系において広く研究されている神経伝達物質である5-HT(訳者注:5-HT(5-ヒドロキシトリプタミン)は、別名「セロトニン」と呼ばれる、脳内神経伝達物質、ホルモン、生理活性アミンの一種です。精神の安定、睡眠、消化管の運動、血小板凝集、血管収縮など、心身の機能において多岐にわたる重要な働きを担っています)は、中枢および末梢の両方の生理学的プロセスに関与し、多様な機能を調節しています(105)。例えば、アルツハイマー病マウスモデルでは、アミロイドβの蓄積は5-HT2A受容体(訳者注:5-HT2A受容体は、脳や血管、血小板に存在するセロトニン受容体の一種で、気分、幻覚、血管収縮に関与する主要な薬理標的です。統合失調症やうつ病治療において、受容体の遮断(クロザピン等)や刺激(シロシビン等)が研究されており、幻覚や認知機能障害、抗うつ作用に深く関わっています)の発現低下と相関しています(106)。一方、5-HT1B受容体(訳者注:5-HT1B(5-ヒドロキシトリプタミン1B)受容体は、主に脳血管や三叉神経終末に存在するセロトニン受容体の一種です。片頭痛の急性期治療薬である「トリプタン製剤」がこの受容体に作用し、血管収縮と神経ペプチド放出抑制により頭痛を緩和します)および5-HT2C受容体(訳者注:5-HT2C受容体は、脳内のセロトニン受容体の一種で、摂食行動、食欲、気分、不安、運動機能の調節に深く関与するGタンパク質共役受容体です。食欲抑制や不安改善の治療標的として重要であり、抗うつ薬、抗精神病薬の作用メカニズムにも関連しています)を標的とすることで、アミロイドβの神経毒性およびタウの過剰リン酸化を軽減できる可能性が示されています(107, 108)。特に、体内の5-HTの90%以上は腸管のエンテロクロマフィン(EC)細胞(訳者注:エンテロクロマフィン(EC)細胞は、腸粘膜に存在し、主にセロトニン(5-HT)を合成・分泌する内分泌細胞です。消化管の運動や粘膜の感覚、特に不快な刺激を感知して迷走神経へ伝達する役割を担い、内臓の痛みや不安に関与します。胃にある類似の細胞(ECL細胞)は胃酸分泌を調節します)によって合成されており、このプロセスにおいて腸内細菌叢とその代謝物、特に短鎖脂肪酸が重要な調節因子となっています(109)。研究によると、これらの短鎖脂肪酸、特に酪酸はエンテロクロマフィン細胞を直接刺激し、「微生物叢-腸-脳」コミュニケーションネットワーク内に直接的なシグナル伝達軸を確立できることが示されています(110)。 |
| これに基づき、短鎖脂肪酸の主要生産菌であるビフィズス菌は、中枢 5-HT レベルを間接的に調整する能力があると考えられています (111–113)。ビフィドバクテリウム アニマリス亜種ラクティス HN019 (B. ラクティス HN019TM) は乳児用食品に利用されており、研究では高齢者の正常な生理機能の維持に効果があることが実証されています。これは、微生物発酵によって生産される 短鎖脂肪酸による 5-HT シグナル伝達の調節に関連している可能性があります (19)。Zhang S らは、APP/PS1 マウスにプレバイオティクスを補給して腸内プロバイオティクスの成長と発達を刺激し、ビフィズス菌の相対的存在量の有意な増加と、APP/PS1 マウスの脳内神経伝達物質γ-アミノ酪酸および 5-HT の濃度の変化を発見し、APP/PS1 マウスの認知機能障害を改善しました (114)。この研究では、直接的なプロバイオティクス補給ではなくプレバイオティクスを採用しましたが、「ビフィズス菌の増加 - 脳由来神経栄養因子レベルの上昇 – アルツハイマー病表現型の改善」という因果関係の連鎖を裏付ける重要な間接的な証拠を提供しています。 |
| 3.4.2. γ-アミノ酪酸(GABA) |
| GABA(訳者注:GABA(ギャバ、γ-アミノ酪酸)は、ストレス軽減、リラックス効果、睡眠の質向上、血圧低下の機能を持つアミノ酸の一種です。脳や脊髄で興奮を鎮める神経伝達物質として働き、現代社会で不足しやすいストレス対策成分として注目されています)は哺乳類の中枢神経系における主要な抑制性神経伝達物質である(115)。GABAはニューロン間のシグナル伝達を媒介し、GABA受容体を活性化することでニューロンの興奮性を調節する(116)。アルツハイマー病の病態において、GABA作動系の調節不全は、ニューロンの過興奮性、神経ネットワーク活動の障害、神経炎症、シナプス障害につながる可能性がある(117)。理論的には、GABAシグナル伝達を増強することで興奮性と抑制性のバランスを回復することは、アルツハイマー病に対する実行可能な治療戦略となる(118, 119)。腸内細菌叢はGABAの重要な末梢供給源と考えられており、特定のビフィズス菌株はグルタミン酸をGABAに変換する遺伝的基盤を有している(120)。 |
| 新たな研究によると、ヒトの消化管におけるGABAは、腸内細菌叢による食事性グルタミン酸ナトリウム(MSG)の変換に由来する可能性があることが示唆されている(31, 121)。しかしながら、腸内由来のビフィドバクテリウム株のGABA合成能力については、十分な研究がなされていない。現在、ビフィズス菌におけるGABA合成に関与する主要な遺伝子は、gadBとgadCである(30)。gadB遺伝子は、ピリドキサールリン酸に依存するグルタミン酸脱炭酸酵素をコードしており、グルタミン酸からGABAを脱炭酸して生成する触媒作用を持つ。一方、gadC遺伝子は、細胞内GABAと細胞外グルタミン酸の交換を促進するタンパク質であるグルタミン酸/GABA対向輸送体をコードしている。その結果、Duranti S et al. NCBI遺伝子データベースのデータを利用し、gadBおよびgadC遺伝子を発現するビフィドバクテリウム株の解析を行い、1002種のビフィドバクテリウムからgadBおよびgadCをコードする81株を同定しました。これらの株には、 B. アドレセンティス、B. アンギュラタム、B. デンティウム、B.メリシクム、B.モウカラベンセ、B.ルミナンチウム、B.サミリイが含まれます(30)。特に、B.アドレセンティス株は、そのゲノム内で最も高いGad遺伝子発現を示し、in vitro試験では、B. アドレセンティスPRL2019やB. aアドレセンティスHD17T2Hなどのように、その前駆体の65%以上をGABAに効率的に変換する能力があることが明らかになりました。これは、このビフィドバクテリウム属分類群が、同属の中で強力なGABA産生菌であることを示しています(30)。Héctor Tamés らは、様々なプロバイオティクス株が乳の発酵においてGABA産生を促進する効果を評価するため、計算シミュレーションとin vitro実験を行い、特定の株であるIPA60004が優れた生存率を示しただけでなく、乳サンプル中のGABA濃度も上昇することを発見しました(122)。E. Barrettらは、ヒト腸由来の91株の細菌を評価した結果、ビフィズス菌によって合成されるGABAには大きなばらつきがあり、ラクトバチルス・ブレビスとビフィドバクテリウム・デンティウムが最も効率的にGABAを産生することを明らかにしました(31)。GABA調節を介してアルツハイマー病症状の改善を目的としたビフィズス菌の応用に関する研究には限界があります。生体内実験では、ビフィズス菌の添加によって腸内GABA合成が促進され、マウスモデルにおける認知能力の向上につながる可能性があることが実証されています(123–126)。しかし、これらの効果の正確なメカニズムは未だ完全には解明されていません。作用する一連のプロセスと細胞・分子動態を明らかにするには、さらなる研究が必要です。 |
| 既存のデータベースや臨床サンプルを活用したアルツハイマー病治療用プロバイオティクスの特定と選択には、大きなハードルが存在します。ビフィズス菌によるアルツハイマー病の改善に関する研究をいくつか表2に示します。既存のデータベースや臨床サンプルコレクションは、規模や地理的多様性という点で制約を受けることが多く、研究成果の一般化可能性と信頼性に大きな影響を与えています(30)。これらの制約は、アルツハイマー病治療に有効なプロバイオティクスを選択するために、より広範で多様なデータセットの必要性を浮き彫りにしています。 |
| 表2.ビフィズス菌によるアルツハイマー病改善に関する部分的な知見(動物実験) |
 |
 |
 |
 |
 |
 |
 |
 |
 |
| 4. 限界 |
| しかしながら、腸内細菌叢の「再構築」は必ずしも完全かつ一貫したものではない。第一に、細菌叢の回復範囲には限界がある。多くの研究において、微生物組成に好ましい変化が見られるものの、全体的な多様性と構造は健康な野生型マウスで観察されるレベルまで完全には回復しないことがしばしば示されている(130, 131, 133)。アルツハイマー病の病態自体が細菌叢に及ぼす深刻な影響により、少数のプロバイオティクスを単純に補給するだけでは、これらの変化を完全に回復させることは困難である可能性がある(90)。第二に、菌株および宿主特異的な影響が大きい。異なるビフィズス菌株(例:B. ロンガム vs. B. ブレーベ)はそれぞれ異なる代謝特性と定着能力を有し、誘発される細菌叢の変化のパターンも異なる(133)。同様に、異なる遺伝的背景を持つ アルツハイマー病モデルマウスは、異なるベースラインのマイクロバイオームとプロバイオティクスへの反応を示すため (64、87、102、134)、研究結果の直接的な比較や外挿が複雑になります。 |
| 重要なエビデンスは、Hongwon Kimらによる研究から得られています (93)。この研究では、プロバイオティクス(B. ビフィダムBGN4およびB. ロンガム BORI)の若齢マウス(3ヶ月齢)と高齢マウス(16ヶ月齢)への影響を巧みに比較しました。その結果、プロバイオティクス介入は若齢マウスの糞便微生物叢の構成を著しく変化させたものの、高齢マウスへの影響は最小限であることが明らかになりました。しかし、この「無反応」微生物叢とは対照的に、プロバイオティクスは高齢マウスのDNA損傷とアポトーシスを同様に回復させ、加齢に伴う認知機能および記憶障害を改善しました。これは、ビフィズス菌の補給が認知機能の向上と神経炎症の抑制に一貫して肯定的な効果を示している一方で、腸内微生物叢を再構築するその能力は普遍的または均一とはほど遠いことを示しています。むしろ、それはモデル依存性と加齢に伴う変動性を示し、現在の研究における顕著かつ中心的な矛盾を構成しています (41、47、93)。 |
| もう一つの根本的な矛盾は、認知機能の改善と中核的な病理学的変化との乖離である。例えば、特定のビフィズス菌を摂取したアルツハイマー病マウスの水迷路試験の成績向上が研究で観察されている。しかし、一部の研究では、アミロイドβプラーク量やタウリン酸化レベルの同時減少は示されておらず(50、65、135)、特にヒトの脳からの対応するデータが欠如している。したがって、ビフィズス菌を介した認知機能の改善と中核的なアルツハイマー病病理学的産物との直接的な関連性を強く示すには、既存の証拠は依然として不十分である。より妥当なメカニズムとしては、神経炎症の緩和、シナプス可塑性の促進、神経伝達物質代謝の調節といった経路を介した認知機能の向上が挙げられる(41、42、47、66、128)。これは、微生物叢の回復による「下流効果」が予想以上に複雑であり、認知機能の改善は単一の病理学的マーカーの改善による必然的な結果ではなく、多因子相互作用の結果である可能性があることを示唆しています。 |
| さらに、このアプローチの長期的な有効性に対する重大な課題は、微生物の変化が一過性であることです。プロバイオティクスの補給を中止すると、マウスの腸内細菌叢は数週間以内に介入前の状態に戻ることがよくあります(136–138)。これは、生細菌の経口投与のみでは、持続的な微生物の定着と生態系の再構築を達成できない可能性があることを示しています。観察された改善は、「機能的調節」の一形態である可能性が高いです。プロバイオティクスは、腸内に一時的に存在する間、微生物叢の長期的な構造構成を根本的に変化させるのではなく、代謝物(短鎖脂肪酸など)または宿主の免疫系との相互作用を通じて有益な生理学的効果を発揮します(139–142)。これはまた、一部の研究で効果を持続させるために長期にわたる継続的な投与が必要である理由を説明しています。 |
| 5. 結論と今後の展望 |
| 本レビューでは、腸内ビフィズス菌とアルツハイマー病との関連性を示す最新のエビデンスを統合し、重要な複雑性と矛盾によって覆い隠されてきた有望な治療ポテンシャルを明らかにした(143)。ビフィズス菌サプリメントの摂取は認知機能に有益であることが研究で一貫して報告されている(51、55、129、135)。しかし、認知機能の改善とアルツハイマー病の中核病態との関連性、その効果が菌株および宿主特異的であること、そして微生物の変化が一過性であることなど、重要なギャップが依然として残っている。 |
| こうした相関関係の知見を原因療法へと転換するには、この分野の発展が不可欠です。今後の研究では、関連性を超えて直接的な因果関係を確立することを優先する必要があります。そのためには、特定の微生物群集を定着させた無菌アルツハイマー病マウスなどの革新的なモデルを用いて、ビフィズス菌とその主要代謝物(例えば、特定の短鎖脂肪酸、トリプトファン誘導体)が神経炎症とシナプス機能の調節において果たす役割を詳細に解明する必要があります(17、78、144)。同時に、重要でありながら十分に研究されていないパラメータにも体系的に取り組む必要があります。研究では、介入の最適なタイミング(発症前期と発症期)を決定し、複数菌株製剤と単一菌株製剤の相乗効果を評価し、宿主の食事や遺伝子との複雑な相互作用を解明する必要があります。最後に、トランスレーショナル・ギャップを埋めるためには、将来の臨床試験をより厳密な方法で設計する必要があります。そのためには、標準化された認知エンドポイント、堅牢なバイオマーカーパネル(神経イメージング、体液バイオマーカーなど)、そして高解像度のメタゲノムシーケンスを組み込むことが必要になります。これらのより洗練されたメカニズムに基づくアプローチを採用することで、アルツハイマー病に対する効果的で新規な治療法の開発に向けて、微生物叢-腸-脳軸を真に理解し、活用することが可能になります。+ |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、Front. Immunol., 03 February 2026に掲載されたRegulating the crosstalk between Bifidobacterium and the brain: a potential therapeutic strategy for Alzheimer's disease.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


