ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
不眠症: 腸内細菌叢との関連性、プロバイオティクスおよびポストバイオティクス療法の展望、 そして今後の方向性 |
Qiong Wu Guangqi Gao et al., |
|
|
| 要約 |
| 背景 |
| 腸内細菌叢は、宿主の遺伝的要因、食生活、ライフスタイルなど、複雑な相互作用によって影響を受けます。腸内細菌叢は代謝プロセスの調節において重要な役割を果たし、様々な疾患と関連しています。腸内細菌叢と脳の双方向的なコミュニケーションを担う腸-脳軸は、睡眠パターンの調節に重要な役割を果たし、睡眠障害の発症に大きく関与していることが、近年の研究で示唆されています。 |
| レビューの目的 |
| 本レビューは、不眠症のメカニズムと腸内細菌叢およびメタボロームとの関連性に関する最新の知見を包括的にまとめることを目的としています。プロバイオティクスとポストバイオティクスは、宿主の腸内細菌叢を調節し、不眠症を軽減する可能性を秘めた有益な微生物とその構成成分および代謝産物です。本レビューでは、不眠症管理におけるプロバイオティクスおよびポストバイオティクス介入試験の最近の進歩を概説し、この分野における既存研究の潜在的な利点と限界の両方を明らかにします。さらに、この分野における今後の研究方向性についても提言します。プロバイオティクスは、腸内細菌叢とその代謝産物を調節し、内分泌系、神経系、免疫系の反応に影響を与えることで、睡眠・覚醒行動を調節することができる。さらに、不眠症の改善におけるプロバイオティクスの役割を理解するためには、標準化された睡眠行動指標と睡眠モニタリング方法が必要である。 |
| 要約図解 |
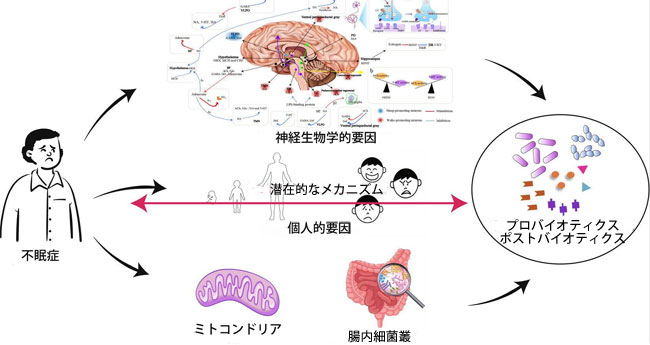 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.不眠症の原因となる要因 |
| 2.1.神経生物学的要因とその機能障害 |
| 2.2.睡眠調節因子の機能障害 |
| 2.3.睡眠促進因子 |
| 2.3.1.γ-アミノ酪酸は重要な抑制性神経伝達物質です |
| 2.3.2.メラトニンは、睡眠調節因子の中で最も初期に同定されたクラスです |
| 2.3.3.アデノシン |
| 2.3.4メラニン濃度ホルモンは調節性神経ペプチドです |
| 2.4.覚醒促進因子 |
| 2.4.1ノルアドレナリンはレム睡眠を評価する上で重要な指標です |
| 2.4.2.ヒスタミンは睡眠改善の重要な標的です |
| 2.4.3.アセチルコリンはコリン作動性神経伝達物質です |
| 2.4.4オレキシンAとオレキシンB |
| 2.5.その他の睡眠調節因子 |
| 2.5.1.セロトニンはモノアミン神経伝達物質です |
| 2.5.2ドーパミン |
| 2.5.3.脳由来神経栄養因子は、不眠症の臨床診断における潜在的なバイオマーカーとして提唱されている |
| 2.5.4.一酸化窒素 |
| 2.6.睡眠覚醒ニューロン間の相互作用の機能不全 |
| 2.7.コリン作動系およびアミン系の機能障害 |
| 2.8.松果体機能障害 |
| 2.9.視床下部-下垂体-副腎軸(HPA) |
| 2.10.個人的要因 |
| 2.11.ミトコンドリアと不眠症 |
| 2.12.不眠症における腸内細菌叢、腸内細菌叢由来代謝物、免疫因子およびその他の因子の変化 |
| 2.13.不眠症における腸内細菌叢の変化 |
| 2.14.不眠症における腸内細菌叢由来代謝物の変化 |
| 2.15.不眠症における免疫因子およびその他の因子の変化 |
| 2.16.不眠症に対するプロバイオティクスおよびポストバイオティクス介入 |
| 2.17.げっ歯類を用いた介入試験 |
| 3.ヒト介入試験 |
| 4.プロバイオティクスとポストバイオティクスによる睡眠調節の潜在的なメカニズム |
| 4.1.腸内細菌叢とメタボロームの再構築 |
| 4.2.腸管バリアと血液-脳関門の完全性を高めます |
| 5. 視床下部-下垂体-副腎軸を介した内分泌経路の調節 |
| 5.1.免疫調節 |
| 5.2.神経調節 |
| 6.結論 |
本文 |
| 1.はじめに |
| 精神疾患の診断・統計マニュアル第5版(DSM-5)によると、不眠症の診断には以下の特定の基準を満たす必要があります。(a)入眠困難、睡眠時間の延長、早朝覚醒など、睡眠時間または睡眠の質に対する不満があり、それに伴う症状がある。(b)睡眠障害により、臨床的に重大な苦痛が生じたり、社会的、職業的、教育的、学業的、行動的、またはその他の重要な機能領域に支障をきたしている。(c)不眠エピソードが週に少なくとも3晩発生し、最低3か月間持続する。(d)十分な睡眠機会があるにもかかわらず、睡眠障害が持続する。(e)不眠症は、他の睡眠覚醒障害のみに起因するものではなく、また、他の睡眠覚醒障害の経過中にのみ発生するものでもない(例:ナルコレプシー、呼吸関連睡眠障害、概日リズム睡眠覚醒障害、その他の医学的疾患による睡眠障害)。 (f) 睡眠障害は、物質の生理的影響(例:物質の使用、投薬)のみに起因するものではない。(g) 併存する精神障害や身体疾患の存在は、不眠症の訴えを完全に説明するものではない。現在、不眠症と日中の過度の眠気は世界中でますます蔓延しており、公衆衛生にとって大きな課題となっている。2011~2012年の健康調査で54,722人のヨーロッパの成人を対象に行われた横断研究では、睡眠障害の有病率が高いことが明らかになり、デンマークとイタリアでは16.6%、ポーランドでは31.2%に及んだ[1]。睡眠は、覚醒中に発生した神経細胞のDNA損傷を修復する上で重要な役割を果たしており[2]、効果的な治療戦略のためには、不眠症の特徴と根本的な原因を理解することが不可欠である。 |
| 不眠症は、遺伝、神経生物学、内分泌、免疫、心理社会的要因など、さまざまな要因に影響される複雑な疾患です[3]。最近の腸内細菌叢の研究により、うつ病、不安、不眠症などの神経学的問題の発症における腸内細菌叢の異常の役割が明らかになり[4]、健康と疾患における腸-脳軸の重要性が強調されています。その結果、腸内細菌叢の調節がこれらの症状を管理するための有望な手段として浮上してきました。プロバイオティクスとポストバイオティクスは、腸内微生物叢のバランスを整え、睡眠の質を改善する可能性のある治療法として注目を集めています。 |
| 本総説では、「プロバイオティクス」「ポストバイオティクス」「腸内細菌叢」「不眠症」というキーワードを用いて、PubMed、Web of Science、Google Scholarの各データベースを広範囲に検索しました。主な目的は、腸内細菌叢と不眠症の関連性を探ることでした。さらに、不眠症に対するプロバイオティクスおよびポストバイオティクス介入に関する関連する臨床試験および動物実験の結果を紹介し、今後の研究方向に関する知見と提案を提供します。 |
| 2.不眠症の原因となる要因 |
| 2.1.神経生物学的要因とその機能障害 |
| 睡眠・覚醒の調節に関わる神経経路の障害、神経伝達物質や受容体の機能異常、ホルモン作用の異常などが、不眠症の主なメカニズムです。睡眠・覚醒の移行に関わる様々な化学物質に関連する神経回路を包括的に理解することは、不眠症の治療戦略を発展させる上で極めて重要です。 |
| 2.2.睡眠調節因子の機能障害 |
| 脳には、主に神経伝達物質であるものの、ホルモンやサイトカインなど、数多くの睡眠調節因子(SRF)が存在します(表1参照)。これらの因子の中には、γ-アミノ酪酸(GABA)、ガラニン(Gal)、アデノシン、メラニン濃度ホルモン(MCH)、メラトニン(Mel)など、睡眠を促進するものがあります。逆に、ヒスタミン(HA)、アセチルコリン(ACh)、オレキシン(ORX)、ノルアドレナリン(NA)など、覚醒を促進する因子も存在します。さらに、5-ヒドロキシトリプタミン(5-HT:セロトニン)、ドーパミン(DA)、脳由来神経栄養因子(BDNF)などの因子も睡眠調節に関与しています。睡眠調節因子とその受容体のメカニズムと機能を理解することは、睡眠・覚醒サイクルにおけるこれらの因子の生理的役割を理解するための基礎となります(表1参照)。 |
| 表1.睡眠調節因子、受容体、主要な情報源、および研究結果 |
 |
 |
 |
 |
 |
 |
 |
| 注:睡眠調節因子は主に睡眠関連の神経伝達物質やホルモンを含みます。受容体とは睡眠調節因子の受容体を意味します。一次発生源とは睡眠調節因子によって生成および放出される特定の脳領域です。 |
| 2.3.睡眠促進因子 |
| 2.3.1.γ-アミノ酪酸(GABA)は重要な抑制性神経伝達物質です |
| 表1にまとめられた研究は、γ-アミノ酪酸(GABA)が睡眠を促進する役割について洞察を与えており、γ-アミノ酪酸抑制性神経伝達物質の分泌、放出、および受容体結合の欠陥が、異常な覚醒、不安、および不眠症と関連していることを示唆しています。特に、腹外側視索前核(VLPO)のγ-アミノ酪酸ニューロンの約80%は、ガラニン1R、ガラニン2R、およびガラニン3Rを含むガラニン(Gal)およびガラニン受容体を共発現しています[5,6]。ガラニン-ガラニン受容体システムは、睡眠覚醒パターンの調節において重要な役割を果たしています。具体的には、ガラニン1は、結節乳頭体核(TMN)における徐波睡眠を促進する一方で、ヒスタミン(HA)ニューロンの活動によって引き起こされる覚醒を抑制します。さらに、下流のガラニン-γ-アミノ酪酸ニューロンは、結節乳頭体核のヒスタミンニューロン、青斑核(LC)のノルアドレナリンニューロン、および背側縫線核(DR)のセロトニン(5-HT)作動性ニューロンに投射し、睡眠調節に影響を与えている。 |
| 2.3.2.メラトニンは、睡眠調節因子の中で最も初期に同定されたクラスです |
| メラトニン(Mel)は明確な概日リズムを示し、メラトニン受容体1およびメラトニン受容体2を介して様々な生理機能を媒介します(表1)。睡眠不足(SD)が腸管バリア機能障害に及ぼす影響は、単なる睡眠不足ではなく、メラトニンlの阻害に起因する可能性があることが示されています[7]。さらに、先行研究では、培養したノルアドレナリンニューロンが松果体 (PG)を刺激してメラトニン合成を開始させるものの、その産生はTNF-αによって一時的に阻害されることが示されました[8]。これは、炎症性サイトカインが松果体の機能に関与していることを示唆しており、不眠症と炎症反応との重要な関連性を強調しています。 |
| 2.3.3.アデノシン |
| 複数の研究により、細胞外アデノシン濃度の上昇が総睡眠時間と徐波活動の増強に重要な役割を果たしていることが示されています[9,10]。覚醒時間が長くなるにつれて脳内のアデノシン濃度は徐々に上昇し、睡眠中は著しく低下します。これは、代謝産物の平衡が睡眠を調節するという理論と一致しています。アデノシンがアデノシン1受容体に結合するとオレキシン(ORX)およびヒスタミンニューロンの活動が抑制され、アデノシン2受容体に結合するとプロスタグランジンD2の作用が抑制されます。これらの作用はいずれも睡眠調節に寄与しています[11,12]。要約すると、アデノシンの産生と代謝に関わる酵素と受容体が共同でアデノシン濃度の安定性を調節し、アデノシンシグナルシステムを形成して体内の生理的恒常性を維持しています。 |
| 2.3.4メラニン濃度ホルモンは調節性神経ペプチドです |
| メラニン濃度ホルモン(MCH)は主に視床下部の後外側部および内側部のニューロンに存在します。広範な研究により、メラニン濃度ホルモンは睡眠、特にレム睡眠の生成と維持に重要な役割を果たしていることが確認されています。げっ歯類では、メラニン濃度ホルモンの作用は特定の受容体であるメラニン濃度ホルモンR1を介して発揮されます。メラニン濃度ホルモンR1は、睡眠や気分を含む恒常性行動の重要な調節因子です。メラニン濃度ホルモンはオレキシンとドーパミン(DA)に対して特異的な抑制効果を示します。メラニン濃度ホルモンによるオレキシンおよびドーパミンニューロンの出力調節は、睡眠の質の向上に寄与します(表1)。 |
| 2.4.覚醒促進因子 |
| 2.4.1ノルアドレナリンはレム睡眠を評価する上で重要な指標です |
| 睡眠不足マウスでは血漿ノルアドレナリン(NA)濃度が有意に上昇し、メラトニン(Mel)濃度の低下と相関することが観察されている[7]。一方、覚醒時間の延長に伴うエネルギー代謝亢進は酸化ストレスを引き起こし、青斑核(LC)領域のノルアドレナリンニューロン数を30~37%有意に減少させる[13,14]。これらの情報と表1に示されたデータを組み合わせると、ノルアドレナリンはレム睡眠を評価する上で重要な指標であり、腹外側視床下部(VLPO)は覚醒反応を媒介する青斑核ノルアドレナリンニューロンの重要なシナプス後標的として機能すると考えられる。さらに、多くの研究で、神経活動がノルアドレナリンβ2受容体シグナル伝達経路を介してミクログリアの動態を制御することが示されており、睡眠覚醒サイクル中のミクログリアの動的な変化と睡眠関連シナプスリモデリングにおけるミクログリアの役割が強調されている[15,16]。 |
| 2.4.2.ヒスタミンは睡眠改善の重要な標的です |
| 結節乳頭体核(TMN)のヒスタミン(HA)ニューロンの約80%は覚醒時にc-Fosを発現し[17]、H1R、H2R、H3R受容体への結合を介して覚醒作用を発揮する。ヒスタミンニューロンは、他の睡眠調節系(アセチルコリン、グルタミン酸、ノルアドレナリン、セロトニン)の活性にも影響を与えることが知られている。これまでの研究では、リモシラクトバチルス・ロイテリの投与により、腸内でL-ヒスチジンがヒスタミンに変換され、H2Rシグナル伝達経路を介してcAMPレベルが上昇し、下流のMEK/ERK MAPK(訳者注:MEK/ERK(MAPK)経路は、細胞の増殖、分化、生存、および死を制御する細胞内シグナル伝達の主要なルートの一つです。細胞表面の受容体が受け取った情報を、一連のタンパク質のリン酸化(スイッチのオン・オフ)を通じて核内のDNAまで伝え、遺伝子の働きを調節します) シグナル伝達が阻害され、大腸の炎症が抑制されることが示されている[18,19]。しかし、プロバイオティクスが同様のメカニズムで睡眠を改善できるかどうかは、まだ明らかになっていない。 |
| 2.4.3.アセチルコリンはコリン作動性神経伝達物質です |
| アセチルコリン(ACh)は主に視床、線条体、前脳基底部(BF)などの領域に神経伝達物質を伝達することで機能します。その神経線維束と上行投射は上行性網様体賦活系を形成し[20]、ノンレム睡眠とレム睡眠の両方に影響を与えることで睡眠の質に影響を及ぼします(表1)。コリン作動性ニューロンは、アセチルコリン受容体に結合することで重要な調節的役割を果たします。シナプス前ムスカリン性アセチルコリン受容体は、γ-アミノ酪酸、グルタミン酸、アセチルコリンなど、様々な神経伝達物質の放出を調節します。さらに、ムスカリン性アセチルコリン1受容体(ACh1R)は、腹外側視床下部外側野(VLPO)ニューロンにおけるγ-アミノ酪酸作動性伝達に影響を与えます[21]。 |
| 2.4.4オレキシンAとオレキシンB |
| オレキシンAとオレキシンB(ヒポクレチン1とヒポクレチン2とも呼ばれる)は、視床下部外側部と後部にある神経細胞から分泌される神経伝達物質で、覚醒を促進する働きがある[22]。マウスでは、1日12時間の睡眠不足を7日間連続で行うと、視床下部外側部におけるオレキシン含有神経細胞の数が24%減少することが分かっている[23]。したがって、このオレキシン神経細胞の減少は、睡眠を促進するための身体の代償機構であると考えられる。また、オレキシン系はノルアドレナリン、ドーパミン、セロトニン(5-HT)、ヒスタミン、アセチルコリンの神経細胞を直接支配し、興奮させることで覚醒を促進することも研究で確認されている(表1)。 |
| 2.5.その他の睡眠調節因子 |
| 2.5.1.セロトニンはモノアミン神経伝達物質です |
| セロトニン(5-ヒドロキシトリプタミン)は、トリプトファンヒドロキシラーゼ(末梢TPH1および中枢神経系TPH2)の作用によりトリプトファンから合成されます。これまでの研究では、プロバイオティクスがトリプトファン代謝を調節することでセロトニンレベルを調節し、腸内細菌叢と睡眠調節システム間のコミュニケーションに影響を与える可能性があることが示されています[24]、[25]、[26]。興味深いことに、セロトニン(5-HT)は覚醒作用と催眠作用の両方を持っています(表1)。脳のさまざまな領域に存在するセロトニン受容体の異なるサブタイプは、それぞれ異なる薬理作用を持つことに注意することが重要です。したがって、関連するメカニズムを理解するためには、異なる受容体サブタイプの発現を調査することが不可欠です。4-クロロ-DL-フェニルアラニン(PCPA)は、セロトニン合成の95%以上を効果的に阻害することができます。したがって、4-クロロ-DL-フェニルアラニンの腹腔内注射は、セロトニン系の障害に関連する不眠症の改善に対する介入の効果を評価するための不眠症動物モデルを構築するためによく用いられます。さらに、セロトニンはメラトニン産生に影響を与えることで睡眠に影響を与える可能性があります。要約すると、現在の研究では、セロトニンは睡眠覚醒行動の調節とレム睡眠の抑制において重要な役割を担っていることが示唆されています。 |
| 2.5.2ドーパミン |
| 脳内におけるドーパミン(DA)の主要な供給源は、腹側被蓋野と黒質緻密部です。ドーパミンは様々な下流受容体を介して覚醒と睡眠の相互作用を調節するため、ドーパミン濃度とそれに対応する受容体の安定性を維持することは、睡眠覚醒システムの適切な機能にとって不可欠です(表1)。 |
| 2.5.3.脳由来神経栄養因子は、不眠症の臨床診断における潜在的なバイオマーカーとして提唱されている |
| 脳由来神経栄養因子(BDNF)は、大脳皮質、嗅球、基底前脳、中脳、視床下部など、脳の様々な部位で発現している。脳由来神経栄養因子の特異的受容体はTrkB(訳者注:TrkB(トロポミオシン関連キナーゼB)は、脳由来神経栄養因子(BDNF)の高親和性受容体であり、神経細胞の生存、分化、シナプス可塑性、および学習・記憶において中心的な役割を果たす受容体チロシンキナーゼです)である[27]。TrkBの活性化は、ホスホリパーゼCγ、細胞外シグナル調節キナーゼ(ERK)、プロテインキナーゼB経路など、複数のシグナル伝達カスケードを活性化し、神経シナプス形成と神経新生を促進することで、脳全体の可塑性を高める[28]。過去10年間に行われた数多くの研究により、睡眠構造障害や不眠症患者における脳由来神経栄養因子の重要な役割が明らかにされてきた。その結果、脳由来神経栄養因子は不眠症の臨床診断における潜在的なバイオマーカーとして提唱された[29]。さらに、脳由来神経栄養因子の機能と調節は、エストロゲン受容体βによっても影響を受ける。表1は、哺乳類およびヒトの睡眠におけるTrkBと脳由来神経栄養因子の役割に関する現在の証拠をまとめたものであり、脳由来神経栄養因子受容体、睡眠異常、および精神疾患との関連性を確立するものである。 |
| 2.5.4.一酸化窒素 |
| 一酸化窒素(NO)は、一酸化窒素合成酵素によるアルギニンの触媒作用によって生成される、非常に親油性の高いガスです。睡眠・覚醒過程において、一酸化窒素はタンパク質中の特定のアミノ酸残基の翻訳後修飾、すなわちシステインのS-ニトロシル化によって作用を発揮します。この修飾は、アデノシン、背側縫線核(DR)、セロトニンニューロン、オレキシンニューロンなどの覚醒促進ニューロンの活動を抑制します。一方、Dzoljicらによる研究では、一酸化窒素合成酵素阻害剤がラットの睡眠を増加させ、覚醒を減少させるという矛盾する結果が報告されています[30]。したがって、睡眠調節における一酸化窒素の役割を完全に理解するためには、さらなる研究が必要です。 |
| 睡眠調節と神経薬理学に関する最新の研究から得られた証拠は、睡眠調節システムが不眠症治療の標的として有望であることを強く示唆している。これらのシステムは単独で機能するのではなく、覚醒と睡眠の切り替えを促進するために、様々な脳核やニューロンを調節することによって効果を発揮することに留意する必要がある。 |
| 2.6.睡眠覚醒ニューロン間の相互作用の機能不全 |
| 正常な睡眠覚醒調節における重要なメカニズムは、腹外側視索前核と、青斑核、結節乳頭体核、背側縫線核のニューロンを含むモノアミン作動性細胞集団との間の相互抑制である(図1)。、腹外側視索前核は睡眠促進中枢として機能し、青斑核、結節乳頭体核、背側縫線核は覚醒促進に関与する。γ-アミノ酪酸作動性伝達は、視床下部および脳幹内の覚醒促進中枢を積極的に抑制し、その活動を効果的に低下させる。さらに、腹外側視索前核から結節乳頭体核に投射するγ-アミノ酪酸受容体は睡眠促進に寄与する。同時に、γ-アミノ酪酸作動性ニューロンはガラニンを共発現し、その細胞体と樹状突起は結節乳頭体核に伸びてシナプス結合を形成する。これらのγ-アミノ酪酸/ガラニンニューロンは、青斑核のノルアドレナリンニューロンおよび背側縫線核のセロトニン(5-HT)ニューロンにも投射し、睡眠をさらに促進する。アデノシンは、オレキシンニューロンやヒスタミンニューロンなどの覚醒促進ニューロンの活動を抑制する。したがって、前脳基底部はγ-アミノ酪酸とアデノシンを利用して、覚醒促進領域への抑制作用を強化している。 |
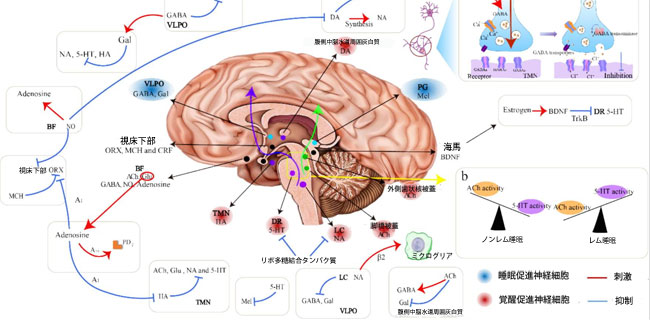 |
図1. 睡眠調節因子と睡眠覚醒調節のメカニズム。 この図は、さまざまな睡眠調節因子が放出される脳領域と、異なる調節因子間の接続を示しています。2種類の睡眠調節ニューロンが示されています。睡眠促進ニューロン(青い円で示されています)と覚醒促進ニューロン(赤い円で示されています)。睡眠促進中枢は、主に腹外側視索前核(VLPO)でのγ-アミノ酪酸とガラニンの放出によって皮質活動を抑制します。さらに、脳の松果体から放出されるメラトニン(Mel)は睡眠促進効果を発揮します。2つの覚醒促進経路(それぞれ紫と緑の矢印で示されています)があり、経路に関与するニューロンと脳領域は紫と緑の点で示されています。その他の睡眠調節因子(黒い円で示されています)は、睡眠覚醒システムの調節に影響を与えます。 (a)γ-アミノ酪酸を例として、シナプスでの神経伝達物質伝達の活性化プロセスが示されています。 γ-アミノ酪酸は、小胞抑制性アミノ酸トランスポーターを介して小胞内に合成、貯蔵、輸送され、神経伝達中に先行ニューロンのシナプス前膜からシナプス間隙に運ばれ、そこでシナプス後ニューロン上の対応する受容体(GABAARおよびGABACR)に結合してイオンチャネルを開き、Cl-が細胞内に流入することで、活動電位の発生の可能性を低下させ、次のニューロンの活動を抑制します。GABABR代謝型受容体は、Gタンパク質活性化を介してK+またはCa2+チャネルを開き、細胞から正電荷イオンを除去するか、細胞膜を過分極させて神経抑制を引き起こし、睡眠を促進します。γ-アミノ酪酸は、γ-アミノ酪酸トランスポーターによってシナプス間隙からシナプス前膜ニューロンに輸送されて再利用されるほか、γ-アミノ酪酸トランスアミナーゼによって不活性化されることもあります。 (b)脳幹領域におけるアセチルコリン系とセロトニン系のバランスが、ノンレム睡眠とレム睡眠を調節します。 略語: 睡眠調節因子: 5-HT、セロトニン(5-ヒドロキシトリプタミン); Ach、アセチルコリン; BDNF、脳由来神経栄養因子; DA、ドーパミン; GABA、γ-アミノ酪酸; Gal、ガラニン; HA、ヒスタミン; Mel、メラトニン; MCH、メラニン濃度ホルモン; NO、一酸化窒素; NA、ノルアドレナリン; ORX、オレキシン。脳の位置 (図中の太字): BF、前脳基底部; DR、背側縫線核; LC、青斑核; TMN、結節乳頭体核; VLPO、腹外側視索前核。受容体: β2、ノルアドレナリンβ2受容体; GABA受容体 (GABAA、GABAB、GABACを含む) TrkB:チロシンキナーゼ受容体B。NREM:ノンレム睡眠、REM:急速眼球運動睡眠。 |
| 覚醒に寄与する上行性網様体賦活系には主に2つの構成要素がある(図1)。1)青斑核(LC)のノルアドレナリンニューロン、背側縫線核(DR)のセロトニンニューロン、結節乳頭体核のヒスタミンニューロン、および腹側中脳水道周囲灰白質のドーパミンニューロンが関与する。結節乳頭体核のヒスタミンニューロンは青斑核のノルアドレナリンニューロンおよび背側縫線核のセロトニンニューロンとシナプス結合を形成し、大脳皮質の活動を開始して覚醒を促進する。青斑核のノルアドレナリンニューロンは視床下部視索前野および腹外側視索前野の睡眠関連ニューロンを直接抑制し、覚醒をさらに促進する。さらに、オレキシン-A/Bおよびメラニン濃度ホルモン含有外側視床下部ニューロンとアセチルコリン含有基底前脳(BF)ニューロンが脳幹の覚醒経路に寄与する。これらのニューロンは基底前脳および皮質領域のコリン作動性ニューロンの活性化を増強し、覚醒を促進する。 2) 脚橋被蓋および外側背側被蓋に位置するコリン作動性ニューロンが関与する。これらのニューロンは、視床中継ニューロンを活性化することで皮質活動を開始する。さらに、ノルアドレナリンやセロトニンなどのモノアミン系ニューロンからの求心性信号は、腹外側視索前核ニューロンを直接抑制する。睡眠促進および覚醒促進の脳領域は相互作用して神経活動を調節し、明確な概日リズムと正常な睡眠・覚醒状態をもたらす。しかし、これらのシステムのいずれかに同時に障害や機能不全が生じると、不眠症につながる可能性がある。 |
| 2.7.コリン作動系およびアミン系の機能障害 |
| ネコを用いた実験では、脳幹のコリン作動系(アセチルコリン:ACh)とアミン系(セロトニン:5-HT)を操作することで睡眠構造が変化することが明らかになった[113]。これら2つの系は、ノンレム睡眠とレム睡眠のサイクルを決定する上で重要な役割を果たしている(図1b)。正常な睡眠では、アミン系はノンレム睡眠中に活性化し、レム睡眠の開始時に不活性化する[114]。さらに、正常な睡眠をとる被験者を対象としたコリン作動性/抗コリン作動性刺激実験により、ノンレム睡眠とレム睡眠の相互作用モデルに関する仮説が検証され、コリン作動性刺激が動物とヒトの両方においてレム睡眠エピソードの発生を促進する可能性が示唆されている。 |
| 2.8.松果体機能障害 |
| 松果体(PG)は頭蓋窩後部に位置し、メラトニン(Mel)の合成と放出の場として機能します(図2a)。先行研究では、松果体切除術によって多くの季節性反応が消失することが示されています[114]。コーヒーの長期摂取は松果体実質の減少と関連しており、後の人生における睡眠の質に影響を与える可能性があります[115]。また、松果体容積の減少はレム睡眠行動障害と関連している可能性があります[116]。松果体実質容積、夜間総睡眠時間、睡眠の質指数、およびメラトニン濃度との関係をさらに調査するため、線維筋痛症の女性30名を対象に頭部MRI検査を実施しました。その結果、松果体容積と総睡眠時間、および夜間メラトニン濃度との間に有意な相関関係が認められました[117]。したがって、松果体容積の減少または変化は、様々な睡眠関連の問題を引き起こす可能性があります。最近の研究では、心臓病患者の睡眠障害は炎症性マクロファージの動員、上頸神経節の線維化によるものであり、その結果、松果体(の神経支配が変性し、メラトニン放出が減少することが観察されている[118]。しかし、別の研究では、松果体切除後もPSGでモニタリングされた睡眠に変化は見られなかったと報告されている[119]。これらの報告は、松果体(が睡眠に及ぼす影響をめぐる既存の論争を浮き彫りにしている。 |
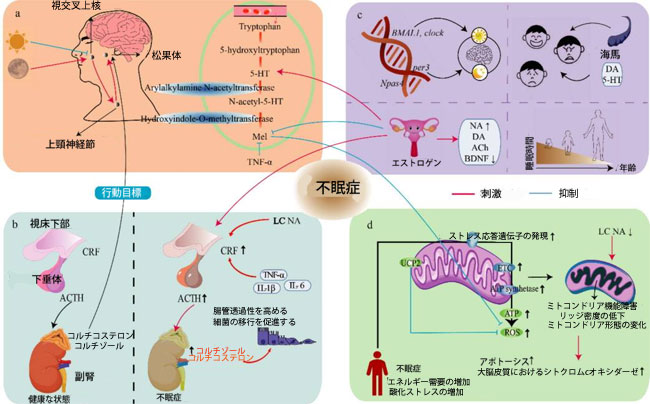 |
図2. その他の睡眠調節メカニズム。 (a) 松果体 (PG) 領域は通常、光信号に応じて メラトニン合成を調節します。松果体の損傷は メラトニンと セロトニン(5-HT) のレベルとそれらの代謝を阻害する可能性があります。暗闇では、視交叉上核神経細胞の軸索が視床下部室傍核に作用する信号を放出します。室傍核細胞は信号を上頸神経節に伝達し、上頸神経節は信号を松果体細胞に伝達します。さらに、松果体 での メラトニン産生は TNF-α によって一時的に阻害され、松果体はコルチコステロン作用の標的にもなります。 (b) 視床下部-下垂体-副腎 (HPA) 軸は主要なストレス応答システムです。不眠症は、視床下部-下垂体-副腎軸のコルチゾール/コルチコステロンレベルの上昇につながる可能性があり、これは青斑核ニューロンのノルアドレナリンおよびいくつかの炎症促進因子(TNF-α、IL-1β、IL-6を含む)と関連している可能性があり、腸管バリア機能に影響を与えます。 (c) 不眠症は個人差があります。遺伝的要因には、概日リズムを調節する時計遺伝子、特定の睡眠調節因子を調節する遺伝子、および視床下部-下垂体-副腎(HPA)軸に影響を与え、ドーパミン、メラトニン、ノルアドレナリン、脳由来神経栄養因子、セロトニンなどを調節する性別関連のエストロゲンが含まれます。さらに、年齢と気分は睡眠パターンに重要な役割を果たし、主にドーパミンとセロトニンに関連しています。個人が年をとると、身体の生理機能が徐々に低下し、松果体は萎縮して最終的に石灰化を起こし、生物時計のリズムが弱まったり消失したりする可能性があります。 (d) ミトコンドリアは、電子伝達とプロトン勾配形成を伴う酸化的リン酸化によって細胞にエネルギーを供給します。電子伝達は、電子伝達鎖と 4 つの ATP 合成酵素複合体の間で行われます。不眠症はしばしば活性酸素種の蓄積、ストレス応答遺伝子 (抗酸化遺伝子 (SOD1、GSTS1、GSTO1、カタラーゼ) およびミトコンドリアストレス遺伝子を含む) の発現の上昇、エネルギーバランスの崩壊、および過剰な酸化ストレスの蓄積を引き起こし、ミトコンドリア機能を損ない、ミトコンドリアの形態を変化させる可能性があります。しかし、これらの変化が不眠症に直接寄与するかどうかはまだ明らかにされていません。さらに、青斑核ニューロンにおける ノルアドレナリンのダウンレギュレーションはミトコンドリア損傷を引き起こします。 略語: 5-HT、5-ヒドロキシトリプタミン(セロトニン); Ach、アセチルコリン; ACTH、副腎皮質刺激ホルモン; BDNF、脳由来神経栄養因子; CRF、副腎皮質刺激ホルモン放出因子;DA、ドーパミン;ETC、電子伝達系;IL、インターロイキン;LC、青斑核;Mel、メラトニン;NA、ノルアドレナリン;ROS、活性酸素種;TNF、腫瘍壊死因子;UCP2、ミトコンドリア脱共役タンパク質2。 |
| 2.9.視床下部-下垂体-副腎軸の過剰反応 |
| 視床下部-下垂体-副腎(HPA)軸はストレス反応の調節に関わる主要な内分泌経路であり、コルチゾールとコルチコステロンはその最終産物です(図2b)。動物実験では、睡眠障害マウス(SDマウス)において唾液コルチコステロン濃度の上昇が認められています[120]。同様に、健常者においても睡眠障害は視床下部-下垂体-副腎軸の反応性を高めることが分かっています[120]。さらに、不眠症患者では視床下部-下垂体-副腎軸の活動が亢進し、過剰な覚醒状態を示すという見解を支持する証拠が蓄積されています[121]。その結果、視床下部-下垂体-副腎軸の過剰活性化によるコルチゾールの過剰産生は、覚醒を刺激し、概日リズムを乱し、不眠症の症状を悪化させる可能性があります。前述のように、男性被験者では睡眠の質の低下がコルチゾールストレス反応の有意な増加と関連していましたが、女性被験者ではこの効果は観察されませんでした。したがって、視床下部-下垂体-副腎軸反応の影響は性別によって異なるようです[122]。これは、エストロゲンと視床下部-下垂体-副腎軸の相互作用によるものと考えられます(詳細は後述)。 |
| 広範な証拠は、コルチゾールと免疫細胞との相互作用、およびサイトカイン放出に対するコルチゾールの制御を支持しています。炎症性サイトカインのレベルが上昇すると、副腎皮質刺激ホルモン放出因子の分泌が刺激され、その結果、副腎から大量のコルチゾールが放出されて炎症が抑制されます。さらに、視床下部-下垂体-副腎軸と炎症反応の亢進は、腸管バリアの完全性を破壊し、腸管透過性を増加させ、細菌の移行と免疫細胞の浸潤を促進し、「リーキー腸」を引き起こします。毒性代謝物が血流に漏れ出すと、視床下部-下垂体-副腎軸の活性化に寄与し、コルチゾール産生の増加につながります[123]。 |
| 2.10個人的要因 |
| 研究により、不眠症には遺伝的要因が強く影響することが一貫して示されています。動物およびヒトにおける候補遺伝子研究では、不眠症の表現型と概日時計遺伝子(図2c)との関連性が特定されており、BMAL1/mop3 [124]、per [125]、clock [126]、Npas4 [127]などが含まれます。さらに、セロトニンランスポーター遺伝子の5'調節領域における44塩基対の挿入/欠失多型は、原発性不眠症と関連しています [128]。加齢に伴い、身体の生理機能は徐々に低下し、加齢に伴う脳の神経細胞の減少または喪失が起こります [52]。同時に、睡眠障害には性差も見られ、入眠困難や睡眠維持困難は女性に多く見られます。不眠症における男女差の考えられる説明の一つは、エストロゲンの影響である。エストロゲンは視床下部-下垂体-副腎軸の活動を高め、セロトニンレべルを上昇させ、ドーパミン、メラトニン、エンドルフィン、セロトニンなどの神経伝達物質を調節する[34,96,129]。注目すべきは、セロトニン(5-HT)やドーパミンなどの神経伝達物質は腸で産生され、脳で産生される量よりも多く、より速いペースで産生されるということである[130]。腸の神経細胞によって産生されるこれらの神経伝達物質は、精神的な健康を改善し、幸福感を高め、さらには記憶力を向上させる可能性を秘めている。 |
| 前述のシグナル伝達経路と調節システムは、不眠症の媒介に大きく寄与している。しかし、不眠症は様々な複雑な生理学的プロセスが関与する多面的な疾患であることに留意する必要がある。これには、様々な睡眠調節因子(SRF)レベルの乱れ、外傷性脳損傷による脳機能障害、睡眠恒常性に関わる神経細胞集団に対する特定の調節因子の影響などが含まれ、また、様々な個人的特性も不眠症に影響を与える可能性のある要因として認識されつつある。 |
| 2.11.ミトコンドリアと不眠症 |
| ミトコンドリアは、酸化的リン酸化によって細胞の主要なエネルギー源であるATPを合成する役割を担っています。ATP供給のわずかな中断でさえ、シナプス活動に大きな影響を与える可能性があります。ラットを用いた研究では、睡眠状態と比較して、覚醒後3時間経過した時点で大脳皮質ミトコンドリアにおけるシトクロムcオキシダーゼサブユニットI、NADHデヒドロゲナーゼサブユニット2、および12S rRNAのmRNA発現レベルが上昇していることが観察されました。また、夜勤労働者の動態や律速段階となるミトコンドリア酵素の発現は概日リズムを示し、覚醒時にミトコンドリア活性が亢進していることが示唆されています[131,132]。覚醒時にはエネルギー消費が増加するため、身体のエネルギー需要を満たすためにミトコンドリアによるATP産生が必要となります。このプロセスには、電子伝達系とATP合成酵素複合体を介した電子伝達とミトコンドリア内膜を横切るプロトン勾配の形成が含まれます。電子伝達系からの電子漏出は、活性酸素種とフリーラジカルを生成する可能性があります。睡眠中、脳は覚醒中に蓄積された活性酸素種を利用し、抗酸化物質であるメラトニンは活性酸素種の抑制に役立ちます。さらに、ミトコンドリア内膜に存在するミトコンドリア脱共役タンパク質2は、睡眠不足時の過剰な活性酸素種の産生に対する緩衝材として機能し、正常なミトコンドリア機能を確保します[133]。睡眠不足が始まると、活性酸素種の蓄積が増加し、酸化ストレスが増大し、それに続いてミトコンドリア機能不全が起こり、アポトーシスにつながります(図2d)。これは、適切な細胞機能と全体的な健康のために、バランスの取れたミトコンドリア機能を維持し、酸化ストレスを最小限に抑えることの重要性を強調しています。 |
| 興味深いことに、睡眠不足はミトコンドリアの形態に影響を与えることがわかっています。マウスでは、4時間の睡眠不足の後、前頭皮質の脊髄密度の低下が観察されました。これに伴い、ミトコンドリア外膜の伸長と膜間腔の拡大が起こり、空胞形成につながりました[134,135]。ただし、一定期間内に睡眠が回復すれば、正常な機能形態が回復できることに注意することが重要です。現在、不眠症がミトコンドリアの機能と形態に影響を与える可能性があることを示唆する説得力のある証拠があります。しかし、ミトコンドリア形態の障害が直接不眠症を引き起こすかどうかを確認する決定的な研究は不足しています。 |
| 要約すると、睡眠を調節する要因は複雑かつ多様であり、複数の要因が個別に、あるいは複合的に睡眠を調節しています。したがって、不眠症を調節する手段としてプロバイオティクスを使用する場合、通常は不眠症の原因をより詳細に理解し、特定の経路を特定することによってプロバイオティクスの調節メカニズムを実証する必要があります。 |
| 2.12.不眠症における腸内細菌叢、腸内細菌叢由来代謝物、免疫因子およびその他の因子の変化 |
| 近年の研究により、不眠症と腸内細菌叢、腸内細菌叢由来代謝物、および免疫因子との複雑な相互作用が明らかになってきました(図3)。本節では、不眠症とこれらの相互に関連する要素との多面的な関係を探ります。続く各節では、不眠症患者における腸内細菌叢とその代謝物の変化、および不眠症の発症と進行における免疫因子の影響について詳しく解説します。これらの複雑な相互作用を解明することで、不眠症の根本的なメカニズムと潜在的な治療法についてより深い理解が得られるでしょう。 |
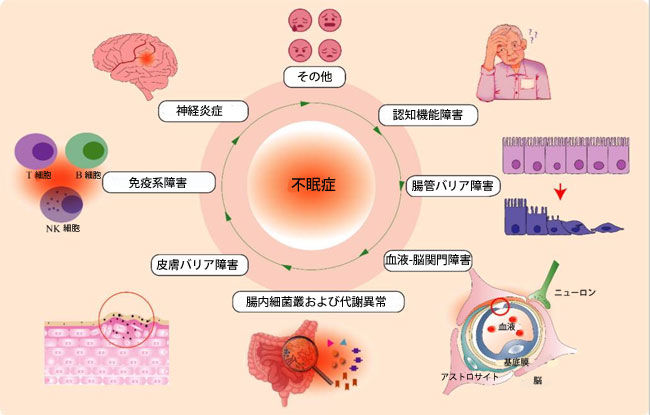 |
図3. 不眠症が身体機能に及ぼす悪影響。 不眠症は、脳機能(神経炎症)、消化器機能(腸内細菌叢および代謝異常)、皮膚バリア機能、免疫系など、さまざまな身体機能に悪影響を及ぼします。同時に、不眠症は不安や抑うつなどの精神的な問題の主要な原因の一つでもあります。これらの悪影響は相互に関連しており、互いに影響し合います。 |
| 2.13.不眠症における腸内細菌叢の変化 |
| 慢性睡眠不足は、炎症の増加、代謝障害、神経学的および精神医学的疾患など、さまざまな健康問題と一貫して関連付けられてきました。特に、これらの有害な結果は、腸内細菌叢の構成の変化と関連していることが明らかになっています(図3)[136]、[137]、[138]。腸内細菌叢は、消化管に生息する複雑な微生物群集であり、腸内恒常性とバリア機能の維持に極めて重要な役割を果たしています。新たな証拠は、不眠症がこの繊細なバランスを崩し、腸内細菌叢の異常を引き起こすことを示唆しています。 |
| ヒトとげっ歯類モデルの両方で実施された13件の観察研究では、不眠症のない人と不眠症のある人の間で腸内細菌叢の構成に有意な変化があるという説得力のある証拠が得られています(表2)。門レベルでは、ラクトバチルス属やストレプトコッカス属などの属を含むファーミクテスとバクテロイデスが、これらの研究で一貫して異なる存在量の細菌分類群として同定されており、不眠症関連のディスバイオシスに関与している可能性が示唆されています。ファーミクテス[139,140]、バクテロイデス [139,141](2件の研究)、テネリクテス [142](1件の研究)の存在量は、不眠症の人とモデルマウスで減少していることがわかりました。対照的に、プロテオバクテリア [143]の存在量は増加しています。注目すべきことに、前向き観察研究では、乳がん手術後に睡眠の質が低下した女性でファーミクテスが増加する傾向が観察されました[141]。これらの矛盾する結果には、さらなる検証が必要である。さらに、腸内微生物門であるベルコミクロビアとレンズファエラの割合が高いほど、睡眠の質が良いことと関連付けられている[144]。 |
| 表2.不眠症に関連する糞便微生物叢、代謝産物、および血液指標の変化 |
 |
 |
 |
注:記号「↑」と「↓」は、それぞれ物質または種のレベルの上昇と下降を表します。 略語:FMTは糞便微生物移植、ILはインターロイキン、IFNはインターフェロン、LPSはリポ多糖、SDは睡眠不足、SCFAは短鎖脂肪酸、TNFは腫瘍壊死因子を意味します。 |
| 家族レベルでは、健康なヒトまたは動物被験者と不眠症患者の間で、いくつかの細菌科の存在量に有意な差が観察された。具体的には、ラクノスピラ科 [139,145] (2つの研究)、コリネバクテリウム科、およびエリシペロトリカ科 [142] (1つの研究) は、不眠症患者または動物モデルで存在量が増加した。逆に、ラクトバチルス科[145] (1つの研究) は存在量が減少した。腸の健康維持に役割を果たすことで知られるクロストリジウム綱目に属する一般的な科であるルミノコッカス科[146] は、2つの臨床研究で有意に減少していることがわかった。したがって、不眠症患者では腸の健康が損なわれていると考えるのは妥当である。しかし、1つの動物モデルでは逆の結果が観察された。注目すべきは、腸の炎症に関連する科であるプレボテラ科に関して、2つの不眠症臨床研究で矛盾する結果が報告されており、不眠症患者の間で一貫性のない変化が観察されたことである。さらに、不眠症の高齢者のコホートでは、モノグロバス科とその属であるモノグロバスが睡眠効率と正の相関関係にあることがわかった[147]。 |
| 属レベルでは、不眠症患者と健常者の間で有意に異なる属がいくつか報告されており、ラクトバチルス、レンサ球菌、バクテロイデス、ラクノスピラ、フェカリバクテリウム、ローズブリア、プレボテラ、ビフィズス菌、アシダミノコッカス、エロモナス、アッカーマンシア、エルシミクロビウム、アネロプラズマ、クロストリジウム・センス・ストリクト、およびブラウティアが含まれる。具体的には、ラクノスピラとバクテロイデスは急性不眠症患者と健常対照者を区別するマーカー細菌として同定され、フェカリバクテリウムとブラウティアは慢性不眠症患者と健常者で異なっていた。さらに、ラクノスピラ、フェカリバクテリウム、バクテロイデス、およびブラウティアは血漿IL-1βレベルとPSQIスコアに関連していた[148]。 |
| 研究された属のうち、連鎖球菌(1つの研究)[149]、アシダミノコッカス(1つの研究)[141]、アエロモナス、およびブラウティア(2つの研究)[139,148]は、不眠症の被験者または動物で存在量が増加していることが示されました。逆に、ビフィズス菌、ラクノスピラ、エルシミクロビウム、アナエロプラズマ(1つの研究)、およびプレボテラ(3つの研究)は、低いレベルで観察されました。連鎖球菌の増加とプレボテラおよびラクノスピラの減少は、うつ病/不安を伴う潰瘍性大腸炎患者の糞便微生物群集でも観察されました[150]。食事成分を代謝して短鎖脂肪酸を生成することで知られるローズブリアは、相反する結果を示し、1つの臨床研究では増加が報告され、別の研究では減少が報告されました。これは、異なる不眠症の状態が、異なる腸内細菌叢構造につながる可能性があることを示唆しています[151]。重要なことに、臨床研究で特定された不眠症に関連する特定の微生物分類群は重複しないことが多く、今後の研究では、更年期周辺期の女性や他の疾患のない慢性不眠症患者などの特定の集団における大規模な腸内細菌叢解析の必要性が強調される。さらに、ラクトバチルスとラクトバチルス・クリスパタスに関しては、ある臨床研究では増加が認められたが[149]、4-クロロ-DL-フェニルアラニン(PCPA)誘発性不眠症動物モデルでは減少が認められた[143]という矛盾する結果が見られた。バクテロイデスについても同様の不一致が観察された[7,152]が、これはヒトと動物の腸内細菌叢の固有の差異に起因する可能性がある。さらに、舌の特徴と口腔微生物プロファイルを不眠症の診断バイオマーカーとして利用する可能性が検討されている。不眠症患者の口腔微生物叢では、健康な人に比べてクロストリジア、ベイロネラ、バチルス、ラクトバチルス科の相対存在量が高いことがわかっており、アクチノバクテリア、クロストリジア、未分類のラクトバチルス科などのいくつかの分類群は、不眠症の潜在的な口腔微生物バイオマーカーとして示唆されている[153]。 |
| これらの知見は、不眠症患者に見られる腸内細菌叢の変化の複雑さと多様性を強調するものであり、特定の微生物群の正確な役割と睡眠関連の結果への潜在的な影響を解明するためのさらなる研究の必要性を示している。腸内細菌叢は全身の健康維持に重要な役割を果たしており、不眠症に伴う腸内細菌叢の異常は宿主に悪影響を及ぼす可能性がある。したがって、腸内細菌叢は不眠症の診断において重要な標的となる。 |
| 2.14.不眠症における腸内細菌叢由来代謝物の変化 |
| 腸内細菌叢の乱れは、腸内微生物の代謝およびそれによって生じる代謝物に影響を与えます。これらの代謝物は、腸脳軸とその機能を結びつける重要なメディエーターです。これらの腸内細菌叢由来代謝物には、短鎖脂肪酸、胆汁酸、アミノ酸、ペプチド、ペプチドグリカン、リポ多糖、バクテリオシンなど、様々な化合物が含まれます。近年の研究結果は、短鎖脂肪酸、胆汁酸、リポ多糖が不眠症に関与していることを示唆しています(図3)。 |
| 6122人の独立した横断的コホートからの証拠は、腸内細菌叢-胆汁酸軸が慢性不眠症と心血管代謝疾患との関連性を確立する上で重要な役割を果たしていることを示唆している。具体的には、この研究では、ムロコール酸とノルコール酸が慢性不眠症と正の相関関係を示し、イソリトコール酸は負の相関関係を示すことがわかった[154]。これらの知見は、腸内細菌叢-胆汁酸軸を標的にすることで、慢性不眠症に関連する心血管代謝への影響を軽減できる可能性があることを示唆している。さらに、睡眠障害モデルマウスで実施された研究では、胆汁酸レベルと不眠症との間に強い関連性があることが明らかになった。その結果、結腸のケノデオキシコール酸レベルが有意に低下し、タウロ-α-ムロコール酸とβ-ムリコール酸レベルが有意に上昇することが示された。デオキシコール酸とリトコール酸は、腸内細菌叢の触媒作用によって肝臓で合成される2つの胆汁酸であり、脱水酸化を受ける。このプロセスに関与する微生物には、ラクトバチルス属、ビフィドバクテリウム属、エンテロバクター属、バクテロイデス属、クロストリジウム属などがある[155]。これらの知見は、不眠症が腸内細菌叢を乱し、胆汁酸代謝に影響を与えるという考えをさらに裏付けるものである。しかし、胆汁酸などの微生物代謝物と不眠症との因果関係については、この分野で実施された検証実験の数が限られているため、さらなる調査が必要であることに留意することが重要である。 |
| リポ多糖はグラム陰性細菌の細胞壁に存在する重要な成分です。微生物と宿主の相互作用のメディエーターであり、腸内に豊富に存在し、腸から放出され、炎症反応を阻害する一連の事象を開始し、全身性炎症と神経炎症、および記憶障害を引き起こします[156,157]。一般的に、炎症プロセスは、エンドトキシン代謝経路を介したNF-κB転写の活性化によって開始され、リポ多糖がリポ多糖結合タンパク質に結合し、その後受容体CD14に転移します。リポ多糖-リポ多糖結合タンパク質CD14複合体は、その後、Toll様受容体4(TLR4)に結合し、炎症性サイトカインの分泌を開始し、代謝性炎症を引き起こします[158]。不眠症の文脈では、睡眠障害は腸内細菌叢の異常を引き起こし、炎症反応を誘発し、ヒトの認知障害を引き起こすことがわかっています(図3)。興味深いことに、これらの効果は無菌マウスでは抑制された[120]。また、抗生物質治療は睡眠障害マウスの認知障害をさらに悪化させる[159]。さらに、「睡眠障害マイクロバイオータ」を無菌マウスに移植すると、認知機能障害、神経炎症レベルの上昇、および認知プロセスに関連する2つの脳領域である海馬と内側前頭前皮質におけるミクログリア活性の増加が特に引き起こされた[120]。これらの知見は、腸内マイクロバイオータが睡眠障害の認知機能と神経炎症への有害な影響を媒介する上で重要な役割を果たしていることを強調している。別の研究では、睡眠障害関連の炎症、認知障害、および腸内マイクロバイオータの乱れは、メラトニンの外因性補給によって軽減できることが示された[140]。著者らは、メラトニンがリポ多糖レベルを低下させ、腸内の有益な微生物と酪酸レベルを促進すると提唱した。これらの変化は、TLR4/NF-κBシグナル伝達経路を調節することにより、海馬の炎症と神経細胞のアポトーシスを軽減します。このような結果は、TLR4/IκBα/NF-κB p65軸を阻害することにより、メラトニン受容体アゴニストであるRamelteon(訳者注:ラメルテオン(先発品名:ロゼレム)は、体内時計を調整するメラトニン受容体に作用し、自然な眠りを誘発する不眠症治療薬です。主に寝付きの悪さ(入眠困難)の改善に用いられ、依存性が少ないのが特徴です。主な副作用は眠気、めまい、頭痛、倦怠感、便秘などです)を投与することで、アストロサイトにおけるリポ多糖誘発性炎症反応が大幅に改善されることを観察した別の研究によって裏付けられています。保護効果はin vivoげっ歯類モデルで確認されており、メラトニン受容体アゴニストが睡眠調節にも重要な役割を果たすアストロサイトにおけるリポ多糖誘発性損傷を保護できることが示唆されています[160,161]。さらに、リポ多糖結合タンパク質はモノアミン(セロトニンやノルアドレナリンなど)の生合成を阻害し、ドーパミン-β-ヒドロキシラーゼおよび芳香族-L-アミノ酸脱炭酸酵素の内因性阻害剤として作用することで睡眠に影響を与えます[162]。 |
| 短鎖脂肪酸は主に大腸での嫌気性細菌発酵によって生成され、腸管免疫機能の維持と腸管バリア機能の調節に重要な役割を果たします[163]。さらに、短鎖脂肪酸はリポ多糖やサイトカインによって刺激されたマクロファージにおけるTNF-αやIL-6などの炎症促進性メディエーターの産生を阻害します[164,165]。研究により、短鎖脂肪酸はミクログリアの成熟を調節し、神経炎症プロセスを予防することも示されています[166]、[167]、[168]。睡眠障害はプロピオン酸、酢酸、酪酸の腸内レベルを低下させることがわかっています[120]。この低下は、ローズブリア、プレボテラ、ラキノスピラなどの腸内短鎖脂肪酸産生細菌の減少を伴います[148]。したがって、短鎖脂肪酸の減少は、不眠症患者や動物モデルで観察されるリポ多糖の増加によって媒介される炎症反応に寄与する可能性があります。しかし、不眠症の高齢者の糞便中短鎖脂肪酸レベルと睡眠の継続性の関係を調査した研究では、酢酸、酪酸、プロピオン酸、および総短鎖脂肪酸の濃度が高いほど、睡眠効率が低く、入眠潜時が長くなることがわかった[147]。その中でも、酪酸は睡眠調節の重要な物質であると考えられている[169]。これらの矛盾する結果は、年齢、性別、体格指数、身体活動、基礎疾患、投薬など、研究間の被験者の生理学的要因のばらつきによるものかもしれない。傾向スコアマッチング分析は、交絡因子を考慮するために利用でき、研究間の公平な比較を可能にする。 |
| さらに、マルチオミクス解析により、不眠症患者とそうでない患者の間で、グリセロリン脂質代謝、グルタチオン代謝、窒素代謝、アラニン、アスパラギン酸、グルタミン酸代謝、アミノアシルtRNA生合成を含む5つの代謝経路に差異があることが明らかになった[149]。要約すると、現在の文献では、不眠症患者の腸内微生物代謝に大きな変化が見られることが示されている。腸内微生物生態系の乱れはしばしば炎症を引き起こし、不眠症の症状や全体的な健康状態を悪化させる可能性がある。したがって、短鎖脂肪酸や胆汁酸などの不足している代謝物を補充することで、不眠症の症状を軽減し、患者の健康状態を改善できる可能性がある。 |
| 2.15.不眠症における免疫因子およびその他の因子の変化 |
| 臨床研究および動物実験では、睡眠障害または睡眠障害が炎症反応の持続的な活性化につながることが一貫して示されています。これは、C反応性タンパク質(CRP)およびIL-1β、IL-6、TNF-αなどの炎症促進因子の血中濃度が著しく上昇し、IL-5やIL-10などの抗炎症因子が減少するという特徴があります。さらに、睡眠障害はリポ多糖、リポ多糖結合タンパク質、コルチゾールの濃度上昇と関連しており、可溶性CD14は減少します(表2)。実験研究では、部分的および完全な睡眠障害の両方が炎症に関与する細胞内シグナル伝達経路を活性化し、IL-6およびTNF-αの転写を上方制御することが示されています[170,171]。メタ分析では睡眠障害と睡眠時間はTNF-αレベルと直接関連しない可能性があると報告されているが、腸内の免疫細胞から放出されるTNF-αとIL-1βが中枢神経系と相互作用し、視床下部の視索前野など覚醒を調節する領域に影響を与える可能性があることは注目に値する。このような相互作用は、視床下部と脳幹のニューロンの発火パターンを変化させ、最終的に脳の覚醒活動に影響を与える可能性がある[172]。さらに、不眠症患者の血中IL-1βレベルの変化と特定の微生物種、特にプレボテラ・アムニー、バッカリス、ティモネンシス、カラーランズとの間に負の相関関係が見られた[149]。これらの知見は、不眠症によって誘発される炎症反応が腸内細菌叢と代謝産物によって調節されていることを示唆している。 |
| さらに、不眠症は、ゾヌリンとS100β(訳者注:S100βは、主に脳内のアストロサイト(グリア細胞)から分泌される分子量約21kDaのカルシウム結合タンパク質です。神経損傷時に血液や脳脊髄液へ放出されるため、頭部外傷、脳卒中、急性脳症などの脳損傷の程度を示すバイオマーカーとして広く臨床利用されています)のレベルの増加、およびダミンオキシダーゼ、D-乳酸、エンドトキシン、腸脂肪酸結合タンパク質のレベルの低下によって示されるように、腸管バリアの完全性と血液-脳関門の透過性を阻害することがわかっています(図3)[120,173]。重要な研究では、睡眠不足中の代謝障害が結腸におけるα-ケトグルタル酸の蓄積につながることがわかりました。過剰なプロリルヒドロキシラーゼ2は低酸素誘導因子1タンパク質を分解し、腸管修復機能の障害につながり、これが腸管バリアへの睡眠不足による損傷の潜在的なメカニズムである可能性があります[174]。これらの知見は、不眠症、腸管バリアの完全性、血液-脳関門透過性の間の複雑な関係を強調しています。 |
| 腸内細菌叢が神経調節において果たす役割は証拠によってますます裏付けられているが[159,176]、腸内細菌叢が不眠症の重要な要因であることを直接特定するには、無菌マウスや糞便微生物叢移植を用いたモデル実験が貴重な知見をもたらす可能性がある。全体として、睡眠障害が個人の健康に及ぼす影響は多面的であり、腸内細菌叢や代謝産物だけに限られない。睡眠障害は生理的リズムを乱し、免疫系などの機能を弱める。したがって、十分な睡眠は全体的な健康を維持し、生活の質を向上させるために不可欠である。今後の研究では、不眠症の長期的な影響を引き続き調査し、公衆衛生への影響を軽減するための効果的な介入策を開発する必要がある。睡眠の重要性に対する一般の認識を高め、睡眠衛生を改善することで、プロバイオティクスによる不眠症に関連する健康問題の予防と管理において進歩が見られると期待できる。 |
| 2.16.不眠症に対するプロバイオティクスおよびポストバイオティクス介入 |
| 上記の結果は、腸内細菌叢と不眠症の間に明確な相互作用関係が存在することを示しています。同時に、腸内細菌叢の構成とプロバイオティクスの間には直接的な関連性があります。多くのプロバイオティクスはもともと消化管から分離されたものであり、FAO/WHOによって「十分な量を摂取した場合に宿主の健康に有益な生きた微生物」と定義されています[183]。さらに、ポストバイオティクスは「宿主に健康上の利益をもたらす無生物微生物および/またはその成分の製剤」と定義されており[184]、同様に腸内細菌叢に好影響を与えます[185]。したがって、プロバイオティクスとポストバイオティクスが不眠症の改善に有益な生物学的活性を持つかどうかを探求することが、新たな潮流となっています。 |
| 2.17.げっ歯類を用いた介入試験 |
| 動物モデルは、不眠症におけるプロバイオティクスの役割を研究する上で効果的なアプローチとなる。不眠症動物モデルは、大きく分けてストレス介入と化学介入の2つの方法で構築される(表3)。ストレス介入では、ローラー、多段式水槽、電気ショックなどの方法を用いて不眠症を誘発する。不眠症動物モデルにおける化学介入は、主に4-クロロ-DL-フェニルアラニンやカフェインなどの物質を用いる。現在、4-クロロ-DL-フェニルアラニンの腹腔内注射による不眠症誘発が、モデル構築における主要な手法となっている。 |
| 表3.動物介入試験におけるプロバイオティクスの効果 |
 |
| 注:プロバイオティクスの投与量は、マウスでは体重1kgあたり0.025kg、ラットでは体重1kgあたり0.25kgに標準化しました。 |
| 4-クロロ-DL-フェニルアラニンの腹腔内注射は、トリプトファン水酸化酵素の選択的かつ不可逆的な阻害剤として広く利用されており、セロトニン(5-HT)合成を効果的に阻害し、不眠症モデルの確立に高い成功率を示している[186]。この方法により、介入がセロトニン作動系障害に起因する不眠症を軽減できるかどうかを評価することができる。さらに、4-クロロ-DL-フェニルアラニン誘発性不眠症は動物実験で一般的に用いられている(表3)。しかし、4-クロロ-DL-フェニルアラニン誘発性不眠症は可逆的な状態であり、一般的に4-クロロ-DL-フェニルアラニン投与後9〜14日間という比較的短い期間しか不眠症の症状が持続しないことに注意する必要がある[187]。4-クロロ-DL-フェニルアラニン投与の時間と投与量を変えることで不眠症の効果を延長する試みは価値がある。しかしながら、以前の介入研究では、4-クロロ-DL-フェニルアラニン誘発性不眠症のラットにおいて、わずか7日間のナラタケ発酵酒の摂取がセロトニン系と腸内細菌叢の調節を介して睡眠の質を改善する効果があることが実証されている[188]。もちろん、短期間のプロバイオティクス介入が睡眠を改善するかどうかについては、さらなる研究が必要である。 |
| げっ歯類を用いた研究は、睡眠サイクルを調節する分子メカニズムの解明にも重要な役割を果たしてきた。例えば、以前の研究では、睡眠サイクル中に発現が変化する遺伝子を解析し、脂質代謝に重要な役割を果たし、正常な睡眠を維持するために必要なアストロサイト脳型脂肪酸結合タンパク質FABP7を同定した。マウスでFABP7遺伝子をノックアウトすると、断続的な睡眠パターンが生じる[189]。これらの遺伝子をノックアウトすることで、プロバイオティクスやその他の関連製品が睡眠の質に及ぼす有益な効果を評価するための不眠症げっ歯類モデルを構築する可能性が期待される。 |
| げっ歯類の睡眠の質の評価は、主に侵襲的な脳波/筋電図法とペントバルビタール誘発睡眠検査(表3)[188,190,191]を用いて行われています。しかし、これらの方法には、睡眠の中断、術後の回復時間、処置に関連した感染症や死亡、電極の位置ずれやノイズ信号などの問題といった欠点があります。ケージの床下のセンシングパッドを使用してマウスの動きを監視するPiezoSleepのような非侵襲的な睡眠モニタリングシステムは、その可能性から注目を集めています。このシステムは、センシングパッドによって検出された振動の変化と覚醒時の呼吸パターンを分析するためにSleepStatsソフトウェアを使用します[192,193]。このシステムは、マウスとラットに埋め込まれた電極を使用して検証されており[192]、自動的かつ視覚的な睡眠覚醒スコアリングの信頼できる代替手段を提供します。ただし、プロバイオティクス介入に関連する不眠症の改善を評価する研究では使用されていません。ペントバルビタール誘発睡眠試験は、健康食品検査評価技術規程(2003年版)に概説されているように、睡眠促進物質の有効性を評価する方法の1つです。この方法は、試験物質がペントバルビタールによって誘発される睡眠時間を延長できるかどうかを評価し、睡眠時間の延長は試験物質の睡眠促進効果を示します。以前の研究では、高収率γ-アミノ酪酸プロバイオティクス株によって生成された発酵乳が、ペントバルビタールナトリウムによって誘発される睡眠時間を延長し、入眠潜時を短縮することがわかり、この細菌株の睡眠延長効果を示しています[191]。さらに、オープンフィールドテストは、不眠症を評価する間接的な方法としても使用できます[194]。 |
| 不眠症改善におけるプロバイオティクスの可能性を評価するための動物実験は、薬物モデルの期間が限られていること、自然回復、睡眠の質の評価が主観的であることなどの課題があるため、限定的である。PiezoSleepシステムは今後の睡眠研究に有望であるが、プロバイオティクスを用いて不眠症を改善するメカニズムを完全に理解するためには、睡眠の質を評価するためのより信頼性の高い方法が必要である。 |
| 3.ヒト介入試験 |
| げっ歯類を用いた研究に加え、不眠症患者を対象とした多数の研究が行われており、ヒト介入試験においてプロバイオティクスの抗不眠作用、睡眠の質改善効果、および抗ストレス効果が検討されている(表4)。これまでの研究では、プロバイオティクスを3~12週間投与することで、PSQI、不眠症重症度指数(ISI)、およびアテネ不眠症尺度で評価した睡眠の質が有意に改善し、同時に不安、ストレス、抑うつ、および認知機能も改善することが示されている[109,152,197]。二重盲検プラセボ対照ランダム化試験では、ラクトバチルス・アシドフィルス Rosell-52またはビフィドバクテリウム・ロンガム Rosell-175を摂取しても、ストレスイベントに関連する生理的または心理的症状や睡眠障害は改善されなかった[198]。これらの研究結果は、すべてのプロバイオティクスが不眠症に有益な効果をもたらすわけではなく、プロバイオティクスの種類によって機能的な特異性がある可能性を示唆している。ただし、前述の研究は睡眠の評価に主観的な尺度のみを用いており、客観的な正確性に欠けていることに留意する必要がある。 |
| 表4.不眠症またはその他の関連症状を有する被験者に対するプロバイオティクスの効果に関するヒト介入研究 |
 |
 |
 |
注:プロバイオティクスの投与量は、成人では体重60kg、小児では体重20kgを基準として標準化しました。 略語:AISはアテネ不眠尺度、EGGは脳波検査、不眠重症度指数はISI、PSQIはピッツバーグ睡眠質問票、ESSはエプワース睡眠尺度を表します。 |
| いくつかの研究では、被験者の睡眠の質をより客観的に評価するために睡眠モニタリング機器が使用されています。これらの研究の中には、プロバイオティクスまたはポストバイオティクスの摂取による効果を評価することに焦点を当てたものもあります。たとえば、脳波と小栗白川あずみ睡眠質問票スコアを使用して睡眠を評価した研究では、ラクチカゼイバチルス・カゼイ・シロタ株の摂取によりノンレム睡眠の減少が防止され、δパワーが20%以上増加したことがわかり、このプロバイオティクス株の摂取がストレス誘発性不眠症を改善する可能性があることが示唆されました[199]。別の研究では、不活化ラクトバチルス・ガセリCP2305を12週間摂取すると、脳波とPSQIで評価した睡眠の質が有意に向上することが示されました[200]。同様に、アクチグラフィーでモニタリングしたラクトバチルス・ヘルベティカスCM4発酵乳の介入後には、睡眠効率の延長と覚醒時間の減少という睡眠改善効果が観察されましたが、主観的モニタリングデータでは同じレベルの改善は示されませんでした[201]。全体として、脳波計の使用は、特に睡眠効率、覚醒回数、睡眠構造などの客観的な情報を提供することにより、睡眠の質をより客観的に評価することを可能にします。脳波計によって得られる客観的な指標は、特に主観的な尺度が有意な改善を示さない場合に、睡眠構造の変化を詳細に理解することができます。しかし、アクチグラフィー記録に基づく絶対および相対睡眠時間、睡眠開始後の絶対および相対覚醒時間、睡眠開始潜時、および睡眠効率は、プロバイオティクス介入によって影響を受けませんでした[202]。14の研究に基づくメタ分析の結果、プロバイオティクスまたはパラプロバイオティクスはPSQIスコアを有意に低下させましたが(-0.78ポイント、95%信頼区間:0.395~1.166、P < 0.001)、その他の主観的な睡眠尺度の変化や、ポリソムノグラフィーまたはアクチグラフィーを使用して測定された睡眠の客観的パラメータの変化には有意な効果は見られませんでした[203]。それだけでなく、別のメタアナリシスでは、腸内細菌叢の調節による睡眠の質の改善効果は有意ではなかった(P = 0.31)[204]。したがって、プロバイオティクスやポストバイオティクスで睡眠を改善するには、評価および分析方法のさらなる改良が必要である。 |
| ポストバイオティクス介入研究の中には、不眠症の改善に有望な効果を示すものもある(表4)。例えば、ラクトバチルス・ヘルベティカスMIKI-020ポストバイオティクスと、リラックス効果で知られるテアニンの組み合わせは、睡眠効率の改善を示した。同様に、不活化ラクトバチルス・ガセリCP2305は睡眠増強効果を示した[207]。しかし、他の研究では、不活化ラクティカセイバチルス・ラムノサスJB-1[208]またはレビラクトバチルス・ブレビスSBC8803[209]を投与しても、睡眠の質に有意な改善は見られなかったが、これらの菌株の中にはマウスの不眠症や概日リズム睡眠障害に改善効果を示したものもある。これらの矛盾する結果は、プロバイオティクスとポストバイオティクスの効果は宿主または種特異的であることを示唆している。研究間で有益な効果にばらつきが見られるのは、細菌株、製品の形態(プロバイオティクスまたはポストバイオティクスとして投与されるか、錠剤、乾燥粉末、またはプロバイオティクス発酵乳)、投与量、介入期間、および種間の違いなどが関係している可能性がある。 |
| 不眠症の根本原因や、気分やストレス関連の問題との関連性など、その他の要因も、プロバイオティクスやポストバイオティクス製品による症状改善効果に影響を与える可能性があります。現在、健康な人の不眠症に関する研究は限られており、この特定の集団を対象とした研究はわずか5件しかありません[201,208,[210], [211], [212]。これらの研究では、「健康な被験者」とは一般的に、睡眠に影響を与える重大な疾患や精神障害のない人を指します。しかし、これらの2つの研究の結果は、睡眠の質を評価するために主観的指標と客観的指標を使用した場合に矛盾を示しています(表4)。これらの矛盾する結果は、睡眠評価方法の選択が、睡眠の質を改善するプロバイオティクスまたはポストバイオティクス介入の効果を決定する結果に影響を与える可能性があることを示唆しています。 |
| 注目すべきは、プロバイオティクスやポストバイオティクスによる介入に関する現在の研究のほとんどが、睡眠改善の根底にある分子メカニズムの分析よりも、治療効果の評価に重点を置いている点である。分子レベルでの有益なメカニズムを理解することは、将来的に有望なプロバイオティクス候補を特定し、不眠症を管理するための非従来型の薬物療法を設計する上で極めて重要である。腸内微生物叢と不眠症との相互作用は、宿主の腸内細菌叢を調節できるプロバイオティクスやポストバイオティクスに基づいた不眠症管理戦略の開発にも新たな道を開く。 |
| 4.プロバイオティクスとポストバイオティクスによる睡眠調節の潜在的なメカニズム |
| 4.1.腸内細菌叢とメタボロームの再構築 |
| ヒトの腸は、消化管全体に存在する神経細胞とグリア細胞の複雑なネットワークから構成される、非常に複雑な神経ネットワークです。腸は栄養吸収という主要な役割に加え、様々なシグナル伝達経路を介して脳とコミュニケーションを取り、気分や行動に影響を与えるという重要な役割も担っています。さらに、クロストリジウム目、ラクトバチルス目、バクテロイデス目、バクテロイデス門、フィルミクテス門などの一部の腸内細菌群は、概日リズムを示します[223]、[224]、[225]。同様に、短鎖脂肪酸や酪酸などの腸内細菌代謝物も、一日を通してリズミカルに変動します[226、227]。その結果、腸内に生息する数兆個の細菌からなる腸内細菌叢は、代謝、消化器、神経系の状態に幅広い影響を与えると考えられている[228]、[229]、[230]、[231]。 |
| 2019年に、アルツハイマー病の治療薬として「GV-971」[232](別名マンナンナトリウム)という新薬が開発されました。この薬は、腸内細菌叢を刺激して必須アミノ酸と短鎖脂肪酸を産生させることで作用します[233]。これらの代謝産物は、脳の老廃物を除去し、神経細胞間の接続を維持するために重要な、ヒトの脳内の神経伝達物質の活性に影響を与えます。この薬の導入は、腸を標的としたアプローチが脳関連疾患の治療に利用できることを示す重要なマイルストーンです。この概念をさらに発展させると、不眠症は腸内細菌叢とその代謝産物の組成の変化を引き起こし、それが睡眠障害と関連している可能性があります。腸と脳の複雑な関係は、プロバイオティクス介入によって腸内細菌叢を標的にすることで、不眠症に関連する症状を軽減できる可能性があることを示唆しています。したがって、プロバイオティクスは、腸内細菌叢とその代謝産物に良い影響を与えることで睡眠を調節し、睡眠パターンを改善する有望な微生物生態学的プロバイオティクス剤として期待されている。 |
| これまでの介入研究では、特定のプロバイオティクス株が不眠症の症状を緩和し、睡眠の質を向上させるという有益な効果を裏付ける証拠が示されており、その有益な効果は腸内細菌叢の調節を伴います。たとえば、ラクティプランティバチルス・プランタルム JYLP-326 は、試験不安のある学生の不眠症の症状を緩和し、腸内細菌叢の異常を部分的に改善しました [152]。ラクティプランティバチルス・プランタルムJYLP-326 に加えて、他のプロバイオティクス株も睡眠に良い効果を示しています。ラクトバチルス・ガセリCP2305 [215] とプロバイオティクス製品 NVP-1704 (リモシラクトバチルス・ロイテリNK33 と ビフィドバクテリウム・アドレセンティスNK98 の 2 つの株から構成) [109] は、どちらも腸内細菌科の増殖を抑制し、睡眠の質を改善しました。注目すべきことに、NVP-1704の補給により腸内乳酸菌とビフィズス菌の量が増加した。別の研究では、ビフィズス菌アニマリス亜種ラクティスBB-12VR(BB-12)を補給したところ、ビフィズス菌のレベルが上昇し、乳児の泣き時間の減少と総睡眠時間の増加に有意に関連していた[220]。これらの知見は、十分な量の腸内ビフィズス菌が睡眠の質を改善する上でプラスの影響を与えること、および特定のプロバイオティクス株がより健康な腸内細菌叢を回復させ、不眠症の緩和に役立つ可能性を示している。これらの効果の根底にあるメカニズム、特にプロバイオティクス摂取後の機能性腸内微生物代謝物の変化を解明するために、さらなる研究が必要である。 |
| 以前の研究では、ビフィズス菌アニマリス亜種ラクティスBB-12VRを補給すると、疝痛のある乳児の糞便中のプロピオン酸レベルが上昇し、途切れることのない睡眠時間が長くなることが示されました [234]。プロバイオティクスの投与は、腸内ビフィズス菌を増加させることで リポ多糖レベルを低下させ、腸管バリアを介した リポ多糖の移行率を低下させます (図 4) [235]。アルコール性肝障害のあるマウスを対象とした研究では、ラクティプランティバチルス・プランタルムJ26 が腸内 リポ多糖含有量を減少させ、潜在的なグラム陰性病原菌の存在量を減少させました [236]。前述のように、Toll 様受容体 4 (TLR4) は、リポ多糖誘導ミクログリア活性化および炎症反応の媒介において重要な役割を果たします [237]。これらの知見は、プロバイオティクス投与がToll 様受容体 4の発現を減少させ、脳内でのNF-κBの転座を阻害し[238]、それによってToll 様受容体 4を介したMAPKシグナル伝達経路の活性化を抑制し[239]、結果として神経炎症を軽減することを示唆している。 |
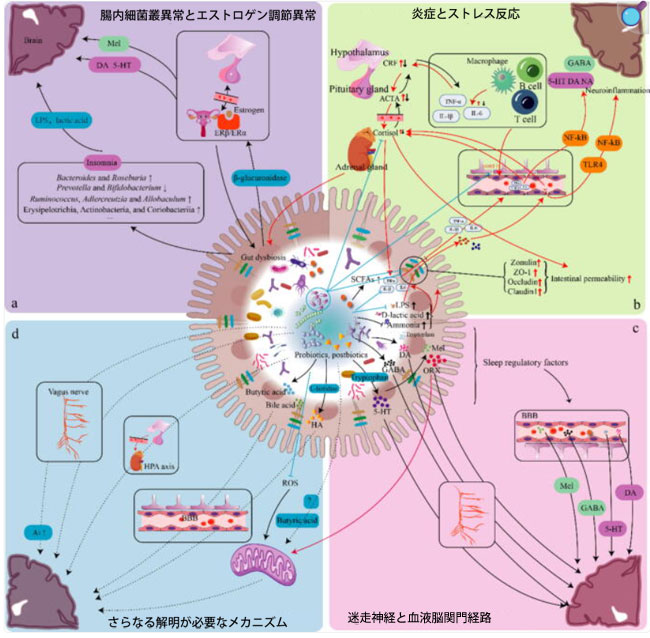 |
図4. 睡眠調節におけるプロバイオティクスの潜在的なメカニズム。 (a) プロバイオティクスの摂取は、腸内細菌叢の構成、代謝産物、および腸管バリアの完全性を調節することができます。腸内細菌叢の異常は腸管バリアの完全性を損ない、リポ多糖の移行や乳酸の全身循環への漏出、炎症誘発因子の産生刺激につながります。最終的に、このような腸管バリア機能の障害は血液-脳関門の機能に影響を与え、有害な腸内代謝産物が脳に入り込み、正常な脳機能に影響を与える可能性があります。β-グルクロニダーゼはエストロゲンの脱抱合に関与する酵素であり、腸内細菌叢の多様性の低下はβ-グルクロニダーゼ活性に悪影響を及ぼし、エストロゲンレベルの低下につながります。エストロゲン障害はメラトニンやセロトニンなどの物質のレベルに影響を与え、睡眠覚醒システムに影響を与えます。 (b) ストレス反応と炎症は腸管バリアの損傷や視床下部-下垂体-副腎(HPA)軸の障害を引き起こす可能性があり、特定の乳酸菌でさえコルチゾールレベルに影響を与える可能性があります。さらに、特定のサイトカインは腸内細菌叢によって調節され、障害を受けると、最終的に神経炎症や脳機能に影響を与える特定の物質の障害を引き起こします。 (c) 腸内細菌叢と腸上皮細胞によって産生されるγ-アミノ酪酸やセロトニン(5-HT)などの睡眠調節因子は、血液-脳関門および迷走神経経路を介して睡眠に影響を与えます。腸粘膜の末梢オレキシンは脳機能を調節することができます。メラトニンは腸内でトリプトファンから合成されます。 (d) プロバイオティクスが不眠症を改善するメカニズムについては、さらに調査する必要がある追加のメカニズムがあります。これらのメカニズムには、プロバイオティクスが他の代謝物、受容体、ミトコンドリアに及ぼす影響が含まれる可能性があります。ミトコンドリア関連経路は睡眠において重要な役割を果たしており、プロバイオティクス介入は活性酸素種レベルを阻害することでミトコンドリア機能を調節することができる[277]。酪酸はミトコンドリア機能の調節において重要なメディエーターであり[278]、オレキシンはミトコンドリア機能とダイナミクスの調節因子である[279]。これらはすべて睡眠覚醒システムに関連している。さらに、特定の細菌群集や代謝物が迷走神経、血液-脳関門を介して、または視床下部-下垂体-副腎軸の活動に影響を与えることで睡眠に影響を与えるかどうかについても検討する必要がある。実線は特定された経路を示し、破線は現在特定されていないか、引き続き検討する必要がある経路を示す。赤線は促進を示し、青線は阻害を示す。 略語:5-HT、5-ヒドロキシトリプタミン(セロトニン);A1、アデノシン受容体;ACTH、副腎皮質刺激ホルモン;BBB、血液-脳関門; CRF、副腎皮質刺激ホルモン放出因子;DA、ドーパミン;IL、インターロイキン;GABA、γ-アミノ酪酸;LPS、リポ多糖;Mel、メラトニン;NA、ノルアドレナリン;NF-κB、チロシンキナーゼ受容体B;ORX、オレキシン;ROS、活性酸素種;SCFA、短鎖脂肪酸;SRF、睡眠調節因子;TLR4、トール様受容体4;TNF、腫瘍壊死因子;ZO-1、ゾヌラオクルデンス-1。 |
| 数多くの研究により、乳酸菌、ビフィズス菌、大腸菌、腸球菌などの特定の腸内微生物やプロバイオティクスが、トリプトファン、セロトニン、脳由来神経栄養因子、γ-アミノ酪酸などの神経伝達物質やさまざまな睡眠調節因子を合成する能力があることが証明されている[24,25,240,241]。以前のマウス研究では、高γ-アミノ酪酸産生ラクトバチルス株によって調製された33.33 mg/kg γ-アミノ酪酸を含む発酵乳を摂取した場合にのみ不眠症が改善し、腸内細菌叢と代謝産物組成に有意な変化が見られ、腸内アドレルクレウツィア、アロバキュラム、酪酸の増加が見られた[191]。有益な効果を引き起こすには、機能性代謝産物の十分な高濃度が必要であることが実証されている。さらに、腸内細菌叢を破壊する抗生物質の使用は、腸内のセロトニンを枯渇させ、睡眠パターンに影響を与えることが示されており[242]、セロトニンが睡眠調節における腸内細菌叢と脳の間のコミュニケーションに役割を果たしている可能性があることを示唆している。セロトニンを合成する能力が高いレビラクトバチルス・ブレビスPBS072やビフィドバクテリウム・ブレーベBB077などのプロバイオティクスは、唾液コルチゾールレベル、睡眠の質、不安などの精神生理学的指標の大幅な改善を示している[197]。同様に、別のプロバイオティクス株であるラクトバチルス・カゼイ327は、結腸でのセロトニンの産生を間接的に増加させることがわかっており[26]、加熱殺菌したラクトバチルス・カゼイ327の摂取は、排便頻度が比較的低い健康な成人の排便を改善する可能性がある[243]。しかし、この菌株に不眠症に対する効果があるかどうかは、さらなる研究が必要である。 |
| これらの研究結果は、腸、腸内細菌叢、脳の間の複雑なコミュニケーションネットワークである腸脳軸の調節における特定のプロバイオティクス株の役割を強調しています。プロバイオティクスの補給は、不眠症によって影響を受ける腸内微生物、腸内細菌叢由来の代謝物(リポ多糖や短鎖脂肪酸など)、γ-アミノ酪酸やセロトニンなどの他の重要な代謝物の乱れたバランスを回復させる可能性があります。これらの因子を調節することにより、プロバイオティクスとその代謝物(ポストバイオティクスとして知られる)は、睡眠の質に直接的または間接的にプラスの影響を与える可能性があります(図4)。 |
| 4.2.腸管バリアと血液-脳関門の完全性を高める |
| 腸管バリアは、腸管免疫を維持し、外部環境からの潜在的な病原体から体を守るために不可欠です[244]。睡眠不足は腸管バリアの完全性を損ない、透過性を高め、ゾヌリン濃度の上昇[120,245]や、ゾヌラオクルデンス-1、オクルディン、クローディン-1などのタイトジャンクションタンパク質の発現低下を引き起こします[7]。腸管バリアの損傷は、腸内細菌叢の異常、ストレス反応、炎症による細胞間タイトジャンクションタンパク質の減少、および腸管細胞の損傷と関連しています。毒素やD-乳酸[221]、アミノ酸代謝から生成される腸内アンモニア[246]、抗生物質、リポ多糖などの代謝産物によって引き起こされる腸内細菌叢の不均衡は、腸管免疫細胞による炎症性因子の放出を誘発し、腸管バリアの完全性を損なう可能性があります。一方、日和見病原菌の過剰増殖も腸内細菌叢の異常や腸管タイトジャンクションの破壊に寄与している[246,247]。コルチゾールの過剰レベルは腸管透過性を高める可能性がある。外因性プロバイオティクスとポストバイオティクスを摂取することで腸内細菌叢と代謝物のバランスを回復させ、腸管バリアの完全性を保護することができる。例えば、ペディオコッカス・ペントコッカス PP04は、オクルディン、クローディン-1、ゾヌラオクルデンス-1などの回腸タイトジャンクションタンパク質の発現を促進する効果を示した[248]。ラクティプランティバチルス・プランタルム J26は腸管リポ多糖レベルを低下させることが示されており、嫌気性細菌によって産生される短鎖脂肪酸は腸管免疫機能の維持と腸管バリア機能の調節に役立つ[165](図4b)。 |
| 腸は体内で最大の内分泌器官であり、神経伝達物質やホルモンなどのさまざまな生物学的シグナルを放出する上で重要な役割を果たしています。これらのシグナルは、有害物質を排除する選択的フィルターとして機能する血液-脳関門を通過して血流に入り、脳に直接影響を与えることができます。不眠症患者は血清中のS100βレベルが高く、不眠症患者からマウスへの糞便微生物叢移植により、レシピエントマウスのS100βレベルが上昇しました[120]。これは、特に血液-脳関門の完全性が弱まっている場合に、腸内微生物叢が血液-脳関門を介して不眠症に影響を与える可能性があることを示唆しています。神経伝達物質および関連するシグナル伝達分子は、腸管神経系に局所的に作用するか、血液-脳関門または迷走神経を介して脳に直接影響を与えることができます。これらは脳機能に影響を与え、腸内の神経細胞に情報を伝達する能力を持っています。さらに、腸内細菌叢はトリプトファンとグルタミン酸を血流中に放出し、これらは下流の輸送体や受容体と相互作用し、それによってセロトニンとγ-アミノ酪酸の合成を促進し、睡眠の質に影響を与える可能性がある[24,25,249]。自然発生的なマウス系統である老化促進マウス8(SAMP8)マウスは、アルツハイマー病で観察される遺伝子発現の変化やタンパク質異常に関連する加速老化特性を示し、睡眠障害やノンレム睡眠とレム睡眠の両方の持続時間の減少も含まれる。プロバイオティクスは、腸内細菌叢とその代謝物のバランスを回復し、炎症やストレス反応を軽減し、抗生物質に代わることで、老化促進マウス8マウスの血液-脳関門損傷を大幅に軽減することが示されている[238](図4c)。要するに、入手可能な実験的証拠は、プロバイオティクスが腸管バリアを保護し、血液-脳関門の完全性を維持することによって不眠症を改善する可能性があることを示唆している。 |
| 5. 視床下部-下垂体-副腎軸を介した内分泌経路の調節 |
| 前述の通り、視床下部-下垂体-副腎(HPA)軸は睡眠調節において重要な役割を果たす重要な内分泌経路です。コルチゾールとエピネフリンはともに、視床下部-下垂体-副腎軸におけるサイトカイン分泌を調節することで、免疫細胞の機能と分化、そして腸内細菌叢に影響を与えます。 |
| ラットを対象とした研究では、ラクチカゼイバチルス・カゼイ・シロタ株を含む餌を 2 週間投与した。水回避ストレスに曝露した後、ラットの血漿コルチコステロン濃度、および室傍核における c-Fos (神経活動のマーカー) と副腎皮質刺激ホルモン放出因子の発現を調べた。結果は、ラクチカゼイバチルス・カゼイ・シロタ株の投与が、ストレス条件下で 視床下部-下垂体-副腎 軸の活動を調節し、コルチコステロン分泌を抑制する可能性があることを示している [250]。熱失活させた ラクトバチルス・ガセリ CP2305 を使用した別の研究では、唾液コルチゾールの放出とストレス応答性マイクロ RNA (miR-144 および miR-144) の発現を抑制しながら睡眠を改善する能力があることが明らかになった [207]。さらに、ラクティプランティバチルス・プランタルム PS128TM の投与は、コルチゾール濃度、不眠症、およびネガティブな感情を大幅に改善した [214]。これらの研究に基づくと、プロバイオティクスはヒトと動物の両方において視床下部-下垂体-副腎軸を調節することで不眠症を改善する可能性を秘めていると推測できる。これらの知見は、プロバイオティクスが睡眠調節とストレス反応に関わる内分泌機構の調節に役割を果たし、不眠症に対する潜在的な治療法となる可能性を示唆している。 |
| 近年の研究により、卵巣ホルモン代謝と脳内ホルモン分泌の調節に関与する視床下部-下垂体-卵巣軸に対する様々な細菌の重要な影響が明らかになってきた(図4a)。Jiachaoらは、ビフィドバクテリウム・アニマリス亜種ラクティス V9による介入が腸内の短鎖脂肪酸レベル(酢酸、プロピオン酸、酪酸)を改善することでペプチドYYと胃空腹ホルモンの放出を刺激し、最終的に血中黄体形成ホルモンと黄体形成ホルモン/卵胞刺激ホルモンレベルを抑制することを発見した[251]。β-グルクロニダーゼはエストロゲンを脱抱合し、エストロゲン受容体αとβに結合させる酵素である[252,253]。腸内微生物の多様性の低下はβ-グルクロニダーゼ活性に悪影響を及ぼし、エストロゲンレベルの低下につながる可能性がある[253]、[254]、[255]。この低下は、有益な細菌の増加と有害な細菌の増殖の抑制に関連している[256]。さらに、視床下部-下垂体-卵巣軸と多くの神経伝達物質の間には相互作用がある。例えば、視床下部-下垂体-卵巣軸の障害は、夜間のメラトニン分泌の低下につながる可能性があり[34]、セロトニン(5-HT)[257]およびドーパミン [258]にも影響を与える可能性がある。 |
| 要約すると、コルチゾールとエストロゲンのレベルに関わる内分泌障害は不眠症の一因となる可能性があります。プロバイオティクスとポストバイオティクスは、ホルモン、腸内細菌叢、および腸内細菌叢由来の代謝産物を調節することにより、これらの内分泌障害に関連する不眠症を軽減する可能性を秘めています。 |
| 5.1.免疫調節 |
| 睡眠調節因子と免疫系は密接な関係にあり、睡眠調節に関与する様々なサイトカインが末梢免疫系に存在します(図4b)。特に、IL-1βは視床下部前部におけるノルアドレナリンとドーパミンの放出を増加させ、視床下部におけるセロトニン(5-HT)濃度を調節します。一方、TNF-αは脳内のセロトニンとその代謝産物である5-ヒドロキシインドール酢酸(5-HIIA)の濃度を上昇させます。さらに、TNF-αとIL-1βは主にコルチゾール濃度に影響を与え、NF-κB経路を活性化することでノンレム睡眠を調節し、その結果、視床下部-下垂体-副腎軸の活性が亢進します[259]。炎症性サイトカインは、キヌレニン経路を開始させることでセロトニン濃度を低下させることもあります[260]。炎症性因子の濃度が低いと、睡眠が促進され、睡眠の質が向上し、神経が保護されます。一方、TNF-α、IL-6、IL-1βなどの炎症性サイトカインのレベル上昇は、有害な影響を及ぼす可能性があります。これらのサイトカインは、グルタミン酸作動性シグナル伝達を増強する一方でγ-アミノ酪酸シグナル伝達を減少させ、その結果、脊髄後角の侵害受容細胞の興奮性が高まり、中枢神経系内の細胞を含む宿主細胞に潜在的な損傷を与える可能性があります[261]。したがって、これらの炎症性サイトカインは不眠症に関連するマーカーとして機能し、中枢性感作に寄与し、睡眠障害を伴う睡眠調節因子障害において重要な役割を果たします。 |
| さらに、免疫系と腸内細菌叢は複雑に相互に関連しています。腸内細菌叢の変化と腸管透過性の亢進は、全身性炎症の主な原因です。例えば、リポ多糖を含むグラム陰性菌の移行は、炎症性サイトカインのレベル上昇につながります[262]。SLAB51のようなプロバイオティクスを摂取すると、ビフィズス菌などの抗炎症性細菌の腸内量が増加し、カンピロバクター目などの炎症性細菌の濃度が低下します。さらに、プロバイオティクスは腸内で短鎖脂肪酸産生菌の増殖を刺激し、短鎖脂肪酸レベルの上昇をもたらします。腸内で抗炎症性および神経保護性の短鎖脂肪酸が増加すると、血流中の炎症性サイトカインのレベルが低下し、抗炎症性サイトカインの濃度が上昇します[263]。さらに、プロバイオティクス補給は、IL-12やIL-4などの様々な炎症性サイトカインのレベルを大幅に低下させる一方で[264]、IL-10、グルタミン酸、一酸化窒素、および総抗酸化能のレベルを著しく増加させることが示されている[265]、[266]、[267]、[268]、[269]。これらの知見は、プロバイオティクスの抗炎症作用の可能性を強調しており、それによって不眠症が改善される。 |
| 5.2.神経調節 |
| 求心性迷走神経は、腸と脳の間の神経伝達経路として機能し、プロバイオティクスが腸-脳軸を介して脳機能を向上させる重要な経路でもあります。迷走神経は腸内細菌叢と不眠症に関連する症状を結びつけています。例えば、迷走神経切断術を受けたマウスや腸内細菌叢を除去したマウスでは、睡眠障害に関連する炎症反応が見られませんでした[140,270]。これは、腸内細菌叢と迷走神経の両方が、睡眠障害関連症状の根底にある経路において重要な役割を果たしていることを示唆しています。プロバイオティクスは、この腸-脳軸を介して脳機能を改善することができます。特に、プロバイオティクス株SBC8803は、睡眠日誌のスコアを改善し、迷走神経を刺激することが報告されています[209]。SBC8803の迷走神経への影響は、セロトニン受容体を阻害することで打ち消すことができます。これらの観察結果から、SBC8803はセロトニンを介したシグナル伝達を伴う迷走神経経路を介して睡眠に影響を与えるという仮説が立てられる(図4c)。 |
| さらに、ラクチカゼイバチルス・ラムノーススJB-1 は、前頭前皮質と扁桃体では γ-アミノ酪酸 mRNA の転写を減少させ、海馬では増加させることがわかっています [271]。これは、プロバイオティクスが脳のさまざまな領域で γ-アミノ酪酸に異なる影響を与える可能性があることを示唆しています。さらに、研究によると、ラクトバチルス・ジョンソニーLa1 を十二指腸内に注射すると、遠心性胃迷走神経の活動が増加し、食物摂取量の増加につながることが示されています [272]。逆に、ラクティカゼイバチルス・パラカゼイST11 はラットの遠心性迷走神経神経細胞の活動を阻害し、食物摂取量の減少につながることがわかっています [273]。これは、プロバイオティクスが菌株特異的なニューロンの調節を示し、開始または阻害のいずれかを引き起こすことを示唆しています。結論として、プロバイオティクスは迷走神経を介して不眠症を調節し、γ-アミノ酪酸とセロトニンを含む神経経路に影響を与え、その調節効果は菌株特異的である。さらに、腸内細菌叢によって産生されるD-乳酸やアンモニアなどの神経毒性代謝物は、迷走神経を介して中枢神経系に入り込み、脳機能に影響を与える可能性がある[274]。 |
| プロバイオティクスは副交感神経と迷走神経を介して視床下部-下垂体-副腎軸を安定させ、睡眠覚醒システムを維持します。ラクトカセイバチルス・カゼイ・シロタの摂取はコルチコステロンホルモンの増加を抑制し、迷走神経にシグナルを送って室傍核のストレス反応を軽減することで睡眠を改善する可能性があることがわかっています[250]。これらの知見は、プロバイオティクスが迷走神経経路を介して睡眠に影響を与えることを示しています。しかし、菌株特異的な効果を特徴づけるには、さらなる実験が必要です。迷走神経における関連受容体の発現を調べることで、迷走神経を介した不眠症改善に関わる特定の分子メカニズムを明らかにすることができます。 |
| 最近の研究では、ショウジョウバエの腸内タンパク質濃度と腸内分泌細胞の活動との間に相関関係があることが明らかになったことは注目に値する。これらの細胞はペプチドCCHa1を放出し、これが脳内の少数のドーパミン神経細胞に信号を送り、ショウジョウバエの機械的振動に対する反応を調節する。ペプチドCCHa1のレベルが上昇すると、ショウジョウバエはより強い振動に反応して睡眠モードに入ることができるが、ペプチドCCHa1を摂取すると弱い振動があっても覚醒状態になる可能性がある[275]。しかし、プロバイオティクスとプレバイオティクスがこのシグナル伝達ペプチドに影響を与えるかどうか、また、このペプチドが迷走神経を利用して信号を伝達するかどうかは不明である。さらに、腸内代謝物に対する他の調節経路や腸内細菌叢の構造についても、さらなる研究が必要である(図4d)。一方、ミトコンドリアと睡眠の関係についても言及したが、多くの研究でミトコンドリアの機能が腸内細菌叢と密接に関連していることが示されている[276]。しかしながら、両者の因果関係は依然として不明である。図4dに示された経路に加えて、他の経路の探索も重要である。したがって、今後の解析では、ミトコンドリア機能の誘導性障害を標的とし、それが睡眠に及ぼす影響やコロニー間の相互作用を検証することに焦点を当てるべきである。 |
| 前述の知見は、プロバイオティクスが腸内細菌叢と代謝異常を改善する可能性があり、同時に神経、免疫、内分泌経路を利用して腸脳軸内でのコミュニケーションを確立するという説得力のある証拠を提供する。この複雑なコミュニケーションは、神経炎症の緩和、迷走神経系の活性化、および脳機能の調節に寄与する。しかしながら、睡眠に対するプロバイオティクス介入のメカニズムに関する現在の理解はまだ初期段階にある。睡眠パターンは、腸管透過性の変化、免疫系の活動、炎症、エネルギー獲得、微生物の多様性など、さまざまな要因によって影響を受ける。プロバイオティクスが腸内細菌叢をどのように調節するかの詳細な経路と、腸-脳軸に関与する特定の調節については、まだ解明されていない。読者の解釈を容易にするために、最後に略語表を追加した(表5)。 |
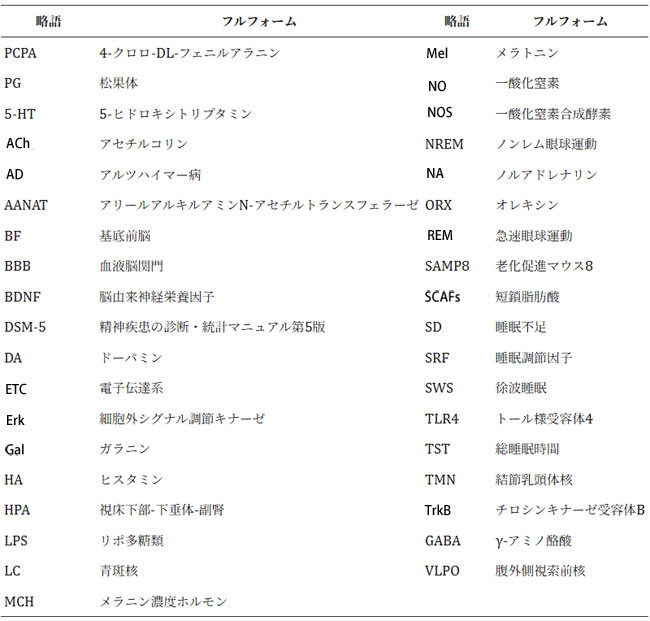
| 表5.本研究で使用した略語一覧 |
 |
| 6.結論 |
| 睡眠と腸内細菌叢の関連性に関する理解は近年大きく進展している。不眠症は、代謝障害、炎症反応、睡眠不足に起因する情緒障害など、腸内細菌叢と密接に関連する生理的・心理的変化を引き起こす可能性がある。腸-脳相関の観点から、不眠症による脳機能障害が腸機能と腸内細菌叢に悪影響を及ぼすことが明らかになっており、プロバイオティクスは不眠症に対する処方薬の代替療法として有望視されている。しかしながら、腸機能障害、腸内細菌叢の異常、そして不眠症症状との因果関係を確立するためには、さらなる研究が必要である。 |
| プロバイオティクスとポストバイオティクスの投与は、健康な腸内細菌叢を回復させ、腸内細菌叢異常症に伴う疾患や代謝障害を改善する効果的な方法として注目されています。睡眠改善におけるプロバイオティクスの作用機序は、腸-脳相関、不眠症に関連する腸内細菌叢の変化、炎症反応、および睡眠の神経調節機構に根ざしています。プロバイオティクスは、腸内細菌叢とその代謝産物を調節し、内分泌系、神経系、および免疫系の反応に影響を与えることで、睡眠-覚醒行動を調節することができます。しかし、現在、プロバイオティクスが不眠症を改善するメカニズムは、適切な動物モデルが不足しているため、十分に検証されていません。 |
| 不眠症の改善におけるプロバイオティクスの役割を理解するには、標準化された睡眠行動指標と睡眠モニタリング方法が必要です。不眠症動物モデルをより正確にし、ヒトの不眠症と比較できるようにするための改良も必要です。最も重要なのは、さまざまな薬剤によって誘発された不眠症モデルと、睡眠薬やプロバイオティクスを含む介入を用いた実験を行うなど、実験デザインがしっかりしていることです。プロバイオティクスと睡眠薬の作用機序を分析および比較することで、プロバイオティクスのメカニズムをより深いレベルで解明することができます。新興のシングルセル空間マルチオミクス技術のような学際的な手法を導入することで、細胞内解像度で組織内の遺伝子発現、代謝、細胞配置を詳細に調査することが可能になります。最近の研究では、これらの技術を使用してマウスの脳と脊髄のさまざまな領域の遺伝子発現を分析し、正確な空間的遺伝子発現プロファイルを提供しています[280]。さらに、マウスの前頭皮質および線条体における加齢に伴う遺伝子発現の変化を研究するために、高解像度の細胞マップが構築されている[280,281]。興味深いことに、非神経細胞は神経細胞と比較して、より顕著な加齢に伴う変化を示し、明確な空間パターンを示した。この技術を不眠症時の脳の遺伝子発現プロファイルの研究に適用することで、この睡眠障害の根本的なメカニズムに関する新たな知見が得られる可能性がある。 |
| 不眠症の改善におけるプロバイオティクスの役割を理解するには、標準化された睡眠行動指標と睡眠モニタリング方法が必要です。不眠症動物モデルをより正確にし、ヒトの不眠症と比較できるようにするための改良も必要です。最も重要なのは、さまざまな薬剤によって誘発された不眠症モデルと、睡眠薬やプロバイオティクスを含む介入を用いた実験を行うなど、実験デザインがしっかりしていることです。プロバイオティクスと睡眠薬の作用機序を分析および比較することで、プロバイオティクスのメカニズムをより深いレベルで解明することができます。新興のシングルセル空間マルチオミクス技術のような学際的な手法を導入することで、細胞内解像度で組織内の遺伝子発現、代謝、細胞配置を詳細に調査することが可能になります。最近の研究では、これらの技術を使用してマウスの脳と脊髄のさまざまな領域の遺伝子発現を分析し、正確な空間的遺伝子発現プロファイルを提供しています[280]。さらに、マウスの前頭皮質および線条体における加齢に伴う遺伝子発現の変化を研究するために、高解像度の細胞マップが構築されている[280,281]。興味深いことに、非神経細胞は神経細胞と比較して、より顕著な加齢に伴う変化を示し、明確な空間パターンを示した。この技術を不眠症時の脳の遺伝子発現プロファイルの研究に適用することで、この睡眠障害の根本的なメカニズムに関する新たな知見が得られる可能性がある。 |
| 不眠症に関する進行中の臨床研究は、プロバイオティクスが睡眠に及ぼす影響を多角的に探究する機会を提供しています。総合的に見ると、分析結果は、プロバイオティクスが腸内細菌叢や睡眠調節因子やサイトカインなどの物質に影響を与える代謝産物を調節することで、不眠症だけでなく、不眠症によって引き起こされる炎症、腸管バリア機能障害、その他の有害作用も調節することを示しています。これらの知見は、プロバイオティクスによる不眠症調節の理解を深めるだけでなく、臨床治療に新たな展望をもたらします。特に、プロバイオティクスは患者の予後を改善する可能性があり、これは臨床上の意思決定に大きな影響を与える可能性があります。さらに、不眠症のメカニズムの研究は複雑であり、基礎研究における確固たる基盤が不可欠です。睡眠構造とパターンをより深く理解し、不眠症を抱える更年期前後の女性など特定の集団を掘り下げ、シングルセル空間マルチオミクスなどの高度な技術を活用することで、プロバイオティクスが介入前後の特殊な細胞や組織の代謝発現にどのように影響を与えるかについての洞察が得られます。この知識は、個々の患者に合わせた微生物精神医学的治療戦略を支援する可能性を秘めています。これらの知見を臨床応用するためには、今後の研究で、プロバイオティクスと他の栄養補助食品の不眠症に対する相乗効果を検討する必要があります。また、睡眠の質を包括的に評価するために、主観的評価と客観的評価の両方の方法を組み合わせることを推奨します。臨床医と研究者は、この分野の進歩を注意深く監視し、このエビデンスを臨床診療に統合することを検討すべきです。これらの取り組みを通じて、不眠症の分野において、より効果的な臨床管理と患者の転帰の改善が期待できます。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、J Adv Res. 2025 Jul 10;82:267–293.に掲載されたInsomnia: the gut microbiome connection, prospects for probiotic and postbiotic therapies, and future directions.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


