ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
補助的なプロバイオティクス療法は、腸内細菌叢と代謝産物の再構築を通じて、 胃食道逆流症の症状緩和を持続させる |
Yingmeng Li et al., |
|
|
| 要約 |
プロトンポンプ阻害薬(PPI)は胃食道逆流症(GERD)の標準治療薬ですが、長期使用は腸内細菌叢の異常、消化器系の副作用、および中止後の症状再発を引き起こします。プロバイオティクスは腸内環境を調節することで補助的な効果をもたらす可能性があります。本研究は、胃食道逆流症患者における多菌種プロバイオティクス(Lihuo)とラベプラゾールの併用療法の有効性、および腸内細菌叢と代謝産物への影響を評価することを目的としました。無作為化二重盲検プラセボ対照試験を実施し、胃食道逆流症患者120名を対象に、ラベプラゾールと多菌種プロバイオティクス(n=64)またはプラセボ(n=56)を8週間投与した後、プロバイオティクスまたはプラセボ単独を4週間投与しました。主要評価項目は、逆流性疾患質問票(RDQ)スコアの変化でした。副次的評価項目には、消化器症状評価尺度、内視鏡的治癒、およびマルチオミクスプロファイリング(ショットガンメタゲノミクス、ファージオーム、非標的/標的メタボロミクス)が含まれた。プラセボ群と比較して、プロバイオティクス群は、12週間の介入後に逆流性疾患質問票スコアが36.51%著しく減少した(P = 0.017)とともに、数値的な内視鏡的治癒率も高かった(36.84% vs 12.50%、P = 0.365)。メタゲノミクスでは、Bifidobacterium animalis、Lactiplantibacillus plantarum、およびClostridium sp.900540255の増加と、Bacteroides uniformisおよびClostridium Q fessumの減少が明らかになった。メタボロミクス解析では、γ-アミノ酪酸、コハク酸、シトルリン、短鎖脂肪酸のレベル上昇が認められ、Bifidobacterium animalisとγ-アミノ酪酸、Bacteroides fragilisとコハク酸など、興味深い微生物と代謝産物の相関関係が認められました(r ≥ 0.30、P < 0.01)。今回の結果は、プロバイオティクス補助療法が腸内細菌叢と生物活性代謝産物の標的調節と関連して、プロトンポンプ阻害薬投与後の症状緩和を持続させることを示唆しています。 |
| 肝要 |
| 胃食道逆流症(GERD)におけるプロトンポンプ阻害薬の長期使用は、腸内細菌叢を乱し、投与中止後に症状の再発を引き起こす可能性がある。本研究では、プロトンポンプ阻害薬投与後の逆流症状の軽減を、プロバイオティクス併用療法が持続させることを明らかにした。プロバイオティクスの使用により、有益な細菌群(BifidobacteriumとLactiplantibacillus plantarum)が増加し、γ-アミノ酪酸、コハク酸、シトルリン、および短鎖脂肪酸が増加した。これらの微生物叢の変化と代謝および臨床症状の改善との間に強い相関関係が認められた。本研究は、プロバイオティクス併用療法が胃食道逆流症の症状コントロールを強化し、腸内細菌叢の代謝恒常性を維持することを示している。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.材料と方法 |
| 2.1.研究デザインと参加者 |
| 2.2.無作為化と盲検化 |
| 2.3.研究デザインと介入 |
| 2.4.評価項目の定義 |
| 2.5.糞便DNA抽出、ショットガンメタゲノムシーケンス、およびシーケンス品質管理 |
| 2.6.細菌ゲノムのアセンブリ、ビニング、および機能予測 |
| 2.7.ファージゲノムプロファイリングと存在量解析 |
| 2.8.液体クロマトグラフィー質量分析法による非標的糞便メタボロミクス解析 |
| 2.9.糞便中の短鎖脂肪酸および神経活性化合物を対象とした糞便メタボロミクス解析 |
| 2.10.統計解析 |
| 3.結果 |
| 3.1.参加者の人口統計学的特性および研究コホート |
| 3.2.プロバイオティクス補給はプロトンポンプ阻害薬中止後の逆流症状の緩和を持続させる |
| 3.3.プロバイオティクスの併用投与は、胃食道逆流症患者の腸内細菌叢を再構築する |
| 3.4.プロバイオティクスの併用投与は胃食道逆流症患者の腸内ファージ群集を調節する |
| 3.5.プロバイオティクス併用投与は、腸内代謝モジュールおよび予測される生物活性代謝物プロファイルを調節する |
| 3.6.プロバイオティクスの併用投与は糞便メタボロームを変化させ、胃食道逆流症患者における微生物と代謝物の相互作用を明らかにする |
| 3.7.プロバイオティクスの併用投与は、神経活性化合物および短鎖脂肪酸の糞便中濃度を調節する |
| 4.考察 |
本文 |
| 1.はじめに |
| 胃食道逆流症(GERD)は、胃内容物が食道に病的に逆流する一般的な消化器疾患であり、胸やけ、逆流、胸骨後部痛などの慢性症状を引き起こし、重症例では粘膜損傷に至ることもあります(1)。胃食道逆流症の世界的な有病率は欧米諸国で最大20%に達し、中国では推定10.6%とされており、医療制度に大きな臨床的・経済的負担を与えています(2~4)。プロトンポンプ阻害薬(PPI)は、強力な酸分泌抑制効果を持つため、依然として第一選択薬として用いられています。しかし、一部の患者ではロトンポンプ阻害薬の使用中止後も症状が持続または再発し、長期投与は下痢、腹痛、便秘などの消化器系の副作用を伴います。重要なことに、ロトンポンプ阻害薬の長期投与は腸内細菌叢の構成と機能を阻害し、ディスバイオシスを悪化させ、腸管バリアの完全性を損ない、腸管感染症や代謝合併症を引き起こしやすくすることが示されています(5~7)。したがって、胃食道逆流症の管理には、代替または補完的な戦略を検討することが重要です。 |
| 新たな証拠は、胃食道逆流症の病態生理における腸内細菌叢の重要な役割を示唆している(8)。腸と脳の間の双方向のコミュニケーションは、腸-脳軸を介して行われ、微生物代謝物、免疫シグナル伝達、神経経路間の複雑な相互作用を伴い、これらはすべて内臓感覚と症状の認識に影響を与える(9)。γ-アミノ酪酸(GABA)、セロトニン(5-HT)、短鎖脂肪酸(SCFA)、トリプトファン誘導体などの主要な微生物代謝物は、腸管バリア機能を調節し、炎症反応を抑制し、胃腸運動と免疫恒常性を調節する(10、11)。これらの知見は、腸内細菌叢とその機能出力を標的とすることが、胃食道逆流症管理のための有望な補助戦略となる可能性を示唆している。 |
| プロバイオティクスは、「適切な量を摂取すると宿主に健康上の利益をもたらす生きた微生物」と定義されています(12)。プロバイオティクスの応用は、微生物バランスを回復し、消化管の健康をサポートする手段として認識されるようになりました。プロバイオティクスは、さまざまな機能性および炎症性腸疾患の症状を改善する効果があることが実証されています(6、13)。たとえば、Lacticaseibacillus paracasei F19は、プロトンポンプ阻害薬関連の腸症状を予防することが報告されています(14)。特に、Bifidobacterium animalis subsp. lactis MH-02をプロトンポンプ阻害薬と併用投与すると、胃食道逆流症患者の症状がより早く解消され、消化器症状評価尺度(GSRS)スコアが大幅に改善し、腸内細菌叢の多様性が向上しました(8)。これらの有望な結果にもかかわらず、胃食道逆流症における特定のプロバイオティクス株の臨床的有効性を評価する質の高いランダム化比較試験、特に縦断的なマイクロバイオームおよびメタボロミクス解析を取り入れた試験は、まだ限られています。 |
| 多菌種プロバイオティクス製剤(Lihuo)は、特性がよく知られている3つの菌株、Lacticaseibacillus paracasei Zhang(Zhang)、Lactiplantibacillus plantarum P9(P9)、およびBifidobacterium animalis subsp. lactis V9(V9)から構成されています。これらの菌株は、個々にも組み合わせても、消化器系の健康に有益な効果を発揮することが実証されています。Lacticaseibacillus paracasei ZhangとBifidobacterium animalis subsp. lactis V9の組み合わせは、腸内細菌叢の調節、炎症の軽減、代謝経路の調節によって便秘を緩和することが示されています(15)。同じ製剤は、腸粘膜細菌叢の再構築によって潰瘍性大腸炎の症状を緩和する効果も実証されています(16)。Lactiplantibacillus plantarum P9の補給は、有益な微生物分類群と代謝産物の増加を伴い、慢性便秘の改善と関連付けられています(17)。さらに、最近の証拠によると、Lactiplantibacillus plantarum P9は腸内細菌叢と代謝産物の機能を変化させることで慢性下痢を改善できることが示されています(18)。これらの菌株がディスバイオシス(腸内細菌叢の乱れ)を軽減し、微生物バランスを回復させる能力があることから、本研究では、補助的な多菌種プロバイオティクス療法が胃食道逆流症患者の症状緩和を強化し、腸内細菌叢の恒常性を促進するという仮説を立てました。 |
| ショットガンメタゲノミクスや非標的メタボロミクスなどの高度なマルチオミクスアプローチを活用したこの無作為化二重盲検プラセボ対照試験では、他菌種プロバイオティクスとラベプラゾールの併用療法の臨床効果を評価し、腸内細菌叢、ファージオーム、メタボロームにおける関連変化を特徴づけます。本研究は、プロバイオティクスを胃食道逆流症の管理における安全かつ効果的な補助療法として使用することを支持する包括的なエビデンスを提供し、微生物調節と臨床的に意義のあるアウトカムとの間のギャップを埋めることを目的としています。 |
| 2.材料と方法 |
| 2.1.研究デザインと参加者 |
| 本研究は、南昌大学第一附属病院(中国、南昌市)において、無作為化プラセボ対照二重盲検並行群間臨床試験として実施された。研究プロトコルは、南昌大学第一附属病院倫理委員会の承認(承認番号:IIT [2020] EC 003-2)を受け、中国臨床試験登録システム(登録番号:ChiCTR2000038409)に登録された。倫理ガイドラインに従い、すべての参加者から登録前に書面によるインフォームドコンセントを得た。 |
| 胃食道逆流症と診断された外来患者を研究施設で募集し、スクリーニングした。組み入れ基準は以下のとおりであった:(i)18~65歳の男性または女性、(ii)過去3か月以内に地元の三次医療機関で胃内視鏡検査を受け、食道炎(ロサンゼルス[LA]グレードA、B、またはC)が確認されたか、または典型的な胃食道逆流症の症状を伴う食道炎がなく、中国語版逆流性疾患質問票(RDQ)の合計スコアが12以上であった(19~21)。以下の基準のいずれかに該当する場合は、参加者を除外した:(i)過去2週間以内に酸抑制剤、制酸剤、消化管運動促進剤、胃粘膜保護剤、ハーブ療法、またはプロバイオティクスなどの胃食道逆流症関連薬を使用していた。 (ii) 肝酵素の上昇(アスパラギン酸アミノトランスフェラーゼまたはアラニンアミノトランスフェラーゼが正常上限値の 2 倍超)、血清クレアチニンが正常上限値の 1 倍超、心不全、または心電図異常;(iii) 過去 3 か月以内に消化性潰瘍、消化管出血、食道静脈瘤、または上部消化管悪性腫瘍の内視鏡診断;(iv) 心筋梗塞、脳梗塞、または悪性腫瘍の既往歴;(v) 胃食道または十二指腸の手術歴;(vi) 妊娠を積極的に試みている、妊娠している、または授乳中;(vii) インフォームドコンセントフォームを理解できない、または個人情報の提供を拒否するなど、研究手順に協力できない;(viii) プロバイオティクスまたは介入製品のいずれかの成分に対する既知のアレルギー;および (ix) 胃内容物停滞または幽門閉塞に続発する食道炎。 |
| 2.2.無作為化と盲検化 |
| 無作為化は、2名の独立したプロジェクト管理者によって、SASソフトウェア(バージョン9.4、SAS Institute、米国ノースカロライナ州キャリー)のPROC PLANプロシージャで作成されたコンピュータ生成のランダムシーケンスを用いて実施されました。参加者はプロバイオティクス群またはプラセボ群に1対1の比率で割り付けられ、割り付け順序は研究期間を通して参加者、担当医師、および研究者には秘匿されました。グループ割り付けは、不透明な連番の封筒に封入され、主要データ解析が完了するまで開封されませんでした。配布の秘匿性を確保するため、独立したプロジェクトマネージャーが、無作為化順序に対応する固有の識別番号をプロバイオティクスとプラセボの小袋に事前にラベル付けしました。両製品の包装と外観は同一であったため、参加者のケアと結果評価に関わるすべての関係者は、グループ割り付けについて盲検化されました。 |
| 2.3.研究デザインと介入 |
| 本研究は、2週間の導入期間、8週間の介入期間、プロトンポンプ阻害薬投与中止後の4週間の追跡期間という3つの段階から構成された(図1a)。 |
|
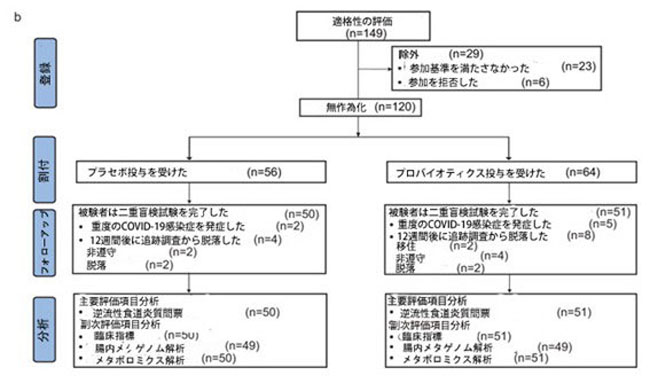 |
図1. 研究デザインと参加者フロー図。 (a) 3段階の研究の概略図:2週間の導入期間、ラベプラゾールとプロバイオティクスまたはプラセボを併用する8週間の介入段階、プロトンポンプ阻害薬中止後にプロバイオティクスまたはプラセボを継続投与する4週間の追跡段階。[略語]PPI: プロトンポンプ阻害薬 (b) 試験報告の統合基準(CONSORT)フロー図。ITT(intention-to-treat、N = 120)およびPP(per-protocol、N = 101)集団における参加者の登録、割り当て、追跡、および最終解析を示す。除外は、脱落、非遵守、または転居による。すべての解析は二重盲検条件下で実施された。 |
| 8週間の介入期間中、参加者全員は、ラベプラゾール(1日1回、食前20mg;エーザイ中国株式会社、中国上海)による標準的なプロトンポンプ阻害薬療法と、多菌種プロバイオティクス混合物またはプラセボのいずれかを併用して投与された。続く4週間の介入期間中、参加者はプロトンポンプ阻害薬の投与を中止し、プロバイオティクスまたはプラセボのみの投与を継続した。 |
| プロバイオティクスとプラセボは、Jinhua Yinhe Biological Technology Co., Ltd.(中国浙江省)から提供された。他菌種プロバイオティクス粉末の各小袋には、Lacticaseibacillus paracasei Zhang(8 × 10⁹ CFU)、Bifidobacterium animalis subsp. lactis V9(2.4 × 10¹⁰ CFU)、およびLactiplantibacillus plantarum P9(8 × 10⁹ CFU)からなる多菌株製剤が含まれていた。プラセボ粉末はマルトデキストリンで構成され、色、食感、味はプロバイオティクスと一致するように調整された。プロバイオティクス群の参加者は、食後にプロバイオティクス粉末を1日2袋摂取し、プラセボ群の参加者はプラセボを1日2袋摂取した。研究期間中、参加者には通常の生活習慣と食習慣を維持するよう指示したが、アルコール、喫煙、および辛いものや脂っこいものなどの刺激物を避けるよう指示した。患者は、各診察時(4週目、8週目、12週目)に、胃食道逆流症関連薬(酸抑制剤、制酸剤、消化管運動促進薬、胃粘膜保護剤、および上記と同様の効能を持つハーブ療法)、プロバイオティクス、プレバイオティクス、およびプロバイオティクスを含む食品(ヨーグルトなど)の使用状況を記録する必要があった。これらの薬剤および製品はすべて厳しく禁止されていた。治療遵守状況は、返却された空の包装単位(ラベプラゾールのブリスターパックおよび小袋)の数を数えることで監視された。参加者が配布された資料の少なくとも80%を返却した場合、遵守状況は適切であるとみなされた。 |
| 2.4.評価項目の定義 |
| 主要評価項目は、ベースライン(0週目)および4週目、8週目、12週目に評価した中国語版逆流性疾患質問票(22)の合計スコアの変化とした。逆流性疾患質問票は、過去1週間の4つの主要症状(胸やけ、非心臓性胸痛、胃酸逆流、胃内容物の逆流)を評価する自己記入式質問票である(23)。各症状は、頻度(0~5)と重症度(0~5)の2つの側面で評価され、0は症状なし、値が高いほど頻度または重症度が増すことを示す。逆流性疾患質問票の合計スコアは、8項目すべてのスコアの合計として算出され、スコアが高いほど症状の負担が大きいことを示す。 |
| 副次的評価項目には、消化器症状評価尺度スコア、体格指数(BMI)、内視鏡的治癒状態、および糞便メタゲノムプロファイルとメタボロームプロファイルの変化が含まれた。消化器症状評価尺度は、過去1週間の胃腸症状を評価する15項目から構成され、腹痛、逆流、下痢、消化不良、便秘の5つのサブスケールに分類された。各項目は0(不快感なし)から3(重度の不快感)で評価された。サブスケールスコアは、関連する項目の平均として計算され、消化器症状評価尺度合計スコアは、15項目すべての平均として算出された。BMIは、各研究訪問時に、一晩絶食後の朝に、標準化された体重および身長測定器具を使用して測定された。胃内視鏡検査は、最初に逆流性食道炎を呈した参加者に対して12週目に繰り返された。すべての処置は、標準化されたプロトコルに従って2人の上級臨床医によって実施され、食道炎の重症度はLA分類システム(グレードA~D)(24)に従って分類され、治癒はLAグレード0(粘膜の損傷なし)への改善と定義された(25、26)。 |
| 有害事象や臨床検査結果を含む安全性に関する結果は、各診察時に記録された。糞便サンプルは、0週、4週、8週、12週にすべての参加者から採取され、直ちに-80℃で凍結保存され、その後の腸内メタゲノムおよびメタボロームの解析に用いられた。 |
| 2.5.糞便DNA抽出、ショットガンメタゲノムシーケンス、およびシーケンス品質管理 |
| 糞便サンプルから、製造元の指示に従い、Magnetic Soil and Stool DNA Kit(DP712; TIANGEN Biotech Co., Ltd.、中国北京)を用いて糞便DNAを抽出した。抽出したDNAは、ライブラリー調製前に定量および品質評価を行った。ショットガンメタゲノムシーケンスは、Illumina Novaseq 6000プラットフォーム(Illumina Inc.、米国カリフォルニア州サンディエゴ)を用い、150 bpのペアエンドリードで実施した。得られた生シーケンスデータは、Kneaddata(https://github.com/biobakery/kneaddata)を用いて、低品質塩基、アダプター配列、および宿主由来リードを除去した。品質フィルタリングおよび宿主由来リードの除去後、サンプルあたり平均10.43 Gbpの高品質で宿主由来リードを含まないクリーンなデータが得られた。 |
| 2.6.細菌ゲノムのアセンブリ、ビニング、および機能予測 |
| クリーンデータは、メタゲノムデータセットに最適化されたデフォルトパラメータ(27)を用いてMEGAHIT(v1.2.9)によりコンティグにアセンブルされた。メタゲノムアセンブルゲノム(MAG)は、MetaBAT2(28)、VAMB(29)、およびDAS Tool(30)を組み合わせたマルチビナーアプローチによって再構築され、その後、冗長性を最小限に抑え、ビンの完全性を向上させるためにカスタムスクリプトによる精緻化が行われた。得られたメタゲノムアセンブルゲノムの品質はCheckM(31)を用いて評価され、高品質(完全性≧80%、汚染率≦5%)、中品質(完全性≧70%、汚染率≦5%)、または部分品質(閾値が低い)に分類された。高品質のメタゲノムアセンブルゲノム は、dRep (32) を使用して、パラメータ -pa 0.95 および -sa 0.95 を使用して重複を除去し、平均ヌクレオチド同一性閾値 95% でゲノムをクラスタリングし、各クラスタから最高品質の代表ゲノムを選択して、種レベルのゲノムビン (SGB) を生成しました。ゲノムビンの分類学的注釈は、Kraken2 を使用して、National Center for Biotechnology Information Non-Redundant Protein Sequence Database に対して行いました。サンプル間の各 ゲノムビンの相対存在量は、CoverM (https://github.com/wwood/CoverM; パラメータ: --min-read-percent-identity 0.95 --min-covered-fraction 0.4) を使用して計算しました。 |
| 腸内代謝モジュール(GMM)、すなわち主要な微生物代謝プロセスに関与する保存された酵素機能のセットは、公開文献およびMetaCycデータベースに基づいて推定された。ゲノムビンの機能的可能性は、オープンリーディングフレーム(Prodigalを使用して予測)を京都遺伝子ゲノム百科事典(KEGG)データベースに対して注釈付けし、代謝モジュールを特定することによって評価された。これらのモジュールのゲノムビン全体にわたる分布は、Omixer-RPM(パラメータ:-c 0.66)を使用して決定された。さらに、メタボロミクスデータセットでトレーニングされたキュレーションされた遺伝子-代謝物リンクデータベースを活用し、MelonnPanワークフローをメタゲノムデータに適用して、腸内生態系における生物活性微生物代謝物のプロファイルを予測した。 |
| 2.7.ファージゲノムプロファイリングと存在量解析 |
| VIBRANT(33)およびCheckV(34)を用いて、1,000 bpを超えるアセンブル配列からウイルスコンティグを同定した。下流解析には、5,000 bpを超える高信頼性ウイルスコンティグのみを残した。これらのコンティグは、種内変異を考慮するため、ヌクレオチド相同性95%、アライメントカバレッジ80%の閾値を用いてCD-HITによりウイルス操作分類単位(vOTU)にクラスタリングした(35)。得られたウイルス操作分類単位は、189,680個の腸管由来ウイルスゲノムを含む包括的な参照データベースであるメタゲノム腸管ウイルスカタログ(36)との比較により、分類学的注釈を付与した。各ウイルス操作分類単位の相対存在量は、CoverM(https://github.com/wwood/CoverM)を使用して、以下のパラメータで計算されました:--min-read-percent-identity 0.95、--min-read-aligned-percent 0.5、--proper-pairs-only、および--exclude-supplementary。 |
| 2.8.液体クロマトグラフィー質量分析法による非標的糞便メタボロミクス解析 |
| 糞便代謝物の抽出は、既報のプロトコル(18、37)に従って実施した。具体的には、糞便サンプルを内部標準として2-クロロフェニルアラニンを含むメタノール溶液中でホモジナイズした。得られたホモジネートを超音波処理して代謝物を効率的に抽出した後、4℃、12,000 rpmで10分間遠心分離した。得られた上清を0.22 μmメンブレンフィルターでろ過し、液体クロマトグラフィー質量分析法による解析に供した。メタボロミクスプロファイリングは、Agilent 1290 Infinity LC超高速液体クロマトグラフィーシステム(Agilent Technologies, Inc.、米国カリフォルニア州サンタクララ)とTriple TOF 6600+質量分析計(AB SCIEX、米国マサチューセッツ州フレイミングハム)を組み合わせた装置を用いて実施した。クロマトグラフィー分離は、25℃に維持されたACQUITY UPLC BEHアミドカラム(2.1 × 100 mm、Waters Corporation、米国マサチューセッツ州ミルフォード)で行われた。移動相は、溶媒A(25 mM酢酸アンモニウムと25 mMアンモニア水溶液)と溶媒B(アセトニトリル)からなり、以下のグラジエント溶出プログラムが用いられた:0~0.5分(95% B);0.5~7分(95%~65% B);7~8分(65%~40% B);8~9分(40% B);9~9.1分(40%~95% B);9.1~12分(95% B)。流速は0.5 mL/分に設定され、注入量は2 μLであった。質量分析計は加熱式エレクトロスプレーイオン化源を備え、正イオンモードと負イオンモードの両方で動作した。質量電荷比(m/z)60~1,000および25~1,000の範囲でフルスキャン質量スペクトルを取得した。主な装置パラメータは、イオン源温度600℃、カーテンガス圧30psi、および両方のイオン化モードにおけるイオンスプレー電圧5,500Vであった。 |
| 生の質量分析データは、ProteoWizard (バージョン v3.0.8789) を使用して mzML 形式に変換され、ピーク検出、アライメント、および統合のために R パッケージ XCMS を使用して処理されました。重要な代謝物の推定同定は、Human Metabolome Database (HMDB; http://www.hmdb.ca/)、LipidMaps (https://www.lipidmaps.org/)、mzCloud (https://www.mzcloud.org/)、Massbank (http://www.massbank.jp)、および 京都遺伝子ゲノム百科事典(https://www.kegg.jp/) データベース (38) と照合することによって達成されました。同定された代謝物のパスウェイおよび機能エンリッチメント分析は、MetaboAnalyst プラットフォーム (https://www.metaboanalyst.ca/MetaboAnalyst/home.xhtml) を使用してさらに実施されました。 |
| 2.9.糞便中の短鎖脂肪酸および神経活性化合物を対象とした糞便メタボロミクス解析 |
| 短鎖脂肪酸の濃度はガスクロマトグラフィー質量分析法(39)を用いて測定した。具体的には、糞便サンプルを秤量し、1 mLの超純水に懸濁後、10秒間ボルテックスミキサーで撹拌し、ボールミルを用いて均質化した。均質化物を氷上で超音波処理した後、4℃、10,000×gで15分間遠心分離した。上清を新しい2 mLマイクロ遠心チューブに移した。続いて、50%硫酸0.1 mLと抽出溶媒(内部標準として2-メチルバレレート25 mg/Lを含むメチルtert-ブチルエーテル)0.8 mLを添加した。混合物を10秒間ボルテックスミキサーで撹拌し、再度同じ条件で遠心分離した。得られた有機相(上澄み液)を回収し、その後の分析のためにサンプルバイアルに移した。ガスクロマトグラフィー質量分析は、Agilent J&W HP-FFAPキャピラリーカラム(30 m × 250 μm × 0.25 μm、Agilent Technologies, Inc.、米国カリフォルニア州サンタクララ)を接続した島津製作所製GC2030-QP2020 NXシステム(島津製作所、京都)を用いて行った。キャリアガスにはヘリウムを用い、流量は1.2 mL/minに一定とした。オーブンの温度プログラムは以下のとおりです。初期温度50℃(1分間保持)、50℃/分の昇温速度で150℃まで上昇(1分間保持)、次に10℃/分の昇温速度で170℃まで上昇(0分間保持)、25℃/分の昇温速度で225℃まで上昇(1分間保持)、最後に40℃/分の昇温速度で240℃まで上昇(1分間保持)。インジェクター、トランスファーライン、イオン源の温度はそれぞれ220℃、240℃、240℃に設定しました。質量分析は、-70 eVの電子衝撃イオン化モードで実施し、m/z範囲33~150でスキャンモードおよび選択イオンモニタリングモードでデータを取得しました。 |
| 神経活性化合物は、検証済みの標的メタボロミクス法(40)を用いて分析した。簡単に説明すると、糞便サンプルを秤量し、80 μLの予冷した抽出溶媒(−20°Cの0.1%ギ酸を含むアセトニトリル)と20 μLの超純水と混合した。混合物を30秒間ボルテックスし、4分間45 Hzで均質化し、氷上で5分間超音波処理を3回繰り返した。−20°Cで一晩インキュベートした後、サンプルを4°Cで12,000 × gで15分間遠心分離した。上清80 μLを40 μLの100 mM Na2CO3溶液と40 μLのアセトニトリル中の2%ベンゾイルクロリドと混合し、室温で30分間インキュベートして極性化合物を誘導体化した。内部標準物質 10 μL を添加した後、サンプルを同じ条件下で再度遠心分離した。得られた上清 40 μL を脱イオン水 20 μL と混合し、超高速液体クロマトグラフィー・タンデム質量分析用のオートサンプラーバイアルに移した。分離は、Waters ACQUITY UPLC HSS T3 カラム (100 × 2.1 mm、1.8 μm; Waters Corporation、Milford、MA、USA) を装備した ExionLC UHPLC システム (AB SCIEX、Framingham、MA、USA) で 4 °C に維持して行った。移動相は、溶媒 A (0.1% ギ酸と 1 mM ギ酸アンモニウムを含む水) と溶媒 B (アセトニトリル) から構成された。オートサンプラーは 6 °C に維持し、注入量は 1 μL とした。検出は、QTRAP 6500+質量分析計(AB SCIEX社、米国マサチューセッツ州フレイミングハム)を用い、正イオンエレクトロスプレーイオン化モードで実施した。イオンスプレー電圧は+5000 V、カーテンガス圧は35 psi、イオン源温度は400℃、ネブライザーガス圧は60 psiに設定した。定量は多重反応モニタリング法を用いて行った。 |
| 2.10.統計解析 |
| サンプルサイズの推定は、主要評価項目である逆流性疾患質問票スコアの変化に基づき、既発表の研究(41)の効果量データと臨床専門家の意見を参考にしました。プロバイオティクス群とプラセボ群の逆流性疾患質問票スコアの平均差は3.67ポイント、プール標準偏差(SD)は6.04と想定しました。両側有意水準5%で検出力80%を達成するには、各群最低43名の参加者が必要でした。脱落率を20%と見積もった結果、目標サンプルサイズは各群53名となりました。 |
| すべての統計解析とデータ可視化はRソフトウェア(バージョン4.1.0)を使用して実行され、図はAdobe Illustratorで精緻化されました。有効性は、intention-to-treat(ITT)集団(訳者注:ランダム化比較試験(RCT)において、ランダム化された全ての患者を、たとえ治療を中止したり、服薬遵守しなかったとしても、最初に割り付けられたグループ(治療方針)に基づいて解析する手法。この原則は「一度割り付けたら、常にその群で解析する」ことを意味する )とper-protocol(PP)集団(訳者注:ランダム化比較試験(RCT)において,計画どおりに治療を完了した被検者だけを対象に解析する方法です)の両方で評価されました。ITT集団には、無作為化されたすべての参加者が含まれ、欠落している症状スコアデータは多重代入法を使用して補完されました。PP集団からは、介入を中止した参加者、または非遵守(割り当てられたレジメンへの遵守率が80%未満と定義)を示した参加者が除外されました。2つの治療群間のベースライン特性は、χ2検定またはFisherの正確確率検定を使用して比較されました。血液ルーチンパラメータ、ならびに肝機能および腎機能検査は、両側Wilcoxon順位和検定を使用してグループ間で比較されました。 逆流性疾患質問票スコア、消化器症状評価尺度スコア、BMI、短鎖脂肪酸、神経活性化合物、およびその他の連続変数における群間および群内差は、それぞれ両側マン・ホイットニー検定(対応なし)またはウィルコクソン順位和検定(対応あり)を用いて評価した。P値が0.05未満の場合を統計的に有意とした。 |
| メタゲノム解析およびメタボロミクス解析では、シャノンおよびシンプソンの多様性指数、主座標分析(Bray-Curtis非類似度)、主成分分析、OPLS-DA、Adonis検定、およびプロクルステス分析を計算し、ggplot2、ggpubr、vegan、optparse、およびmixOmicsを含むいくつかのRパッケージを使用して実行しました。連続変数の群間および群内差は、対応のないまたは両側対応のあるWilcoxon順位和検定を使用して評価しました。臨床症状スコア、腸内微生物分類群、および糞便代謝物間の関連性を調べるために、両側Pearson相関分析を実施しました。 |
| 3.結果 |
| 3.1.参加者の人口統計学的特性および研究コホート |
| 合計149名が研究参加資格の評価を受け、うち29名が除外されました。23名は参加基準を満たさなかったため、6名は無作為化前に同意を撤回したためです。残りの120名は書面によるインフォームドコンセントを提供し、ITT集団に登録され、プロバイオティクス群(n = 64)またはプラセボ群(n = 56)に無作為に割り付けられました。12週間の試験期間中に、19名が介入を中止しました。内訳はプロバイオティクス群13名、プラセボ群6名で、主な理由はCOVID-19感染、追跡不能、または自主的な離脱でした。その結果、101名がプロトコルに従って試験を完了し、PP集団はプロバイオティクス群51名、プラセボ群50名となりました(図1b)。 |
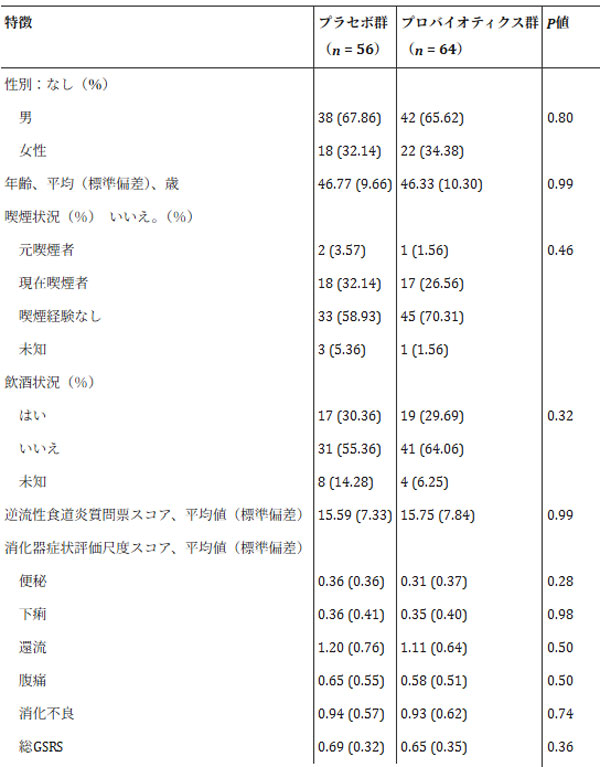
| ITT集団(N = 120)のベースラインの人口統計学的および臨床的特徴を表1にまとめた。年齢と性別は自己申告であり、ランダム化の際に層別化されなかった。プロバイオティクス群とプラセボ群の患者の平均(標準偏差)年齢は、それぞれ46.33(10.30)歳と46.77(9.66)歳であった。プロバイオティクス群とプラセボ群の男性被験者の割合はそれぞれ65.62%と67.86%であり、女性被験者の割合はそれぞれ34.38%と32.14%であった。プロバイオティクス群とプラセボ群の平均(標準偏差)体格指数値は、それぞれ24.38(3.19)と23.93(3.09)であった。プロバイオティクス群とプラセボ群の間で、年齢、BMI、性別分布、アレルギー歴、喫煙・飲酒歴、併存疾患、消化器系薬剤の既往歴などのベースライン特性に統計的に有意な差は認められなかった(P > 0.05)。 |
| 表1. ITT集団の人口統計学的特性およびベースライン特性 |
 |
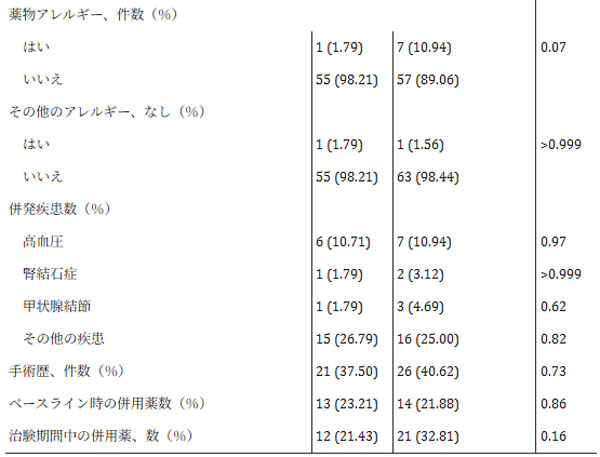 |
| a カテゴリー変数は、適切な場合は ϧ2 検定またはフィッシャーの正確確率検定を使用して比較され、グループ間の有意な差は観察されませんでした。[略語]ITT:intention-to-treat(治療意図) |
| 3.2.プロバイオティクス補給はプロトンポンプ阻害薬中止後の逆流症状の緩和を持続させる |
| ベースライン(0週目)では、逆流性疾患質問票((RDQ))および消化器症状評価尺度(GSRS)スコアにおいてプロバイオティクス群とプラセボ群との間に有意差は認められなかった(P > 0.05、図2;図S1;表S1およびS2)。プロバイオティクスとラベプラゾールの併用療法の8週間の期間中、ITT解析では、逆流性疾患質問票および消化器症状評価尺度スコアはプロバイオティクス群とプラセボ群の両方で有意に低下したことが明らかになった(P < 0.05)。ただし、8週目の逆流性疾患質問票スコアには群間差は認められなかった(4.92 ± 5.70 vs. 5.20 ± 5.87、P > 0.05)。プロバイオティクス群はプラセボ群と比較して胃腸症状の改善が有意に大きく(図2、表S1)、便秘スコアは4週目と8週目でそれぞれ54.05%と43.24%有意に低下し、下痢スコアは8週目で22.58%有意に低下した。プロトコル遵守解析ではこれらの傾向が確認され、4週目と8週目の便秘スコアと8週目の下痢スコアの両方で統計的に有意な低下が認められた(P < 0.05; 図S1、表S2)。 |
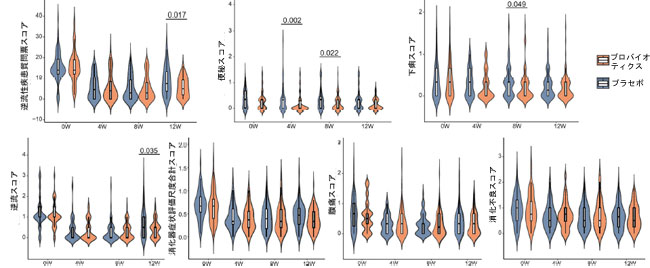 |
| 図2. プロバイオティクス補給は、ITT集団においてプロトンポンプ阻害薬中止後の逆流緩和を持続させる。 ITT集団において、逆流性疾患質問票スコアおよび消化器症状評価尺度合計スコアとサブスコア(便秘、下痢、逆流、腹痛、消化不良)の変化を12週間にわたって評価した。データは、プロバイオティクス(pro; n = 64)群とプラセボ(pla; n = 56)群について、0週(0w)、4週(4w)、8週(8w)、12週(12w)で示されている。各時点における群間差は、両側ウィルコクソン順位和検定を用いて評価し、有意なP値(P < 0.05)を示した。バイオリンプロットでは、ボックスは四分位範囲を表し、中央値は内側の線で示されている。ひげは、四分位範囲の1.5倍以内の最小値と最大値まで伸びている。 |
| ラベプラゾールの投与中止後、続く4週間の追跡調査期間中、プロバイオティクス群の患者は引き続き優れた症状改善を示しました。12週目には、プロバイオティクス群の逆流性疾患質問票スコアは8週目と比較して有意差は認められませんでしたが、プラセボ群は8週目と比較して有意な増加を示し(P < 0.05)、プロバイオティクス群は12週目にプラセボ群と比較して逆流性疾患質問票スコアが36.51%大きく減少しました(5.67 ± 4.59 vs. 8.93 ± 7.10、P = 0.017、図2)。PP解析では、さらに顕著な44.98%の相対的改善が明らかになりました(P = 0.007、図S1)。さらに、プロバイオティクス群は、12週目にプラセボ群と比較して逆流スコアが41.89%減少しました(P = 0.035、図2、表S1)。PP解析では、この改善は逆流および総消化器症状評価尺度スコアの両方の有意な減少を伴い(P < 0.05、図S1、表S2)、症状の持続的な改善を示しました。これらの結果は、プロトンポンプ阻害薬中止後のプロバイオティクス補給の継続が、症状の長期的な緩和をサポートし、早期の再発を防ぐ可能性があることを示唆しています。ITT解析またはPP解析のいずれにおいても、試験全体を通して腹痛、消化不良、またはBMIに群間差は認められませんでした(P > 0.05、図2、図S1)。これは、プロバイオティクス製剤が腸運動関連および逆流特異的症状に選択的な効果をもたらすことを示しています。 |
| 12週目には27名の参加者について内視鏡検査が行われた(図S2)。プロバイオティクス群では、LAグレードAの食道炎患者の割合が73.68%から36.84%に減少し、グレードBの患者の割合は21.05%から15.79%に減少した。一方、プラセボ群では、グレードAは62.50%から50.00%に減少し、グレードBは変化しなかった。各群で1名ずつLAグレードCの患者がいたが、グレードDの症例は認められなかった。内視鏡的治癒率(LAグレード0への改善)はプロバイオティクス群(36.84%)の方がプラセボ群(12.50%)よりも高かったが、統計的に有意な差は認められなかった(P = 0.365)。しかしながら、これらの結果は、特に軽度から中等度の逆流性食道炎において、プロバイオティクスが粘膜回復をサポートする可能性を示唆している。 |
| プロバイオティクス補給は、胃食道逆流症患者において安全かつ忍容性が高いことが示されました。介入前後に、血液、尿、便の一般検査、肝機能および腎機能評価、心電図検査を含む包括的な安全性評価を実施しました。ベースライン時および介入後において、プロバイオティクス群とプラセボ群のいずれにおいても、臨床的に有意な異常は認められませんでした(表S3)。研究期間中に、合計25件の非重篤な有害事象が記録されました(表S4)。報告された事象には、上気道感染症、歯肉炎、下痢、めまい、咽頭痛、腹部膨満感などが含まれます。有害事象の全体的な発生率は、プロバイオティクス群(17件、26.56%)がプラセボ群(8件、14.29%)よりも有意差はありませんでしたが、わずかに高い傾向が見られました(P = 0.10)。プラセボ群の被験者1名に、声帯肉芽腫という重篤な有害事象が1件発生しました。この事象は入院を要しましたが、標準的な医療処置により完全に回復しました。独立した臨床評価の結果、有害事象はいずれもプロバイオティクス製剤または治験手順とは関連がないと判断されました。これらの結果は、多菌種プロバイオティクス混合物の補助的補給が安全であり、全身または消化器系のパラメータに悪影響を及ぼさず、胃食道逆流症患者においてプラセボと同等の安全性レベルを示すことを示しています。 |
| 3.3.プロバイオティクスの併用投与は、胃食道逆流症患者の腸内細菌叢を再構築する |
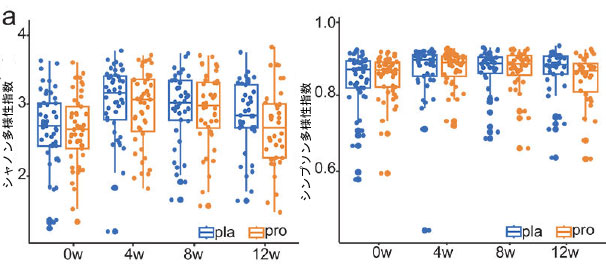
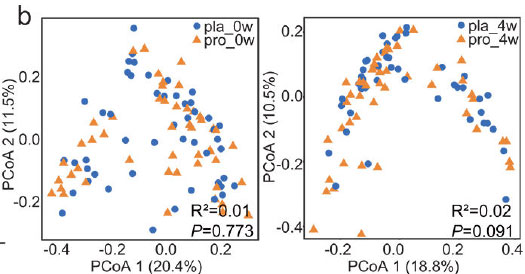
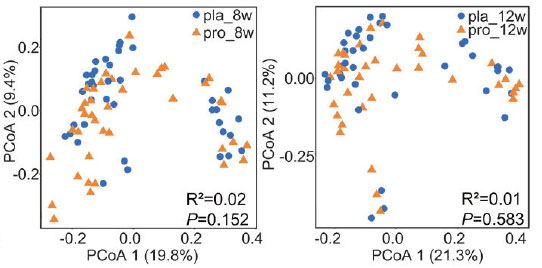
| シャノン指数およびシンプソン指数を用いて評価したα多様性において、プロバイオティクス投与群とプラセボ投与群の間で、いずれの時点においても有意差は認められなかった(P > 0.05;図3a)。同様に、主座標分析(Bray-Curtis非類似度)においても、介入期間を通して両群間で微生物群集の明確なクラスター化は認められなかった(図3b)。これは、プロバイオティクス補給による腸内細菌叢全体の構造的変化は認められなかったことを示している。 |
 |
 |
 |
 |
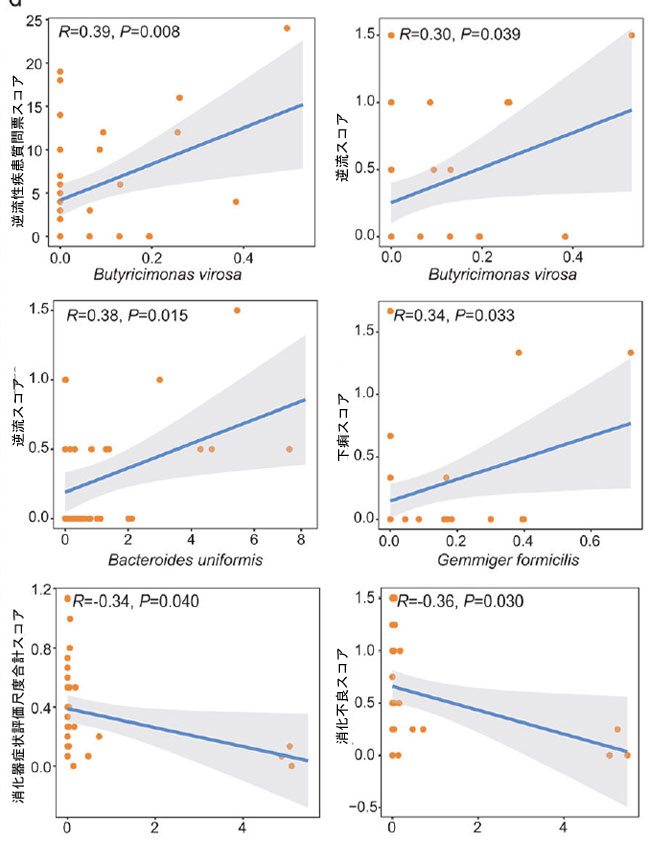 |
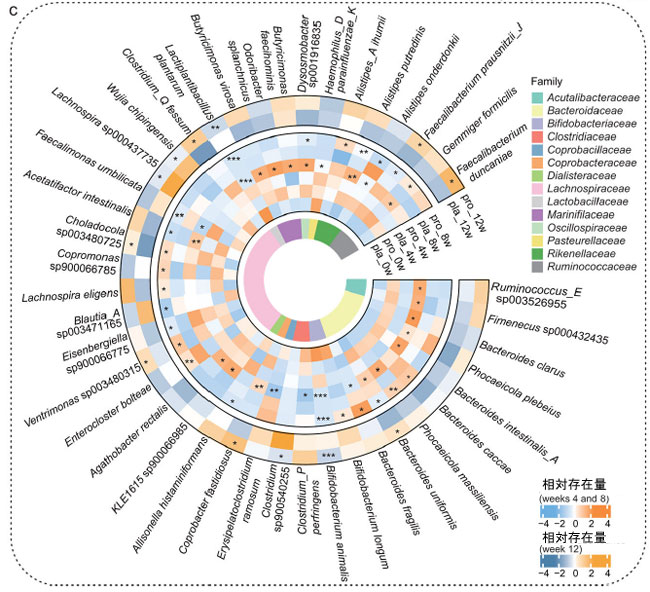
図3.プロバイオティクス補給は、症状緩和と機能的相関のある腸内細菌叢を再構築します。 [略語]pla:プラセボ群、pro:プロバイオティクス群 (a) プロバイオティクス群 (pro; n = 49) とプラセボ群 (pla; n = 49) の 0 週 (0w)、4 週 (4w)、8 週 (8w)、および 12 週 (12w) におけるアルファ多様性 (シャノンおよびシンプソンの多様性指数) を示すボックスプロット。 (b) 腸内細菌叢の主座標分析 (Bray-Curtis 非類似度)。各プロットの右下隅に Adonis テストの結果を示します。 (c) 介入期間中のグループ間 (pro、n = 49; pla、n = 49) で有意に異なる種レベルのゲノムビン (SGB) の相対存在量を示す円形プロット。カラースケールは相対存在量を表し、高い (赤) から低い (青) まであります。統計的差異は、両側ウィルコクソン順位和検定(* P < 0.05、** P < 0.01、*** P < 0.001)を用いて評価した。 (d)プロバイオティクス群における4週目、8週目、12週目のゲノムビンの差次的存在量と臨床症状スコアとの関連性を示すピアソン相関散布図。 |
| 世界的なコミュニティの変化は見られなかったものの、詳細な分析により、介入期間中に平均相対存在量が 0.01% 以上の ゲノムビンが 42 種類あることが明らかになった (表 S5)。これらのゲノムビンのベースラインの不均衡はグループ間で有意に検出されず、介入前の比較可能性が確認された。プロバイオティクスとラベプラゾールの併用療法の 8 週間の段階では、プラセボと比較してプロバイオティクス群で 37 種類のゲノムビン が有意に増加しており、その中には Bifidobacterium animalis、Faecalimonas umbilicata、Lactiplantibacillus plantarum などが含まれる (すべての比較で P ≤ 0.05、図 3c)。これらはすべて、短鎖脂肪酸産生や腸管バリアのサポートなど、有益な代謝活動に関連している。逆に、これまでディスバイオシスや炎症誘発能と関連付けられてきた Gemmiger formicilis や Bacteroides uniformis などの分類群は、その存在量が有意に減少した (すべての比較で P ≤ 0.05、図 3c)。4 週間のプロバイオティクスのみのフェーズ (12 週間目) の後も、いくつかの分類学的変化が持続した。Bifidobacterium animalis、Lactiplantibacillus plantarum、および Clostridium sp900540255 はプロバイオティクス群で増加したが、Bacteroides uniformis および Clostridium Q fessum はプラセボと比較して低いままであった (すべての比較で P ≤ 0.05、図 3c)。これらの結果は、プロバイオティクス補給が、プロトンポンプ阻害薬療法の中止後も、主要な機能分類群の選択的かつ持続的な再構築を誘導することを示唆している。 |
| 微生物動態と臨床転帰との潜在的な関連性を調べるために、ゲノムビンの存在量と症状スコアの間でピアソン相関分析を実施した(図3d)。4週目には、Butyricimonas virosaは逆流性疾患質問票スコア(r = 0.39、P = 0.008)と逆流スコア(r = 0.30、P = 0.039)の両方と有意な正の相関を示した。8週目には、Bacteroides uniformisは逆流の重症度と正の相関を示し(r = 0.38、P = 0.015)、Gemmiger formicilisは下痢スコアと正の相関を示した(r = 0.34、P = 0.033)。 12週目までに、Clostridium sp900540255は総消化器症状評価尺度スコア(r = −0.34、P = 0.040)および消化不良スコア(r = −0.36、P = 0.030)と有意な負の相関を示し、胃腸症状のコントロールにおける保護的役割を示唆した。これらの結果を総合すると、補助的なプロバイオティクス療法は、有益な分類群の標的的な増加と潜在的に有害な分類群の抑制を促進することが示された。特定のゲノムビンと症状改善との間に観察された相関は、胃食道逆流症患者における微生物叢の調節と臨床転帰との間の機能的なつながりを裏付けている。 |
| 3.4.プロバイオティクスの併用投与は胃食道逆流症患者の腸内ファージ群集を調節する |
| 包括的なファージ群集解析により、糞便サンプルから42,554個の非重複ウイルス操作分類単位(vOTU)が同定された。これらのうち33.79%は、12の既知のバクテリオファージ科に分類された。ゲノム品質評価の結果、640個(4.45%)が完全ゲノム、2,289個(15.92%)が高品質ゲノム、11,451個(79.63%)が中品質ゲノムであることが明らかになった(図S3a)。細菌叢における結果と同様に、プロバイオティクス群とプラセボ群の間で、ファージ群集全体のα多様性(シャノン指数およびシンプソン多様性指数)または主座標分析によるβ多様性に、いずれの時点においても有意差は認められなかった(P > 0.05;図S3bおよびc)。さらに、細菌微生物叢のシャノン多様性とファージ群集の間には強い相関関係が観察され(R = 0.888、P < 0.001、図S3d)、細菌宿主とその関連ファージ間の協調的な動態が示唆された。この関係はプロクルステス解析によってさらに検証され、細菌群集とウイルス群集の組成変動に高い一致度が見られ(R = 0.939、P = 0.001、図S3e)、腸内生態系内での緊密に結合した協調的な相互作用が裏付けられた。 |
| 介入全体を通してファージ群集構造は安定しており、10の異なる科から構成され、すべてのサブグループでSiphoviridaeとMyoviridaeが優勢で、これらが腸内ファージ群集の中核を形成していた(図S3f)。注目すべきは、グループ間でファージプロファイルは全体的に非常に類似していたものの、差分存在量解析により、プロバイオティクス補給後に特定のウイルス操作分類単位(vOTU)に有意な変化が見られたことである(すべての場合でP < 0.05、図S3g)。これらの結果は、補助的なプロバイオティクス療法が腸内ウイルス叢を広範囲に再編成するのではなく、特定のバクテリオファージ集団に選択的に影響を与える可能性があることを示している。 |
| 3.5.プロバイオティクス併用投与は、腸内代謝モジュールおよび予測される生物活性代謝物プロファイルを調節する |
| 合計76個の腸内代謝モジュール(GMM)が同定され、そのうち14個の腸内代謝モジュールは、介入期間中にプロバイオティクス群とプラセボ群の間で有意な差を示した(P < 0.05;図S4a)。プロバイオティクスとラベプラゾールの併用療法を4週間行った後、プロバイオティクス群では、プラセボ群と比較して、トリプトファン合成、ヒスタミン分解、ビタミンK2合成II、および酢酸合成Iに関与する微生物経路の存在量が有意に増加した。逆に、γ-アミノ酪酸分解およびビタミンB12生合成Iに関連する経路は、プロバイオティクス群で有意に減少した(いずれの場合もP < 0.05;図S4a)。 8週目までに、プロバイオティクス群では、酢酸、イソ吉草酸、ビタミンK2、B6、B12の合成に関連する経路がさらに増加していることが示された(すべての場合でP < 0.05、図S4a)。12週目には、ロイシン分解経路がプロバイオティクス群で有意に増加したままであり(P = 0.017、図S4a)、神経活性物質、短鎖脂肪酸、アミノ酸関連の微生物代謝能の選択的調節が示唆された。 |
| メタゲノムプロファイルを生物学的に解釈可能な代謝物予測に変換するために、MelonnPan(訳者注:MelonnPanは、マイクロバイオームのシーケンスデータから代謝産物の組成を予測するための計算手法です)ワークフローが適用されました。腸内細菌叢の分類学的構成に基づいて、MelonnPanはすべてのサンプルで80の代謝物を予測しました。非計量多次元尺度構成法では、グループ間で予測された代謝物プロファイルに有意な全体的な分離は見られませんでしたが(図S4b)、対象を絞った調査により、介入中にグループ間で有意な差がある8つの代謝物が特定されました(表S6)。特に、プロバイオティクス群では、4週目にケノデオキシコール酸とフィトスフィンゴシンのレベルが上昇し(それぞれP = 0.019と0.046、図S4c)、続いて8週目にグルタミン酸とシトルリンが増加しました(それぞれP = 0.044と0.020、図S4c)。フィトスフィンゴシンは抗炎症作用と抗菌作用を持ち、主要な胆汁酸であるケノデオキシコール酸は腸管運動と腸内細菌叢の構成に影響を与える可能性がある。グルタミン酸はγ-アミノ酪酸(GABA)合成の前駆体であり、腸管バリア機能に関与する一方、シトルリンは一酸化窒素産生と胃腸運動に関連している。これらの結果は、プロバイオティクス補給が腸内細菌叢の機能的可能性を直接調節し、代謝経路と予測される生物活性代謝物の量の両方を変化させることを示している。 |
| 3.6.プロバイオティクスの併用投与は糞便メタボロームを変化させ、胃食道逆流症患者における微生物と代謝物の相互作用を明らかにする |
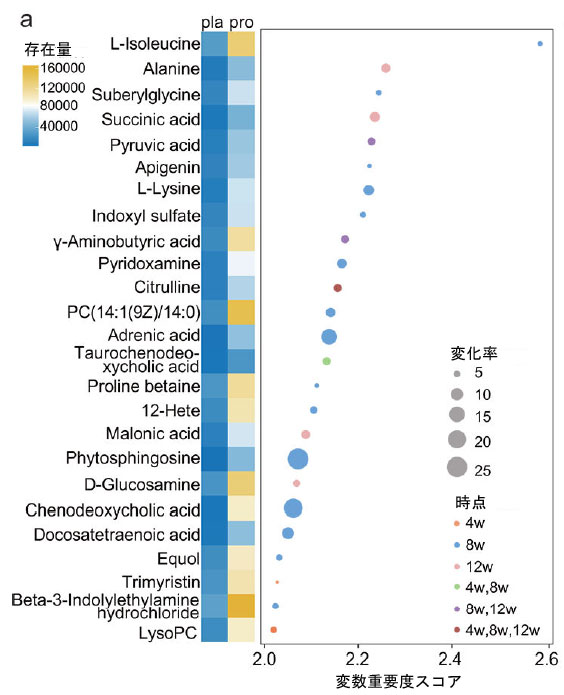
| 次に、介入期間中の糞便メタボローム(訳者注:メタボローム(Metabolome)とは、生体内の細胞や組織に含まれるアミノ酸、糖、有機酸などの低分子代謝物質(メタボライト)の総体です)の変化を解析した。機器の性能と分析の安定性は、品質管理サンプルの主成分分析によって確認された。スコアプロット(図S5a)においてサンプルが密にクラスターを形成したことから、システムドリフトが最小限であり、非標的メタボロミクスワークフローの再現性が高いことが示された。OPLS-DA(訳者注:OPLS-DA(Orthogonal Projections to Latent Structure Discriminant Analysis)は、2つのグループ間の差異を最大化し、関連する特徴量(代謝物など)を明確に抽出する多変量解析手法です)は、複数の時点においてプロバイオティクス群とプラセボ群の代謝プロファイルを効果的に区別した(図S5b)。代謝物レベルの差分解析は、厳密な閾値(投影における変数重要度スコア > 2.0、P < 0.05、フォールドチェンジ > 4または< 0.25)を用いて実施した。このアプローチにより、両群間で有意に異なる25種類の糞便代謝物が同定され、ベースラインに有意差を示すものはなかった(図4a、表S7)。 4週目には、プロバイオティクス群はプラセボ群と比較して、トリミリスチン(抗炎症作用を持つ可能性のあるトリグリセリド)とタウロケノデオキシコール酸(脂質消化と腸内シグナル伝達に関与するタウリン抱合胆汁酸)のレベルが有意に高かった(P < 0.05、図4a)。8週目には、L-イソロイシンやL-リジンを含むいくつかのアミノ酸がプロバイオティクス群で有意に増加しており(P < 0.05、図4aおよびb)、これは微生物によるアミノ酸合成の促進または宿主による利用の減少を反映している。12週間の介入終了時には、トリカルボン酸回路の中間体であり、糖新生と酪酸産生の基質であるコハク酸がプロバイオティクス群で有意に増加していた(P < 0.05、図4aおよびb)。注目すべきことに、シトルリンとγ-アミノ酪酸は、プロバイオティクスとプロトンポンプ阻害薬の併用期とそれに続くプロバイオティクス単独期の両方で一貫して増加しており(P < 0.05、図4b)、酸抑制が中止された後も微生物の代謝活動が持続していることを示唆している。シトルリンは尿素と一酸化窒素合成経路の重要な中間体であり、腸管バリアの完全性と運動性に関連している一方、γ-アミノ酪酸は抗炎症作用と腸-脳軸調節機能を持つ神経活性代謝物である。25の差次的代謝物の経路解析により、いくつかの重要な代謝ネットワークで有意な増加が明らかになった。最も影響を受けた経路には、アラニン、アスパラギン酸、グルタミン酸代謝、アルギニンとプロリン代謝、酪酸代謝、ピルビン酸代謝、解糖/糖新生、クエン酸回路(TCA回路)が含まれる(図4c)。これらの研究結果は、プロバイオティクスの摂取が、エネルギー産生、アミノ酸恒常性、短鎖脂肪酸生合成に関連する微生物代謝の機能的変化を促進することを示している。 |
 |
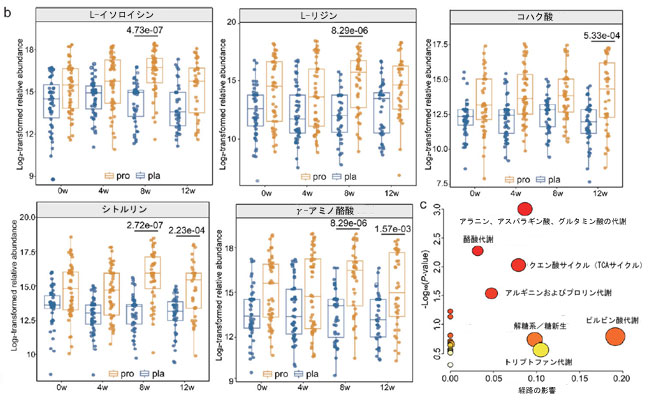 |
図4. プロバイオティクス補給は糞便メタボロームを再構築し、主要な代謝経路を豊かにします。 [略語]Pla:プラセボ群、pro:プロバイオティクス群 (a) 4週目 (4w)、8週目 (8w)、および/または12週目 (12w) におけるプロバイオティクス (pro; n = 51) とプラセボ (pla; n = 50) のグループ間で、糞便代謝物の存在量に差があることを示すヒートマップ (投影における変数重要度スコア > 2.0、P < 0.05、およびフォールドチェンジ > 4 または < 0.25)。円の大きさはフォールドチェンジの大きさを反映し、色は有意なグループ間差が観察された時点を示します。カラースケールは代謝物の存在量レベルを表します。 (b) L-イソロイシン、L-リジン、コハク酸、シトルリン、γ-アミノ酪酸などの、プロバイオティクスに反応する重要な代謝物の相対存在量のボックスプロット。ボックスは四分位範囲を表し、中央値は内側の線で示されます。ひげは、四分位範囲の 1.5 倍以内の最低値と最高値まで伸びています。グループ間の統計的差異は、Benjamini-Hochberg 補正を用いた両側 Wilcoxon 順位和検定を使用して評価しました。 (c) 異なる存在量の糞便代謝物に基づくパスウェイ濃縮分析。円のサイズは濃縮比を表します (円が大きいほど濃縮度が高い)。色は -log10 (P 値) を反映しており、赤は統計的有意性が高いことを示し、黄色は有意性が低いことを示します。 |
| これらの代謝変化の潜在的な微生物要因を調査するために、有意に変化した代謝物と細菌種の間で両側ピアソン相関分析を実施しました(図S5c)。シトルリンは、Bifidobacterium animalis(r = 0.30、P = 0.002)およびBifidobacterium longum(r = 0.40、P < 0.001)と有意な正の相関を示しましたが、γ-アミノ酪酸(GABA)はBifidobacterium animalis(r = 0.30、P = 0.005)およびFaecalimonas umbilicata(r = 0.40、P < 0.001)と正の相関を示しました。さらに、コハク酸はBacteroides fragilis(r = 0.33、P < 0.001)と有意な正の相関を示しました。これらの相関は、特定のプロバイオティクス関連分類群と生物活性代謝物産生との間の協調関係を示唆しています。これらの結果を総合すると、補助的なプロバイオティクス療法は、胃食道逆流症患者の糞便代謝産物の著しい持続的なリモデリングを誘導し、腸の健康、神経調節、およびエネルギー代謝に関連する代謝産物の顕著な増加をもたらすことが示された。 |
| 3.7.プロバイオティクスの併用投与は、神経活性化合物および短鎖脂肪酸の糞便中濃度を調節する |
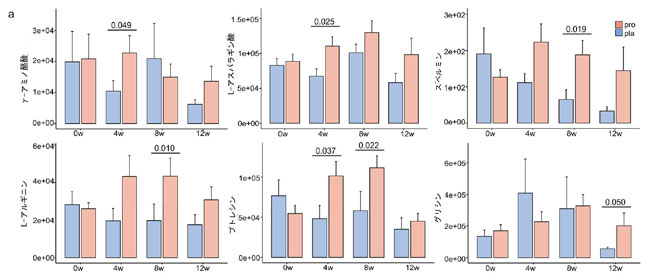
| 標的メタボロミクス解析により、プロバイオティクス補給は、腸-脳軸シグナル伝達およびエネルギー代謝に関連する主要な微生物代謝物の糞便中濃度を著しく変化させることが明らかになった(図5A;表S8)。プラセボ群と比較して、プロバイオティクス群では4週目にγ-アミノ酪酸およびL-アスパラギン酸濃度が有意に上昇し、8週目にはスペルミンおよびL-アルギニン濃度が増加した。特に、プトレシン濃度は4週目と8週目の両方でプロバイオティクス群で有意に高かった(P < 0.05)。一方、グリシン濃度は、プロバイオティクス単独投与期間後の12週目に増加傾向を示した(P = 0.050)。 |
 |
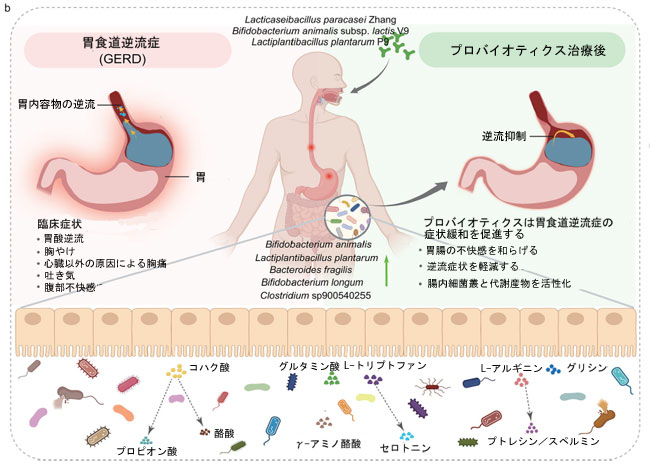 |
図5. 統合されたマルチオミクスフレームワークは、プロバイオティクスの併用投与と胃食道逆流症の症状改善を関連付けます。 (a) プロバイオティクス(pro; n = 51)とプラセボ(pla; n = 50)のグループにおける、0週(0w)、4週(4w)、8週(8w)、12週(12w)での主要糞便代謝物のレベル(任意単位)を示す棒グラフ。エラーバーは平均の標準誤差を表します。統計的有意性は両側ウィルコクソン順位和検定を使用して評価され、有意差(P < 0.05)に達した比較のP値が表示されます。 [略語]pla:プラセボ群、pro:プロビオティクス群 (b)多菌種プロバイオティクス補給の効果をまとめた概念モデル。プロバイオティクスは胃食道逆流症の症状を緩和し、腸内微生物組成を調節し、γ-アミノ酪酸、セロトニン、短鎖脂肪酸などの有益な分類群と代謝物の持続的な増加をサポートし、逆流症状の緩和を継続します。この統合的な枠組みは、微生物の調節と臨床転帰との間の機能的な関連性を示している。 |
| 縦断的なグループ内分析により、12 週間の介入期間中にプロバイオティクス群で動的な代謝変化がさらに明らかになった(表 S8)。8 週目までに、糞便中の酪酸、プロピオン酸、L-ロイシン、L-バリン、プトレシン、メチオニンのレベルがベースライン(0 週目)と比較して有意に増加した(P < 0.05)。セロトニン(5-HT )および微生物インドール誘導体の前駆体である L-トリプトファンは、8 週目に 4 週目よりも有意に高く、酪酸は 12 週目にもベースラインと比較して高いままであった(P < 0.05)。これは、有益な微生物代謝活性の持続的な増強を示している。対照的に、セロトニンレベルは 8 週目と 12 週目にベースラインと比較して有意に低下しており(P < 0.05)、宿主のセロトニン作動性シグナル伝達の潜在的な変化を示唆している。さらに、L-グルタミン、L-トリプトファン、プトレシン、メチオニンなどのいくつかの代謝産物は、8週目と比較して12週目に減少しました(P < 0.05)。これは、フィードバック制御、基質枯渇、またはプロトンポンプ阻害薬中止後の微生物群集の適応を反映している可能性があります。これらの結果を総合すると、プロバイオティクス介入が腸内メタボロームに及ぼす機能的な影響が強調され、微生物活性と宿主に関連する代謝経路が結び付けられ、胃食道逆流症患者で観察された臨床的効果の根底にある可能性が示唆されます。 |
| 4.考察 |
| 過去数十年間で、胃食道逆流症は世界的に蔓延する消化器疾患として認識されるようになってきた(2)。プロトンポンプ阻害薬は強力な酸分泌抑制効果を持つため、胃食道逆流症治療の要となっている。しかし、プロトンポンプ阻害薬の長期使用は、消化器系の副作用、腸管感染症への感受性の増加、および中止後の再発率の高さと関連している(42、43)。本無作為化二重盲検プラセボ対照試験では、胃食道逆流症治療におけるラベプラゾールとの併用療法として、多菌種製剤を用いたプロバイオティクス補助療法の有効性を評価した。 |
| この研究の興味深い発見は、プロバイオティクスの併用投与がプロトンポンプ阻害薬中止後の症状緩和の持続を著しくサポートし、腸内微生物組成と代謝プロファイルの好ましい変化を伴うことである(図5b)。重要なことに、ラベプラゾール中止後の4週間のプロバイオティクス単独投与期間中、逆流性疾患質問票スコアはプラセボ群と比較してプロバイオティクス群で35.21%(ITT)および40.87%(PP)減少しており、プロバイオティクスの継続使用が症状の再発を防ぐのに役立つ可能性を示している。さらに、プロバイオティクス群では逆流および総消化器症状評価尺度スコアの両方で顕著な改善が見られた。これらの結果は、Bifidobacterium bifidum YIT 10347 を 4 週間摂取すると食後の不快感が改善する (44) こと、および加熱殺菌したLactobacillus johnsonii No. 1088 を毎日摂取すると胸やけの症状が軽減する (45) ことを示す以前の報告と一致しています。さらに、マルチオミクスデータは、持続的な逆流緩和に対する強力で直接的な生物学的根拠を提供します。有益な分類群 (Bifidobacterium animalisなど) の有意な増加と、生物活性代謝物との強い相関は、排便習慣の変化とは無関係に、内臓過敏症を軽減し、粘膜の完全性を強化するもっともらしい経路を示しています。たとえば、Bifidobacterium animalisと γ-アミノ酪酸の増加 (r = 0.30、P = 0.005) との相関は重要です。γ-アミノ酪酸は、食道の感受性を調節することが知られている主要な抑制性神経伝達物質です (46)。これは、内視鏡的治癒率の顕著な数値差(36.84% vs. 12.50%、P = 0.365)がプロバイオティクス群に有利であったことと一致しており、この介入が粘膜修復を促進している可能性を示唆している。食道組織自体へのこの効果は、調節されたマイクロバイオームとその代謝産物(例:短鎖脂肪酸、コハク酸)の全身的な抗炎症作用とバリア強化作用の直接的な結果であると考えられる。これらのデータは総合的に、プロバイオティクスを標準的なプロトンポンプ阻害薬療法と統合することで、異なるものの相補的なメカニズムを通じて胃食道逆流症の症状コントロールを強化し、患者の転帰を改善できる治療的可能性を強調している。 |
| プロバイオティクスは、主に腸内細菌叢とその機能出力を調節することによって健康上の利点を発揮します(47)。この研究では、微生物メタゲノム解析により、プロバイオティクス補給により、Bifidobacterium animalis、Lactiplantibacillus plantarum、Bacteroides fragilis、Bifidobacterium longum、Clostridium sp.900540255などの有益な細菌分類群が有意に増加し、Siphoviridae科およびMyoviridae科に関連する特定のウイルス操作分類単位(vOTU)も増加したことが明らかになりました。特に、Bifidobacterium animalis subsp. lactis MH-02は、逆流性食道炎患者の消化器症状評価尺度スコアを低下させ、寛解期間を延長することが示されています(8)。 Lactiplantibacillus plantarum、Bacteroides fragilis、Bifidobacterium longum、Clostridium sp.900540255など、増加した分類群の多くは、特に酪酸と酢酸などの短鎖脂肪酸の産生菌として知られており、腸内恒常性の維持、上皮バリアの完全性の強化、病原性微生物の抑制に重要な役割を果たしている(8、13、48~50)。さらに、我々の研究結果は、プロバイオティクス治療により、非びらん性逆流性疾患や食道がん発生と関連付けられてきた分類群であるBacteroides uniformisとGemmiger formicilisの存在量が有意に減少したことを示している(51~53)。これらの微生物の変化は、プロバイオティクスの臨床的利点が、少なくとも部分的には、腸内生態系をより好ましい回復力のある構成へと再構築することによってもたらされることを示唆している。 |
| 腸内細菌叢由来の代謝産物は、複雑な宿主と微生物の相互作用において重要なシグナル伝達分子である(54)。本研究では、プロバイオティクス介入により、胃酸分泌を刺激し、プロトンポンプ阻害薬と併用することで逆流防止療法の有効性を高めることが知られている代謝産物であるコハク酸が有意に増加した(55)。注目すべきことに、特定の腸内微生物はコハク酸を酢酸と酪酸に変換することができ(56)、これらは両方ともプロバイオティクス群で増加していた。酪酸は結腸細胞の主要なエネルギー源として機能するだけでなく、タイトジャンクションタンパク質の調節を介して腸管バリア機能を強化し、強力な抗炎症作用を発揮し、好酸球性食道炎などの疾患において保護効果を発揮する(57、58)。さらに、プロバイオティクス補給は、腸管運動、免疫機能、内臓感覚を調節するγ-アミノ酪酸(GABA)、セロトニン(5-HT)、L-トリプトファンなどの主要な神経活性代謝産物を調節した(59)。食事性L-トリプトファン補給は胃食道逆流症の症状を緩和することが報告されている(60)。その下流代謝産物であるセロトニンは、胃腸の蠕動運動と運動性の重要な調節因子である(61)。しかし、セロトニンレベルの上昇はタイトジャンクションタンパク質の発現を変化させることで食道上皮バリア機能を阻害し、胃食道逆流症の病因に寄与する可能性がある(62)。興味深いことに、本研究ではプロバイオティクス介入後にL-アルギニン、プトレシン、スペルミンのレベルが上昇することも観察された。L-アルギニンはプロスタグランジンを介した粘膜防御を促進することで逆流性食道炎から保護することが示されており(63、64)、結腸運動性を改善する可能性がある(65)。その下流代謝産物であるプトレシンとスペルミンは、腸上皮細胞の増殖、粘膜修復、腸バリア機能に不可欠である(66、67)。これらの代謝変化を総合すると、プロバイオティクスが消化管の健康に貢献する多面的なメカニズムが明らかになり、その影響は微生物組成にとどまらず、機能的な代謝再プログラミングにまで及ぶことがわかる。 |
| 本研究にはいくつかの限界がある。第一に、研究対象集団は中国人のみで構成されていたため、他の民族や地域集団への結果の一般化可能性が制限される可能性がある。第二に、参加者には通常の食習慣を維持するよう指示したが、食事摂取量は厳密に管理されていなかったため、食事の影響により腸内細菌叢の構成にばらつきが生じる可能性がある。さらに、食道炎患者のうち内視鏡検査を受けたのはわずか27名であった。このサンプルサイズの小ささは、治癒率の評価において偽陰性の結果につながる可能性がある。最後に、主要評価項目については十分な検出力があったものの、サンプルサイズと追跡期間が限られていた。胃食道逆流症管理におけるプロバイオティクスの長期的な効果と持続性を確認するためには、より大規模な多施設共同研究と長期追跡調査が必要である。 |
| 結論として、この無作為化比較試験は、多菌種プロバイオティクス製剤を用いた補助的プロバイオティクス療法が、重篤な有害事象の報告がなく、胃食道逆流症の管理において安全かつ効果的な戦略であることを示しています。この療法は、腸内生態系の標的調節によって、プロトンポンプ阻害薬治療中および治療後も持続的な症状緩和をもたらします。有益な細菌の増加、有害な分類群の抑制、短鎖脂肪酸、γ-アミノ酪酸、コハク酸などの主要な生物活性代謝物の増加は、観察された臨床的効果の多面的なメカニズム的基盤を提供します。これらの機能的変化は、内視鏡的治癒の改善傾向と一致しており、今回の知見の生物学的妥当性を裏付けています。これらの結果は、プロバイオティクスがプロトンポンプ阻害薬療法の貴重な補助療法となる可能性を強調し、多様な集団において症状および内視鏡的効果の両方を確認できる、将来の大規模研究の基盤となります。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、mSystems. 2026 Jan 29;11(2):e01568-25.に掲載されたAdjunctive probiotic therapy sustains symptom relief in gastroesophageal reflux disease through gut microbiome-metabolome remodeling.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |