ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
腸内細菌叢と骨の老化:腸管-X軸モードに焦点を当てて |
Yuan-Wei Zhang et al., |
|
|
| 要約 |
研究が進むにつれ、加齢に伴う様々な臓器間の相互作用が研究のホットスポットとして注目を集めるようになった。骨粗鬆症、変形性関節症、椎間板変性症といった骨老化関連疾患における腸内細菌叢の役割は、これまで幅広く研究されてきた。本レビューではまず、腸内細菌叢と骨粗鬆症、変形性関節症、椎間板変性症との密接な関連性を概説し、次に、神経調節(腸内細菌叢-腸-脳-骨軸)、免疫調節(Th17細胞とTreg細胞のバランス)、内分泌調節(腸由来ホルモンと5-HT)、代謝産物を介した調節(短鎖脂肪酸)、細菌性細胞外小胞、そして微生物ニッチの変化や腸内細菌叢関連バイオマーカーの変化といった、腸管-X軸の潜在的なメカニズムについて考察する。さらに、臨床応用性を高めるために、食事療法、プロバイオティクス、糞便微生物移植、身体活動などの潜在的な介入戦略をまとめました。このレビューでは、「腸-骨軸」、「腸-関節軸」、「腸-椎間板軸」の根底にある共通のパターン化されたメカニズムを探るために、「腸-X軸」という統合的な概念を創造的に提示しました。さらに、この共通のパターンが骨老化関連疾患を制御する潜在的なメカニズムを掘り下げ、この軸に基づいて骨老化に対する治療戦略を将来的に概説します。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2. 腸内細菌叢と骨老化の密接な関連性(腸管-X軸モデルに基づく) |
| 2.1. 骨粗鬆症(腸-骨軸) |
| 2.2. 変形性関節症(腸-関節軸) |
| 2.3. 椎間板変性(腸-椎間板軸) |
| 3. 腸管-X軸モードが骨老化の調節に関与する可能性のあるメカニズム |
| 3.1. 神経調節 |
| 3.2. 免疫調節 |
| 3.3. 内分泌調節 |
| 3.4. 代謝産物による調節 |
| 3.5. 細菌性細胞外小胞と微生物ニッチの変化 |
| 3.6. 腸内細菌叢関連バイオマーカー |
| 4. 腸管-X軸関連経路に基づく健全な骨老化改善のための基礎的アプローチ |
| 4.1. 食事介入 |
| 4.2. プロバイオティクスとプレバイオティクスの補給 |
| 4.3. 糞便微生物叢移植 |
| 4.4. 身体活動 |
| 4.5. 腸内細菌叢関連バイオマーカー |
| 5. 現在の骨老化研究における腸管-X軸モデルの課題と改善の方向性 |
| 6. 結論と展望 |
本文 |
| 1.はじめに |
| 世界的な人口高齢化の進行に伴い、60歳以上の人口は10億人を超え、2050年までに世界人口の約4分の1を占める可能性がある[1]。老化は人間の生命過程における避けられない自然法則であり、個人の遺伝子、生活習慣、外部環境など複数の要因と密接に関連し、体内の複数の臓器や組織の機能低下として現れる[2,3]。中でも、人体の基本構造である骨は、人間の運動システムの重要な構成要素であり、構造的支持、姿勢維持、運動能力といった重要な機能を担うだけでなく、内臓保護、ミネラル貯蔵、代謝調節においても不可欠な役割を果たしている[4,5]。加齢に伴い、骨の老化は人間の健康に影響を与える重要な要因となっており、骨量の減少、骨の微細構造の変化、骨強度の低下、軟骨の変性などの老化の特徴として現れます [6、7、8]。また、骨粗鬆症、骨粗鬆症性骨折、変形性関節症、椎間板変性などの加齢関連疾患の進行にも重要な役割を果たしています [9、10、11、12、13]。 |
| 腸内細菌叢は、腸内に生息する数百兆個の微生物であり、ヒトの遺伝子プールの重要な構成要素である[14]。先天的な違いに加えて、腸内細菌叢の多様性と複雑さは出生後の環境で継続的に変化し、宿主の代謝、内分泌、免疫調節のさまざまな側面に関与し、宿主のさまざまな生理機能と病理機能に影響を与える[15,16]。腸内細菌叢のバランスと安定性は、宿主の健康を維持する上で重要な役割を果たす。加齢、精神的ストレス、不健康な食習慣とライフスタイル、抗生物質の使用など、いくつかの要因が腸内細菌叢の構成、量、多様性に影響を与える可能性がある[16、17、18、19、20、21]。そこでは、宿主の老化プロセスが継続的に進行するにつれて、体内では腸粘膜バリア機能の損傷、免疫機能不全、代謝系障害などが複雑化し、腸疾患(大腸がん、潰瘍性大腸炎、クローン病、過敏性腸症候群など)や腸外疾患(骨老化関連疾患、全身性代謝疾患、免疫系疾患、生殖器系疾患、心血管疾患、泌尿器系疾患、神経変性疾患など)のリスクと重症度が増大する[22、23、24、25、26]。過去の長い研究過程で、この分野の学者は骨老化の原因と制御メカニズムについて一定の理解を得てきたが、骨老化は現在の学術界では依然として困難で避けられない生物学的障壁として認識されている[27,28]。現代の物質的・医学的水準の向上により、骨老化関連疾患のリスクは低減し、人間の寿命はある程度まで延びました。平均寿命の延長に伴い、全人口に占める高齢者の割合は徐々に増加しており、高齢者の健康状態にはさらなる注意が必要です[29,30]。骨老化と腸内細菌叢との関連性および関連する調節メカニズムを理解することは、高齢者の骨の状態をより良く改善することに貢献する可能性があります。 |
| 研究が継続的に深まるにつれて、高齢者の体内のさまざまな臓器間の相互連結相互作用が、近年研究のホットスポットになり続けている[31,32]。骨粗鬆症、変形性関節症、椎間板変性などの骨老化関連疾患における腸内細菌叢の役割が集中的に研究されており、腸-骨軸、腸-関節軸、腸-椎間板軸(まとめて腸-X軸モードとして知られる)などの対応する研究概念が出現している[33、34、35]。これらの軸は、「腸管漏出-炎症-標的組織破壊」というコア経路を共有しており、これは骨老化関連疾患の全身的制御の重要なメカニズムである。こうした状況を踏まえ、新たな研究や最新の文献と合わせて、本レビューでは、腸内細菌叢と骨老化関連疾患との密接な関連性について、腸管-X軸モードに基づく詳細な考察、骨老化の調節に関わる腸管-X軸モードの潜在的なメカニズム、腸管-X軸関連経路に基づく健康な骨老化を改善するための基礎的なアプローチ、および現在の骨老化関連研究における腸管-X軸モードの課題と改善の可能性のある方向性について詳述し、この学術コミュニティにおける既存の知識を要約するとともに、今後の同様の研究のための参考資料を提供する。 |
| 2. 腸内細菌叢と骨老化の密接な関連性(腸管-X軸モデルに基づく) |
| 腸内細菌叢と宿主の免疫系および代謝系との複雑な相互作用は、全身の様々な臓器の機能と特性に影響を与え、腸管-X軸に対する調節効果を構成する可能性がある[36]。この種のクロストークは、宿主、微生物、およびその関連代謝産物間の直接的または間接的な相互作用を介して発生し、標的臓器を標的として調節する[37]。宿主と腸内細菌叢間の調節には、多様な細胞経路、および多段階の多様な微生物種間の多方向的なコミュニケーションが関与している[38,39]。軸のクロスリンク相互作用プロセスでは、さまざまな微生物が胆汁酸、短鎖脂肪酸(SCFA)、コリン、炎症因子、神経伝達物質、小分子、毒性物質などを産生することにより、体の生理的または病理的な代謝プロセスを調節し、それによって人間の健康と病気の発生に大きな影響を及ぼします [40、41、42、43] 。腸と骨格系の間の複雑な相互作用を完全に理解するには、双方向コミュニケーションの観点からその分子メカニズムを示す必要があります [44]。この観点から、腸-X軸のメカニズムの詳細な分析と特性への影響は、骨老化関連疾患の標的介入にとって非常に重要です。ここで、図1は、腸-X軸モードに基づいて腸内細菌叢と骨老化の間の不可分な関連性を示し、表1は、疾患対象、関連する微生物叢、および発見を含む腸-X軸内のコア関係をまとめています。 |
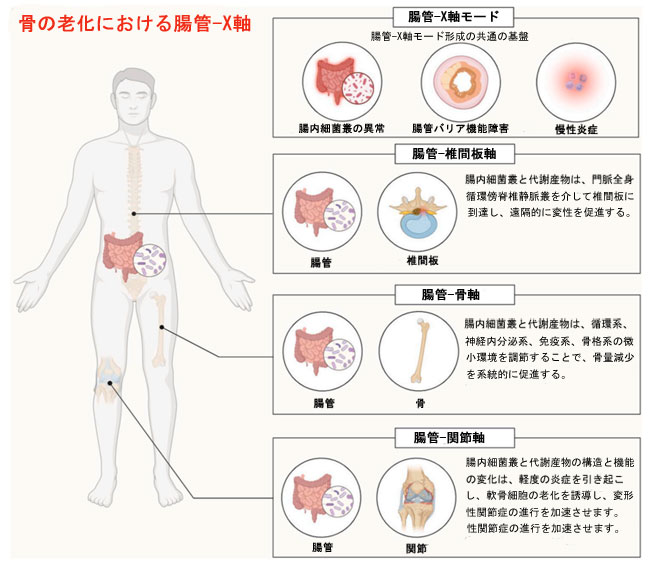 |
| 図1. 腸内細菌叢と骨老化の密接な関連性は、腸管-X軸モデルに基づいて示される。 |
| 表1.腸管-X軸内の主要な関係 |
 |
 |
| 注:OVX、卵巣摘出術;SCFAs、短鎖脂肪酸;TGR5、タケダGタンパク質共役受容体5;BMD、骨密度;OA、変形性関節症;MMP-13、マトリックスメタロプロテアーゼ-13;IVDD、椎間板疾患;IVD、椎間板;ECM、細胞外マトリックス;FMT、糞便微生物叢移植。 |
| 2.1. 骨粗鬆症(腸-骨軸) |
| 骨粗鬆症は、骨量の減少と骨微細構造の破壊を特徴とする全身性の代謝性骨老化関連疾患であり、骨の脆弱性の増大と骨折の発生につながる可能性がある[59,60]。世界的な人口高齢化の深刻化に伴い、骨粗鬆症とその結果生じる脆弱性骨折は、世界的に重要な公衆衛生上の問題となっている[61]。これまでの報告によると、世界中で2億人以上が骨粗鬆症に罹患しており、女性の3分の1、男性の5分の1が生涯に少なくとも一度は脆弱性骨折を経験し、個人、家族、そして公衆衛生システムに大きな負担をかけている[62]。さらに、腸内細菌叢は、人体内の非常に複雑で多様な生態系として、宿主の恒常性調節において極めて重要な役割を果たしている。近年、いくつかの先行研究により、骨粗鬆症患者の腸内細菌叢は健康な人の腸内細菌叢とは異なり、人体の骨量減少の重症度も腸内細菌叢の変化と密接に関連していることが明らかになっている[45,63]。研究の継続的な深化と腸-骨軸の概念の提唱により、骨粗鬆症の発生と進行における腸内細菌叢の調節的役割と重要性は、近年、集団ベースの研究と動物実験の両方で研究のホットスポットとなっている[46,47]。 |
| 腸-骨軸の文脈において、集団ベースの研究の観点から、尾崎ら[48]は、閉経後の日本人女性における腸内細菌叢の構成、骨代謝、および骨折リスクの関連性を調査し、バクテロイデスとリケネラ科が骨量の減少と潜在的な骨折リスクに関連している可能性があり、骨代謝に関する基礎的な微生物叢関連経路のその後の研究が関連する治療アプローチを示唆し、骨粗鬆症の予防と治療を強化する可能性があることを指摘した。Jiら[49]は、骨粗鬆症患者27名、骨減少症患者44名、対照群23名から糞便サンプルを採取し、16S rRNA遺伝子配列解析を用いて腸内微生物群集の構成を評価し、骨粗鬆症および骨減少症の閉経後女性の腸内微生物叢は健康な人と異なる可能性があることを明らかにし、腸内微生物叢と閉経後骨疾患との関連性に関する新たな研究エビデンスを提供した。Liら[50]は、低骨密度(BMD)群および対照群に属する適格者から特定の糞便サンプルを採取し、16S rRNA遺伝子配列解析を行い、低骨密度群では存在量と特定の機能経路が変化したいくつかの分類群を発見し、骨代謝研究分野における微生物叢関連メカニズムの解明に向けた新たなエビデンスを提供した。Zuoら[64]は、中国多民族コホート研究から99,556人の参加者を登録し、広範囲の高度と骨密度の関連性、およびこの関連性における腸内細菌叢の潜在的な調節的役割を調査した。結果は、高地への曝露が成人の骨密度を低下させ、骨粗鬆症のリスクを高める可能性があり、腸内細菌叢の調節が骨密度の低下を緩和する潜在的なアプローチになる可能性があることを示唆した。以前のランダム化比較試験で、Liら[65]は、ラクトバチルス・ロイテリ ATCC PTA 6475の補給が低骨密度の高齢女性の骨量減少を減少させる可能性があることも実証しており、この効果は、L. ロイテリ ATCC PTA 6475の補給が低骨密度の高齢女性の腸内細菌叢と炎症状態の悪化を防ぎ、骨代謝に有益な効果をもたらすためである。これに加えて、Zhaoら[66]は、閉経後骨粗鬆症患者40人をプロバイオティクス群(ビフィドバクテリウム・アニマリス亜種ラクティスProbio-M8、カルシウム、カルシトリオールを投与)とプラセボ群(プラセボ、カルシウム、カルシトリオールを投与)に無作為に割り付け、その結果、従来の薬剤/サプリメントとProbio-M8を併用投与する方が、薬剤/サプリメント単独よりも閉経後骨粗鬆症の管理に効果的であることが示された。Linら[67]は、閉経前および閉経後の中国人女性517人を対象に系統的なマルチオミクス評価を実施し、バクテロイデス・ブルガリスと骨密度の間に負の相関関係を検出した。これは白人アメリカ人でも検証された。これらの知見は、腸内細菌叢とその関連代謝物を変化させることによる骨粗鬆症の予防と治療の基礎を提供した。総合的に見ると、複数の集団ベースの研究によって、腸-骨軸が骨粗鬆症の調節に及ぼす影響と重要性が検証されており、現象の発見から腸-骨軸に基づいた介入の開発へと徐々に移行しつつある。 |
| 動物実験に関しては、Guan ら [46] は、エストロゲン欠乏によりマウスの フィルミクテス門/バクテロイデス門 の割合が増加し、血清リポ多糖 (LPS) が有意に増加する一方、腸内細菌叢の一部を除去すると、卵巣摘出に起因する骨代謝の遺伝的変化を逆転させ、エストロゲン欠乏による骨量減少を改善できることを調査した。正常マウスを卵巣摘出誘発マウスの腸内細菌叢に移植すると骨量減少が生じるが、卵巣摘出誘発マウスを正常マウスの腸内細菌叢に移植すると骨粗鬆症の進行を逆転させることができ、閉経後骨粗鬆症はエストロゲンの直接的な影響だけでなく、腸内細菌叢を介したエストロゲン欠乏によって引き起こされる骨代謝障害でもあることが明らかになった。Zhang ら[68]は、長期にわたる高脂肪食(HFD)が腸管透過性亢進、全身性炎症、腸内細菌叢の不均衡を引き起こし、骨量の減少につながる可能性があることを実証した。また、フラクトオリゴ糖(FOS)とガラクトオリゴ糖(GOS)を継続的に投与することで、高脂肪食を摂取したマウスの腸内細菌叢の生物多様性と短鎖脂肪酸濃度が増加し、腸管透過性亢進と炎症性サイトカインが逆転し、最終的に高脂肪食誘発性骨量減少から保護されることも実証した。さらに、Wangら [69]は、16S rRNAハイスループットシーケンスを用いて骨粗鬆症と正常骨量の閉経後女性の糞便サンプルを検出し、プレボテラ・ヒスティコラがグループ間で有意に発現差のある微生物群集であることを示し、卵巣摘出誘発閉経後骨粗鬆症マウスを作製し、P. ヒスティコラを経口投与した。その結果、P. ヒスティコラの注入はマウスの卵巣摘出誘発骨量減少に有益な効果があり、関連するメカニズムは腸管透過性の向上、腸内細菌叢のディスバイオシスの是正、および炎症性サイトカインの放出の減少に関与していることが明らかになった。一般的に、腸内細菌叢とその関連代謝物が腸-骨軸の文脈において骨の調節に果たす役割を検証し、より深く理解するために、動物実験がますます多く行われており、単純な現象の発見から、より深いメカニズムの解明と介入の探索へと徐々に進化している。腸-骨軸の研究価値と将来的な可能性は、依然として注目に値する。 |
| 2.2. 変形性関節症(腸-関節軸) |
| 変形性関節症は、体の関節に発生する一般的な疾患であり、その主な特徴は、時間の経過とともに関節軟骨が徐々に変性、破壊され、骨増殖が生じることです。その結果、関節痛、こわばり、機能制限が生じ、身体的および精神的な健康状態や生活の質に大きな影響を与えます[70,71]。変形性関節症は世界的に広く蔓延しており、その有病率と発生率は年齢とともに増加します[72]。これまでの報告によると、世界中で40歳以上の成人の22%以上が変形性関節症を患っており、世界中で5億人以上が変形性関節症の影響を受けています[73、74、 75]。最も一般的な関節変性疾患である変形性関節症の病因は解明されておらず、変形性関節症の進行を遅らせる安全かつ効果的な薬剤は存在しない[76]。一方、近年、機械的要因や遺伝的要因に加えて、低度炎症の存在が変形性関節症の病因において重要な役割を果たしており、この種の低度炎症は腸内細菌叢の構成と関連しているらしいという証拠が増えつつある[77,78]。これまでのいくつかの研究では、腸内細菌叢の異常が体内の慢性全身性炎症を引き起こし、それが変形性関節症の重要な病因メカニズムの一つであると示唆されている[78,79]。したがって、変形性関節症の発生と進行における腸-関節軸の役割と潜在的なメカニズムを探求することは、変形性関節症の予防と治療のための新たな方法と方向性を提供するのに役立つ可能性がある。 |
| 腸と関節の軸という観点から、集団ベースの研究に関して、Thompson ら [80] は、440 の糞便メタゲノム (変形性関節症患者 221 人、対照群 219 人) を分析し、変形性関節症における腸内細菌叢の関与を促進するコロニー構造と関連する機能プロセスを記述した。結果は、変形性関節症の発症、進行、重症度において、宿主の遺伝、免疫系、腸内細菌叢の間に相互作用があることを示唆した。これらの人々の腸内細菌叢の約 2% は、炎症性腸疾患に似た異常を示した。血液中の炎症マーカーが増加した個体では、典型的な口腔および炎症性細菌叢の保有が増加し、典型的な腸内細菌叢の存在量が減少しており、腸内細菌叢の構成の変化を示している。炎症特性の部分的な変化は、宿主の生理的および免疫恒常性の変化に対する正のフィードバックである可能性がある。 Wei ら [51] は、前向きで大規模なサンプル、安定した追跡調査による自然集団コホートに基づいて、腸内細菌叢の異常と手の変形性関節症の進行との関連性を調査し、重要な役割を果たす重要な細菌属 (ビロフィラおよび デスルフォビブリオ) と関連する代謝経路 (アミノ酸、炭水化物、および脂質) を特定し、手の変形性関節症の病因をさらに解明するための新しいアイデアと、予防と治療のための新しいターゲットを探索するための理論的根拠を提供しました。これに基づいて、Wei ら[52]は、湘雅変形性関節症研究を探索コホートとして使用し、腸内細菌叢の不均衡によって媒介されるトリプトファン代謝障害と手変形性関節症の発生率との相関関係を特定し、さらに湘雅歩行研究コホートにおける主要なトリプトファン代謝物と手変形性関節症の発生率との関連性、および血清尿酸の重要な役割を検証した[81]。コミュニティベースの研究では、Jiangら[53]は真菌微生物叢と真菌-細菌関連ネットワークと膝滑膜炎との関連性を分析し、真菌微生物叢と真菌-細菌関連ネットワークの変化が膝滑膜炎に関連していることを示し、膝滑膜炎における腸-関節軸のメカニズムの理解と潜在的な標的の示唆に貢献した。Chenら[54]は、関節炎患者の腸内ウイルス叢の特徴を検出し、変形性関節炎および痛風性関節炎患者の腸内ウイルス叢におけるウイルスの多様性と分類の明確な変化を強調し、関節炎の病因と治療アプローチに関する独自の洞察を提供した。一般的に、より大規模な前向きコホートの確立とより精密な臨床介入の開発により、変形性関節炎における腸-関節軸の理解は絶えず拡大している[82]。 |
| 動物実験では、Guan ら [55] は、抗生物質による腸内細菌叢の除去がマウスの血清炎症レベルを低下させ、変形性関節症の進行を遅らせることを示した。雌マウスと比較して、雄マウスでは腸内細菌叢の除去後に軟骨下骨の骨梁厚と骨棘スコアが有意に増加し、腸と関節の軸の理解に貢献し、変形性関節症、性別、腸内細菌叢の関連性を明らかにした。Schlupp ら [56] は、C57BL6/J マウスに異性腸内細菌叢移植の有無にかかわらず内側半月板手術の不安定化を介して変形性関節症を誘発し、マウスの腸内細菌叢の性差が変形性関節症の結果と関連しており、異性腸内細菌叢移植によって可逆的であり、血清サイトカインの変化と関連していることを示した。 Mi ら [83] は、腸管バリアと糞便メタボロミクスを調節することにより、外傷後変形性関節炎マウスにおけるプレバイオティクスの保護効果を評価し、プレバイオティクスによって軟骨変性、骨棘形成、および腸炎症が有意に減少したことを指摘した。Hahn ら [84] は、通常のマウスと無菌マウスにおける関節損傷に対する初期反応を比較し、腸内細菌叢が、おそらく自然免疫系の調節を介して、関節外傷後の急性期の過程における外傷後変形性関節炎の進行を促進する可能性があることを調査した。Mendez ら[85]は、外傷後変形性関節症のリスクに影響を与える可能性のある外的要因を損傷前に評価し、抗生物質治療によって引き起こされる損傷時の炎症状態の減少とWntシグナル伝達調節タンパク質Rspo1の発現の低下が、外傷後変形性関節症の転帰を最適化できることを明らかにした。Schottら[86]は、以前の研究で腸内細菌叢の転座が関節の炎症と変性に影響を与える可能性があることを示し、フルクトオリゴ糖が炎症を抑制し、肥満が腸内細菌叢に与える影響を逆転させることで変形性関節症を効果的に逆転させることができることを示した。Yangら[87]は、GLP-1を介した腸関節軸が腸管FXRシグナル伝達を標的とする新しい変形性関節症治療を発見した。この研究では、以下の3つの主要な発見とブレークスルーが得られました。1) 主要代謝物の同定:標的メタボロミクスにより、変形性関節症患者では胆汁酸グリココール酸(GUDCA)のレベルが有意に低下していることが明らかになりました。胆汁酸グリココール酸を補給すると、胆汁酸受容体FXRを阻害することにより、マウスの変形性関節症の進行が効果的に軽減されました。2) 新規の「腸-関節軸」メカニズムの解明:胆汁酸グリココール酸は腸管FXRを阻害することにより腸管幹細胞の増殖を促進し、GLP-1陽性L細胞数を増加させ、それによって血清GLP-1レベルを上昇させます。GLP-1は関節内のGLP-1Rに作用することにより軟骨保護効果を発揮します。3) 微生物-代謝物-薬剤の相乗効果の確立:変形性関節症患者の腸管におけるC. bolteaeの減少は、胆汁酸グリココール酸レベルと正の相関関係があります。この細菌を再導入したり、その代謝前駆体であるウルソデオキシコール酸(UDCA、市販薬)を補給したりすると、マウスの変形性関節症の進行が遅くなります。臨床データ分析では、ウルソデオキシコール酸の使用がヒトの変形性関節症患者における関節置換術のリスク低下と相関することがさらに確認されています。要約すると、腸管関節軸の研究と、変形性関節症の潜在的なメカニズムと介入を探るためのその応用に関する研究は現在進行中であり、この分野における研究の深さと幅をさらに拡大していくことが依然として必要です。 |
| 2.3. 椎間板変性(腸-椎間板軸) |
| 高齢化の進展に伴い、脊椎変性疾患の患者数は増加傾向にある[88]。脊椎変性疾患の危険因子としては、主に加齢、重労働、外傷、遺伝、肥満、メタボリックシンドロームなどが挙げられる[89,90]。脊椎変性疾患による持続的な疼痛や麻痺は、患者の生活や仕事に支障をきたす主要な問題となっており、患者本人、家族、そして社会全体に大きな経済的負担をもたらしている[91,92]。脊椎構造の進行性変性は、生体力学的損傷やストレスだけでなく、生化学的ストレス因子にも起因しており、これらは脊椎構造内の細胞や組織の正常な活動に悪影響を及ぼす可能性がある[93]。生体力学的因子と生化学的因子の複雑な相互作用が、椎間板変性の病態生理を引き起こす。椎間板は一般的に体内で最大の無血管構造と考えられており、変性椎間板疾患では血管の侵入が認められることがある[94]。これに関して、椎間板変性は多因子性であるが、慢性的な制御不能な低度炎症がその病因と関連していることが徐々に明らかになってきている[95]。血液-椎間板バリアの存在により、椎間板は免疫特権を有し、全身感染から保護されているが、これは免疫系による椎間板内の免疫監視も妨げている[96]。椎間板内の酸素不足と免疫監視の欠如は、変性椎間板内で嫌気性微生物叢が増殖するのに理想的な条件を作り出す[97,98]。椎間板内で増殖する微生物叢は、炎症因子を放出することでより多くの炎症細胞を動員することができる[99]。したがって、損傷した椎間板は、体液性免疫および細胞性免疫を回避する微生物の増殖や、有害な微生物代謝物の拡散にとって理想的な場所となる可能性がある[100]。腸内細菌叢の異常は、腸内細菌叢とその代謝物が血流や椎間板に移行し、椎間板変性を引き起こしたり悪化させたりする可能性がある。このことから、腸-椎間板軸の概念も浮上しており、これは椎間板変性や腰痛において重要な役割を果たす可能性がある。 |
| 腸-椎間板軸の文脈において、Zheng ら [101] は、腸内細菌叢と椎間板変性の因果関係、およびメンデルランダム化による潜在的な細菌特性の存在を調査し、腸内細菌叢と椎間板変性の因果的影響を明らかにし、現在の研究の文脈で潜在的な作用機序を解明した。Fang ら [102] は、腸内細菌叢とその代謝経路と腰痛、坐骨神経痛、椎間板変性のリスクとの因果関係を評価し、一部の微生物分類群とその代謝経路がそれらと因果関係があり、潜在的な介入標的となる可能性があることを示唆した。Wang ら[57]は、三必湯が腸内細菌叢と血清代謝恒常性を広範囲に調節し、炎症反応を減少させ、細胞外マトリックスの分解を抑制し、椎間板の高さと水分含有量を改善して、椎間板変性に対する明らかな治療効果が得られることを調査した。Wangら[103]は、強金荘曲風混合物が髄核細胞における細胞外マトリックスの合成と分解の平衡を維持することにより、椎間板変性に対する遅延効果を示すことを指摘した。これらの効果は、NOD様受容体ファミリーピリンドメイン含有3(NLRP3)インフラマソーム発現の抑制効果、腸内細菌叢の不均衡の改善、脂質代謝と密接に絡み合う乱れた代謝経路(腸内細菌科とクロストリジウム)の調節効果に大きく関与している。Yaoら[58]は、糞便微生物移植が椎間板の細胞安定性の管理と組織病理学的損傷の緩和にプラスの効果があり、椎間板変性ラットの腸内微生物叢の多様性と豊富さに影響を与え、糞便微生物移植は椎間板変性の改善のための有望な標的となる可能性があることを示した。一般的に、腸内微生物叢のディスバイオシスによって引き起こされる菌血症と慢性低レベル炎症は、脊椎構造に悪影響を及ぼし、椎間板変性の発生と進行を促進する可能性があり、椎間板変性は世界的に蔓延しているため、症状を軽減し、椎間板変性の進行を阻止するための効果的な疾患修飾治療アプローチが緊急に必要とされている。この点において、腸-椎間板軸の観点は、椎間板変性の病因と治療に関する新たな見解を提供する可能性がある。 |
| 3. 腸管-X軸モードが骨老化の調節に関与する可能性のあるメカニズム |
| 骨は常に変化し続ける動的な器官であり、骨形成と骨吸収のプロセスは身体の老化過程で継続的に起こります。これらは骨老化に密接に関連する主要な活動であり、ヒト骨格系の様々な生理的および病理的プロセスに関与しています[104,105]。骨リモデリングサイクルの順序は、破骨細胞による骨吸収から始まり、続いて骨芽細胞による骨形成が行われます[106]。このプロセスは、骨髄間葉系幹細胞の継続的な供給による骨芽細胞の分化に依存しています[107]。骨組織において、骨髄間葉系幹細胞は自己複製能力と、脂肪細胞、骨芽細胞、軟骨細胞など複数の系統に分化する能力を示すことができます[108,109]。骨芽細胞は、骨を置き換えて骨吸収後に類骨関節を石灰化するために有機骨基質タンパク質を合成および沈着させ、それによって骨形成と骨吸収のバランスを調節します[110,111]。一般的に、骨代謝バランスは、カルシウムやリンなどのミネラルの代謝バランス、骨密度、骨強度の維持に重要かつ肯定的な役割を果たしていることが認められています[112,113]。骨代謝の不均衡は、骨軟化症、骨粗鬆症、変形性関節症などのさまざまな代謝性骨老化関連疾患につながる可能性があります。免疫機能、炎症反応、体内のホルモンレベルなどの複数の要因が骨代謝に影響を与える可能性があります[114,115]。腸-関節軸では、腸内細菌叢によって産生される炎症性メディエーターが血流を介して関節に到達し、軟骨細胞と滑膜細胞を直接刺激します。このプロセスにより、マトリックスメタロプロテアーゼ(MMP)やトロンボスポンジンモチーフを有するディスインテグリンおよびメタロプロテアーゼ(ADAMTS)などの分解酵素の発現が上方制御されると同時に、コラーゲンIIとアグリカンの合成が抑制されます。腸-椎間板軸では、腸内細菌叢の異常によって引き起こされる炎症性メディエーターが主に髄核細胞の合成-分解バランスを崩し、細胞外マトリックスの進行性分解を引き起こします。腸内細菌叢に関する関連研究が深まるにつれて、腸内細菌叢と骨老化関連疾患との関連性も継続的に研究され、腸-X軸モードの深層研究へと発展してきました。図2は、骨老化の調節に関与する腸管-X軸モードの関連メカニズムを示しています。 |
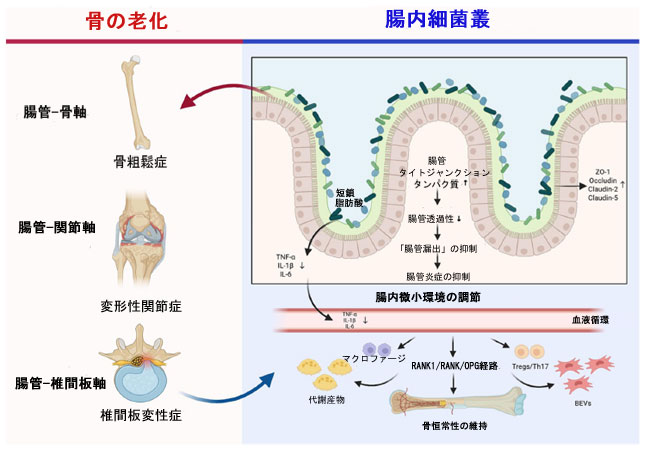 |
図2. 骨老化の調節に関与する腸管-X軸モードの関連メカニズム。 注:SCFAs、短鎖脂肪酸;TNF-α、腫瘍壊死因子アルファ;IL-1β、インターロイキン-1β;IL-6、インターロイキン-6;RANKL、核内κBリガンド受容体活性化因子;RANK、核内κB受容体活性化因子;OPG、オステオプロテゲリン;BEVs、細菌細胞外小胞;ZO-1、ゾヌラオクルデンス-1;Treg、制御性T細胞;Th 17、Tヘルパー細胞17。 |
| 3.1. 神経調節 |
| 中枢神経系は腸機能の調節において中心的な役割を果たしており、腸内細菌叢は、宿主の腸と脳の活動を統合する腸内細菌叢-腸-脳軸として知られる、中枢神経系のボトムアップ型双方向神経体液性コミュニケーションシステムにおいて重要な役割を担っている[116]。骨代謝は神経系の影響を受け、神経ペプチドを分泌する神経線維は代謝活性の高い骨に豊富に存在することが分析されており、自律神経線維は骨膜、フォルクマン管、骨髄、成長板の骨軟骨接合部、滑膜の付着血管などで検出されている[117]。一方、骨は機械的刺激を感知できる組織として、張力、圧力、位置知覚などの信号を細胞の生化学的応答へとさらに処理することができる[118,119]。一方、骨は常にリモデリングされる活動的な組織であり、神経関連分子は正常な骨代謝において栄養的な役割を果たしており、その中にはグルタミン酸、カルシトニン遺伝子関連タンパク質、サブスタンスP、血管作動性腸ペプチドなどが含まれる神経ペプチド候補がある[120]。中枢神経系と腸内細菌叢は、脳と腸の間で情報を伝達するメディエーターとして、アセチルコリン、γ-アミノ酪酸、5-ヒドロキシトリプタミンなどの化学信号を使用している[97,121,122]。この点に関して、これまでの研究では、ラクトコッカス属、ミクソバクテリア属、ラクトバチルス属、およびビフィズス菌がレプチン濃度と正の相関関係にあることが指摘されている[123]。レプチン濃度は、クロストリジウム、プレボテラおよびアロパスツレラと負の相関関係にある[124]。脳幹ニューロンに発現するレプチン受容体に結合した後、レプチンは脳幹ニューロンにおけるセロトニンの放出と視床下部腹内側核におけるセロトニン受容体2Cの発現を抑制し、骨芽細胞に発現するβ2アドレナリン受容体を介して骨吸収を促進する[125]。一方、レプチンの濃度が低下すると、5-ヒドロキシトリプタミンの放出により交感神経系の活動が低下し、骨代謝のバランスに影響を与え、骨老化関連疾患の一因となる。 |
| 脳信号と腸信号は、単一または統合された形態を介して直接的または間接的に骨に作用し、骨細胞、特に破骨細胞の活動と量に影響を与えたり、骨筋単位を調節したり、皮質骨の質を低下させたり、海綿骨の数を減少させたり、骨密度の低下を引き起こしたり、骨老化関連疾患を誘発したりする可能性があります[126,127]。脳卒中または脳虚血の患者における以前の低外傷骨折リスク評価では、健康な対照群と比較して骨折リスクが4倍増加することが示されており、その根本的なメカニズムは、骨代謝に不可欠な神経栄養因子の欠乏、それに続く骨不使用萎縮または中枢神経系の機能不全である可能性があります[128]。Yatsonskyら[129]は、腸内細菌叢の異常が体内のカルシウム輸送障害、T細胞応答の増強、サイトカインの作用による全身性炎症の活性化につながり、それによって破骨細胞の活性化と骨吸収を誘発する可能性があると示唆した。したがって、中枢神経系と腸内細菌叢は化学信号を媒体として脳と腸の間で情報を伝達し、神経調節の役割を織り合わせている。しかし、既存の研究にはまだいくつかの限界がある。特定の微生物はセロトニンなどの中枢神経伝達物質のレベルに影響を与えることができ、これらの神経伝達物質は骨代謝を調節することができるが、特定の微生物またはその代謝物が神経回路を介して骨細胞を精密に調節する方法は不明である。メカニズムレベルでは、腸内細菌叢が神経経路を介して骨代謝に影響を与える因果関係を確立するために、無菌動物モデル、特定の菌株の定着、および選択的神経経路遺伝学を統合した研究が必要である。臨床応用レベルでは、神経変性疾患または精神疾患患者における腸内細菌叢の変化、血清神経活性分子レベル、および骨代謝マーカー/骨折リスクの時間的関連性を分析するために、前向きコホート研究を実施すべきである。これらのヒトを対象とした研究は、相関分析からメカニズム主導型の臨床応用へと研究分野を前進させるだろう。 |
| 3.2. 免疫調節 |
| 腸内細菌叢の変化は、腸管内で局所的または全身的に免疫応答を引き起こす可能性があり、腸内細菌叢の異常状態は、骨代謝に関連するいくつかのサイトカインの増加につながる可能性がある[130]。腸内細菌叢は免疫細胞と相互作用し、自然免疫および獲得免疫プロセスに関与する特定のシグナル伝達経路を調節することが確認されている[131]。これまでの研究では、腸内細菌叢はTヘルパー細胞17(Th17)と制御性T細胞(Treg)のバランスと密接に関連していることが明らかになっており、腸内細菌叢がTh17とTreg間の免疫不均衡を引き起こす可能性があることが示されている[132,133]。Th17とTregは、同じ前駆細胞に由来する、機能的に相反する2つの重要なリンパ球サブセットであり、その分化には形質転換成長因子β(TGF-β)の調節に関与するシグナル伝達経路が必要である[134]。さらに、Th17とTregは骨恒常性、特に破骨細胞分化の維持に不可欠です。研究により、Tregによるインターロイキン(IL)-17の発現低下が破骨細胞分化と骨吸収を阻害する一方、Th17は核内κBリガンド受容体活性化因子(RANKL)経路を介して破骨細胞を活性化し、破骨細胞分化を促進することが明らかになっています[135,136]。さらに、TregはIL-10を介して破骨細胞前駆細胞に結合するか、細胞傷害性Tリンパ球関連タンパク質4(CTLA4)を介して破骨細胞分化と活性を阻害し、骨量減少を抑制します[137]。成熟したTh17と関連する炎症因子IL-17は、骨老化関連疾患の病態形成における主要な推進力です。主に、IL-17はRANKL(訳者注:RANKL(Receptor Activator of Nuclear Factor-κB Ligand)は、骨芽細胞や骨細胞が発現するタンパク質で、破骨細胞(骨を溶かす細胞)の分化・成熟を促進し、骨吸収を誘導する主要な因子です。骨代謝の恒常性維持に不可欠であり、RANKLの過剰な働きを阻害する薬(デノスマブなど)は、骨粗鬆症や関節リウマチの治療に用いられています)とその受容体RANKの発現を著しく上方制御し、破骨細胞の活性を高め、骨代謝バランスを崩し、骨老化関連疾患を引き起こす可能性がある[137,138]。さらに、TregとTh17のバランスは骨量の維持に重要な役割を果たしており、ラクトバチルス・アシドフィルスとクロストリジウム・ディフィシルはTregとTh17のバランスを調節することで、マウスの卵巣摘出誘発性骨量減少を抑制することも実証されている[139]。また、コンニャクオリゴ糖はTregとTh17のバランスを調節し、炎症性サイトカインのレベルを低下させ、抗炎症性サイトカインのレベルを高めることで、骨老化関連疾患の発生と進行に関与している[140]。上記の研究は、腸内細菌叢を介したTreg/Th17バランスが骨代謝に調節効果を及ぼす可能性があることを示唆している。しかしながら、腸管-免疫-骨格軸を直接的に結びつける因果関係の証拠は限られており、一部の研究は依然として推測的な関係にとどまっています。したがって、これらの知見を検証するためには、より詳細なメカニズム研究が必要です。総合的に見ると、腸内細菌叢はTh17とTreg間の動的平衡を調節することで骨代謝に大きな影響を与えます。腸内細菌叢のバランスが崩れると、IL-17を介した炎症促進反応が引き起こされ、RANKL/RANK経路(訳者注:RANKL/RANK経路は、骨芽細胞や骨細胞が発現するRANKLが、破骨細胞前駆細胞の受容体RANKに結合し、破骨細胞の分化・成熟・生存を促進して骨吸収(骨破壊)を誘導する、骨代謝の根幹となるシグナル経路です。この経路は骨の恒常性維持に不可欠であり、癌の骨転移や骨粗鬆症の病態において過剰に活性化し、骨破壊を引き起こします)が活性化され、骨吸収が促進されます。逆に、健康な腸内細菌叢や特定のプレバイオティクスは、Tregの抑制機能を維持し、骨量を保護するのに役立ちます。これは、腸内細菌叢の異常と骨老化関連疾患を結びつける中核的な免疫学的架け橋を明らかにし、腸を調節する食事療法やプロバイオティクス介入による骨の健康を標的とするための重要な理論的根拠を提供します。 |
| 3.3. 内分泌調節 |
| 腸内細菌叢は、体内の仮想的な内分泌器官として、内分泌系と相互作用し、骨老化関連疾患に影響を与える可能性があります。関連ホルモンの欠乏は、骨量減少の促進や骨形成への影響につながる可能性があります[141]。グルコース依存性インスリン分泌刺激ポリペプチド(GIP)は腸管から分泌され、グルコース依存的にインスリン分泌を促進します[142]。GIPは、GLP-1やGLP-2と同様に、内分泌調節の一環として骨老化に影響を与える腸管由来ホルモンです[143]。骨代謝への影響は主に特定の受容体に依存し、骨芽細胞と破骨細胞の増殖とアポトーシスに影響を与えることで骨恒常性を維持します[144]。GIPとGLP-1は骨吸収と骨形成を双方向に調節できますが、GLP-2は一般的に骨形成には影響を与えず、骨吸収のみに影響を与えます[145]。そこでは、体がさまざまな経路でグルコースを摂取すると、十二指腸のK細胞が感知してGIPを分泌し、血流中に放出され、GIPは骨細胞上のGIP受容体(GIPR)に作用する可能性がある[146]。研究によると、GIPはカルシウムイオンの骨組織への流入と、血中カルシウムから骨カルシウムへの変換を促進する可能性がある[147,148]。さらに、セロトニン(5-HT)のシグナル伝達系は、骨の発達と維持において重要な調節的役割を果たしていると考えられており、末梢腸管セロトニンは骨形成を減少させ、中枢脳由来のセロトニンは骨形成を促進し、骨吸収を阻害する[149]。これまでの研究では、腸管セロトニンは、骨の転写因子フォークヘッドボックスタンパク質O1(FOXO1)と転写活性化因子に作用して、骨芽細胞の増殖を阻害し、骨形成を減少させることが明らかになっている[150]。また、脂肪細胞からのレプチン放出は、脳幹核のセロトニン産生ニューロンの合成と興奮性を低下させ、それによって中枢セロトニンによる骨量増加効果を阻害することが示されています。そのメカニズムは、低密度リポタンパク質受容体関連タンパク質5(LRP5)およびFOXO1に関連している可能性があります[151]。LRP5によるトリプトファン水酸化酵素1(TPH1)の調節により、末梢循環中の5-HTが変化し、それによって骨量に影響を与える可能性があります[152]。総合すると、セロトニンはさまざまなメカニズムを介して骨に影響を与え、腸管および脳由来のセロトニンの割合と含有量を変化させることは、骨の老化関連疾患の改善に重要な意味を持つ可能性があります。腸管は、GIP、GLP-1、GLP-2、セロトニンなど複数のホルモンを分泌することで、骨代謝バランスを系統的に調節する、いわば内分泌器官として機能します。これらの腸管ホルモンは、骨芽細胞と破骨細胞上の特定の受容体に作用することで、骨形成と骨吸収に直接影響を与えます。特に注目すべきは、異なる供給源由来のセロトニンが骨量に対して相反する調節効果を示すことです。これは、骨老化における腸管内分泌機能の重要な役割を明らかにし、腸管ホルモン軸を調節することで骨老化関連疾患の予防と治療を行うための重要な理論的根拠となります。 |
| 3.4. 代謝産物による調節 |
| 体内の代謝過程において、腸内細菌叢は短鎖脂肪酸、二次胆汁酸、トリメチルアミン-N-オキシド(TMAO)、インドール誘導体、ポリアミンなど、様々な活性物質を産生する[153,154]。これらの代謝産物は腸管から全身循環へと拡散し、代謝を調節する。まず、短鎖脂肪酸は炭素数1~6の飽和脂肪酸の一種であり、腸内細菌叢によって難消化性炭水化物(酢酸、プロピオン酸、酪酸など)から代謝される[155]。プロピオン酸と酢酸は主に肝臓で吸収され、グルコース産生の主要な供給源となる[156]。閉経前および閉経後の女性を対象としたヒトの研究では、バクテロイデス・ブルガリスと骨密度の間に負の相関関係が見られ、血清吉草酸は微生物群集由来の代謝産物であり、骨密度と正の相関関係があり、バクテロイデス・ブルガリスによって下方制御されることがわかった[157]。酪酸は重要なエネルギー源として、腸内のホルモンレベルを調節し、インスリン感受性を改善し、プロピオン酸とともに腸-脳軸を介して腸の糖新生を促進し、脂肪酸酸化を刺激し、肥満とインスリン抵抗性を抑制し、腸内恒常性を維持することができる[158]。グルコース代謝は、骨芽細胞と破骨細胞の分化と形成のためのエネルギー源を提供する。エネルギー代謝が異常になると、骨芽細胞前駆細胞は骨芽細胞分化から脂肪細胞分化に変化し、さまざまな深層メカニズムを介して骨老化関連疾患を引き起こす可能性がある[159]。さらに、プロピオン酸と酪酸は破骨細胞の代謝的再結合を誘導し、TNF受容体関連因子6(TRAF6)や活性化T細胞核因子細胞質1(NFATc1)などの破骨細胞遺伝子を減少させ、それによって破骨細胞の分化と骨吸収を阻害する[160]。短鎖脂肪酸はGタンパク質共役受容体(GPCR)を活性化することによって破骨細胞の形成を阻害するか、ヒストン脱アセチル化酵素(HDAC)を介して骨吸収を抑制し、一時的に骨吸収を促進する可能性がある[161]。第二に、トリメチルアミン-N-オキシドは食事性コリンの腸内細菌叢依存性代謝物である。これまでの研究では、トリメチルアミン-N-オキシドが炎症反応を活性化しNF-κBシグナル伝達経路を上方制御することにより、骨髄間葉系幹細胞(BMSC)の増殖を抑制し、骨芽細胞への分化を阻害し、骨代謝の不均衡を引き起こし、骨老化関連疾患を誘発することが示されている[162]。第三に、一次胆汁酸は肝臓で胆汁酸塩を生成し、それが小腸に分泌され、腸内細菌叢によって代謝されて二次胆汁酸を生成する。腸内細菌叢は一次胆汁酸の数と種類を変化させ、その結果、代謝効果が変化し、胆汁酸の代謝に影響を与える可能性がある[163]。さらに、二次胆汁酸はビタミンD受容体のリガンドとして作用し、1,25-ジヒドロキシビタミンD3の代謝を調節し、骨恒常性とミネラルバランスの維持に重要な役割を果たし、骨老化関連疾患に影響を与える可能性がある[164]。第四に、インドール誘導体は抗菌ペプチド、ムチンタンパク質の産生、腸絨毛細胞の増殖を刺激し、病原体の異常増殖を抑制し、腸粘膜の完全性を維持することができる[165]。フミン酸、スペルミジン、スペルミンなどのポリアミンは、遺伝子発現を調節し、腸上皮細胞の増殖を促進し、腸管バリア機能を維持し、免疫系の機能に影響を与えることで骨老化関連疾患を調節することができる[166]。以前のレビューでは、骨粗鬆症に代表される骨老化関連疾患の研究分野における腸内細菌叢とその関連代謝物の重要な調節的役割と意義について詳しく説明したことに留意すべきである[21]。 |
| 3.5. 細菌性細胞外小胞と微生物ニッチの変化 |
| 細菌性細胞外小胞(BEV)は、独自のナノスケール構造、安定した積載能力、優れた生体適合性を有し、宿主細胞への生物活性物質の送達を可能にし、骨代謝を調節します。さらに、その豊富な存在量と生理学的効果から、腸管と骨の間のコミュニケーションにおける有望なメディエーターとなり、この相互作用のメカニズムに関する全く新しい視点を提供する可能性があります[167]。近年、腸内細菌叢と宿主の相互作用における中心的なメディエーターとして、細菌性細胞外小胞は変形性関節症(OA)の病理学的メカニズムを解明する鍵を握っていると考えられています。細菌性細胞外小胞は、グラム陰性(G−)細菌とグラム陽性(G+)細菌によって分泌されるナノスケールのリン脂質小胞です。生物活性成分を運搬し、腸管バリアを通過して循環系に入り込み、関節の免疫微小環境と軟骨の代謝バランスを調節することができます。従来の薬物送達システムと比較して、細菌性細胞外小胞は高収率、低免疫原性、およびエンジニアリングによる改変の容易さという利点を提供します。細菌性細胞外小胞は、ディスバイオシスを検出することによって変形性関節症の初期病理学的特徴を反映する「シグナル増幅器」として機能するだけでなく、抗炎症因子、遺伝子編集ツール、または修復促進分子の標的送達を介して関節の炎症と軟骨変性に対する精密な介入も可能にします[168]。このことから、細菌性細胞外小胞は変形性関節症の診断と治療において多次元的な革新の可能性を示しています。血液または糞便中の細菌性細胞外小胞の分析を介して変形性関節症の早期スクリーニングを可能にする診断バイオマーカーとして機能する可能性があります。病原性細菌の細菌性細胞外小胞分泌を阻害するか、プロバイオティクス源からの細菌性細胞外小胞を補充することにより、腸と関節の免疫バランスを回復することができます。エンジニアリングされた細菌性細胞外小胞は、標的修飾を介してmiRNA、抗炎症因子、または組織修復タンパク質を精密に送達し、軟骨代謝を直接制御して炎症を抑制することによって、従来の限界をさらに克服します。さらに、細菌性細胞外小胞は生体材料と組み合わせることで、軟骨再生を相乗的に促進します。細菌性細胞外小胞は、本来的に免疫原性が低く、薬剤搭載能力が高く、バリア透過性も高いため、変形性関節症の治療において革新的な理論的・技術的ブレークスルーをもたらします。 |
| 微生物ニッチの変化は、腸管-X軸を調節するための重要な経路としても機能します。Chenら[169]は、腸管-骨恒常性を回復するために、自己補充可能な代謝増強シンバイオティクスマイクロスフィアを開発しました。持続可能なプレバイオティクス基質であるヒアルロン酸は、ラクトバチルス・ラムノサスGGの代謝ニッチと微生物恒常性をサポートし、短鎖脂肪酸(酪酸、イソ酪酸、吉草酸を含む)の産生を促進し、主要な破骨細胞シグナル伝達因子のダウンレギュレーションに寄与します。このin situ発酵による経口マイクロスフィア戦略は、腸管-X軸を介して微生物叢関連代謝障害に対処するための新たな洞察を提供します。 |
| 3.6. 腸内細菌叢関連バイオマーカー |
| 短鎖脂肪酸、トリプトファン代謝産物、その他のバイオマーカーは、Treg/Th17免疫バランスを調節することで、破骨細胞の分化と骨吸収活性を精密に制御します。ディスバイオシス時には、これらのバイオマーカーの異常は骨免疫系の不均衡状態を直接反映し、介入後の正常化は免疫恒常性の回復を示します。さらに、リポ多糖類およびエンドトキシン関連マーカーは腸管バリア透過性を示し、そのレベルの変化は全身性の低度炎症を直接反映します[130]。このことから、炎症はNF-κB経路を活性化することで骨基質の分解を促進し、これらのマーカーの減少はバリア修復と炎症緩和の効果を評価する直接的な証拠となります。腸内細菌叢バイオマーカーの組み合わせモデルは、微生物機能遺伝子の存在量と宿主代謝産物フラックスを動的にモニタリングすることで、微生物生態系機能の全体的な回復を評価します。例えば、酪酸合成と抗炎症性サイトカインの同時増加は、局所的な微生物叢の再構築から全身的な筋骨格代謝の改善へと進行することを示している[170]。 |
| 4. 腸管-X軸関連経路に基づく健全な骨老化改善のための基礎的アプローチ |
| 現在、腸内細菌叢関連生物製剤、プロバイオティクス、プレバイオティクス、食事摂取、運動、糞便微生物移植などの介入戦略に関する研究が継続的に深まるにつれ、腸内細菌叢とその関連代謝物を標的とした骨老化関連疾患の予防と治療のための介入アプローチが、研究者によって徐々に評価され、継続的に研究されている[171、172、173]。腸内細菌叢とその関連代謝物は、宿主の骨恒常性を含む様々な生命活動の動的バランスを維持する上で重要な因子である[174]。腸管X軸の様式が証明されていることを前提として、上記の介入を介して骨老化関連疾患を制御する効果的な経路となる可能性があり、図3にその関連内容をまとめた。 |
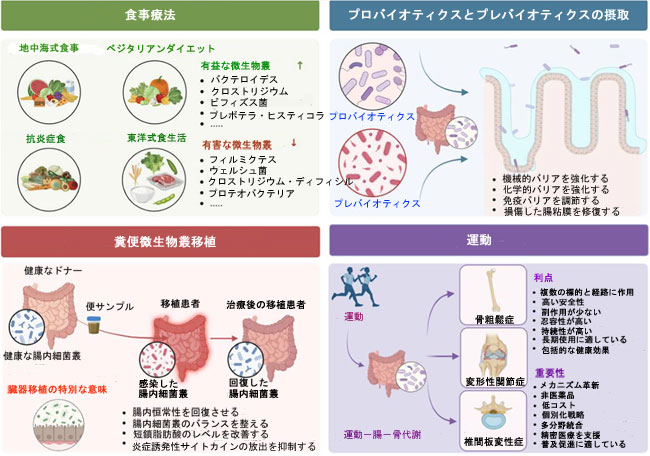 |
| 図3. 腸管-X軸関連経路に基づく、健康な骨老化を改善するための基本的なアプローチ。 |
| 4.1. 食事介入 |
| 食事は腸内細菌叢に影響を与える主要因であり、最も容易に変更または制御できる要因でもあります。食事による腸内細菌叢の変化は直接的かつ迅速です[175]。健康的な食事パターンとして認められている地中海式食生活は、穀物、野菜、果物、ナッツ、オリーブオイルを大量に摂取し、魚を適量、鶏肉、乳製品を少量摂取し、食事中に主にワインの形で適量のエタノールを定期的に摂取することを特徴としています[176]。対象とした観察研究のメタ回帰分析では、地中海式食生活スコアと股関節骨折リスクとの間に有意な負の線形関係が認められました[177]。以前の研究では、地中海式食生活への依存度が高い人の股関節骨折発生率は依存度が低い人よりもはるかに低いことが示唆されており、地中海式食生活への依存度が骨折リスクに反比例することが確認されています[178]。Moszakら[179]は、地中海食が、バクテロイデス、クロストリジウム、ビフィドバクテリウム・ロンガムなどの微生物叢の量を増やし、フィルミクテスの量を減らすことで、腸内微生物叢を効果的に調節できることを明らかにした。その中で、バクテロイデスは短鎖脂肪酸の代謝と生成の鍵であり、クロストリジウムは有機酸からより多くの短鎖脂肪酸の放出を促進できる。この研究では、マウスに経口アロエ多糖類を投与することで短鎖脂肪酸の量が増加した(3週間、300 mg/kg)[180]。短鎖脂肪酸ののサプリメント(4週間、67.5 mM酢酸)をマウスの飲料水に添加すると、破骨細胞のエネルギー代謝を妨害し、破骨細胞の形成を直接阻害し、循環インスリン様成長因子1(IGF-1)を調節することで間接的に骨リモデリングに関与することができる[181]。Chenら[182]は実験研究で、ラクトースの適度な補給が、腸粘膜バリア機能の強化、腸炎症反応の減少、腸内細菌叢と短鎖脂肪酸の組成の上昇により、マウスの骨量減少を改善できることを指摘した。Liら[183]は、プエラリンが腸粘膜バリアの完全性を修復し、短鎖脂肪酸のレベルを調節することにより、ラットの腸内細菌叢を改善し、腸内細菌叢のディスバイオシスを是正し、抗骨粗鬆症効果を発揮することを示唆した。Liら[184]は実験研究により、マグロ骨粉が腸粘膜バリア機能を修復し、炎症性サイトカインの放出を抑制し、腸内細菌叢の組成、量、多様性を調節することにより、マウスのグルココルチコイド誘発性骨粗鬆症を改善できることを実証した。Zhengら[185]は、粗多糖類の膝変形性関節症の進行に対する保護効果を調査し、桑、特に200 mg/kgの用量では、膝変形性関節症のラットにおいて、異常な歩行パターンを効果的に改善し、腸の炎症レベルを低下させ、軟骨下骨の損失を軽減し、損傷した関節面を修復し、軟骨破壊を遅らせ、腸内細菌叢の調節異常プロファイルを正に調節することを強調した。次に、ベジタリアン食パターン(平均6か月)は、植物性食品が主体の食パターンであり、穀物、野菜、果物、豆類の摂取量が多く、魚、卵、お茶の摂取量が中程度で、塩と乳製品の摂取量が少ないことを特徴とする[186]。以前の研究では、高健康植物性食事指数(hPDI)スコアの食事が腰椎と大腿骨頸部の骨密度に効果的な保護効果があり、中高年者の骨粗鬆症リスクの低減と密接に関連していることが示唆されました[187]。さらに、健康的な菜食主義の食事パターンは骨量減少に対する保護効果があり、不健康な菜食主義の食事パターンは骨粗鬆症の閉経後女性の骨密度に悪影響を与える可能性があります。したがって、生物学的価値の高い菜食主義の食事パターンに従うことは、骨老化関連疾患の遅延に非常に重要です。第三に、東洋の食事パターンは地中海の食事パターンに似ており、抗炎症の食事パターンと同様の効果と有効性があり、食物繊維、植物化学物質、葉酸をより多く摂取する傾向があります[188]。さらに、混合高繊維食(水溶性繊維20%と不溶性繊維20%)、高イヌリン食、高グアーガム食、高セルロース食、または異なるイヌリン投与量(12週間/22週間)の食事を与えたマウスは、腸内細菌叢が異なることが研究で判明しました。食物繊維を多く含む食事を長期間摂取すると、腸内細菌叢の多様性、特にビフィズス菌、乳酸菌、ルミノコッカスなどの有益な細菌叢の増加が促進され、短鎖脂肪酸のレベルを効果的に高め、骨老化関連疾患の調節に直接的または間接的に関与する可能性がある[189,190]。ある研究では、食品由来のオリザノールが腸内細菌叢-TLR4/NF-κB/NLRP3シグナル伝達軸を介してデキストラン硫酸ナトリウム(DSS)刺激による腸管バリア損傷と炎症反応を改善することがわかった。(食品由来のオリザノールを0.5% CMC-Na溶液に均一に分散させて懸濁液を調製し、100 mg/kg/日、14日間投与した)。そこでは、ルミノコッカスは酪酸の産生に必須の微生物であり、酪酸は骨髄由来マクロファージにおけるNLRP3インフラマソームの活性化を阻害し、骨吸収を軽減し、破骨細胞の分化を阻害し、足の配列に影響を与え、密な足帯やアクチンリングの形成を減らし、破骨細胞の骨吸収能力を損ない、骨の健康を維持することができる[191]。以前のレビューでは、骨粗鬆症に代表される骨老化関連疾患における腸内微生物叢とその関連代謝物の食事に基づく調節の重要な調節的役割と意義についても明らかにしたことに注目すべきである[16]。 |
| 4.2. プロバイオティクスとプレバイオティクスの補給 |
| プロバイオティクスは、十分な量で宿主に健康上の利益をもたらす生きた微生物と定義され、プレバイオティクスは、腸内細菌叢によって選択的に利用され、宿主の健康に生理的な利益をもたらす消化されない食品成分と定義されます[192]。現在、乳酸菌、ビフィズス菌など、いくつかの種類のプロバイオティクスとプレバイオティクスが、工業および農業生産、食品および医薬品製造業界で広く使用されています[193]。プロバイオティクスとプレバイオティクスの骨老化関連疾患に対する調節効果と影響に関する研究が徐々に増えています[194,195]。プロバイオティクスとプレバイオティクスの骨老化関連疾患に対する効果は表2に示されています。Chiang et al. [196]は、卵巣摘出(OVX)によって誘発された閉経後骨粗鬆症マウスにラクトバチルス・プランタルム NTU 101を含む餌(L. プランタルムNTU 101で発酵させた大豆脱脂乳の凍結乾燥粉末0.1gを毎日経口投与、8週間)を与えると、骨体積率が有意に増加したと報告している。以前の研究では、Darら[197]は、卵巣摘出によって誘発された閉経後骨粗鬆症マウスにバチルス・クラウシイを6週間経口投与すると、Treg-Th17細胞のバランスを回復し、炎症誘発性サイトカインを抑制し、抗炎症性サイトカインの発現を高めることで、エストロゲン欠乏による骨量減少を抑制できることを示した。Liら[198]は、グルココルチコイドデキサメタゾン誘発性骨量減少動物モデルにおいて、プロバイオティクスL. プランタルム(4/10週間、経口投与、1.0 × 10⁹ CFU/日/ラット)の骨量に対する保護効果とその潜在的なメカニズムを評価し、L.プランタルムがピラジンとγ-グルタミルシステインの血清レベルを顕著に上昇させ、それが破骨細胞形成の抑制と骨芽細胞形成の促進に関連していることを示唆した。さらに、Zhuらは、 [199]は、閉経後骨粗鬆症に対するブチリシコッカス・プルカエコルムと3-ヒドロキシアントラニル酸の併用(12週間、経口投与、1.09 × 10⁹ CFU/mL、投与量4.55 × 10⁹ CFU/kgに相当)の影響を評価し、腸内細菌叢とTh17/Treg、および大腿骨の立体パラメータとの間に関連性があること、B. プルカエコルムと3-ヒドロキシアントラニル酸の同時投与により、閉経後骨粗鬆症の改善に関連する腸内細菌叢の増殖が促進されることを指摘した。さらに、変形性関節症の治療または緩和にプロバイオティクスを利用するという考えも広まっている。これまでの報告では、ストレプトコッカス・サーモフィルス(8週間経口投与)、ラクトバチルス・ペントサス(プロバイオティクスとして)、γ-アミノ酪酸(GABA)が、生体内で変形性関節症に抵抗し、試験管内でIL-1β誘導軟骨細胞の変化を軽減し、プロバイオティクスによる治療が軟骨の異化を抑制し、マウスの関節を変性から救ったことが明らかになっている[200,201]。最近、閉経後女性の膝変形性関節症に対するB. アニマルス亜種ラクチス Probio-M8の補助効果を評価するために、4か月のヒト試験が実施された。この研究では、Probio-M8とコンドロイチン硫酸の併用投与が膝変形性関節症の症状を大幅に軽減することが実証された。プロバイオティクス介入は、腸内細菌叢および関連する代謝経路の調節を介して治療効果を高め、炎症を軽減し、臨床転帰を改善します[202]。腸-X軸モードに基づいて、プロバイオティクスとプレバイオティクスは、宿主腸内代謝物の調節、腸粘膜バリア機能、免疫調節、内分泌調節など、複数の観点から骨老化関連疾患を調節することができ、体内の骨代謝の調節におけるプロバイオティクスとプレバイオティクスの独自の応用価値を説明し、さらに将来の骨老化関連疾患の予防と治療のための新しいアイデアと参考価値を提供します。さらに、以前のレビューでは、骨粗鬆症に代表される骨老化関連疾患における腸内細菌叢とその関連代謝物のプロバイオティクス/プレバイオティクスに基づく調節の重要な調節的役割と意義をまとめたことに注目する価値があります[13]。 |
| 表2.プロバイオティクスとプレバイオティクスが骨老化関連疾患に及ぼす影響 |
 |
| 注: OVX、卵巣摘出術; OA、変形性関節症; GABA、γ-アミノ酪酸; ACLT、前十字靭帯切断術; IFN-γ、インターフェロンγ; IL-4、インターロイキン4; IL-10、インターロイキン10; WOMAC、ウェスタンオンタリオおよびマクマスター大学変形性関節症指数; Treg、制御性T細胞; Th 17、Tヘルパー細胞17。 |
| 4.3. 糞便微生物叢移植 |
| 近年、新たな移植技術として、糞便微生物叢移植は研究者の注目を集めている。簡単に言うと、糞便微生物叢移植とは、ドナーの糞便中の微生物叢を、経管栄養または経口投与によってレシピエントに移植する手法であり、腸内微生物の恒常性を回復させ、腸内微生物の不均衡を改善することを目的としている[203,204]。糞便微生物叢移植は、レシピエントの腸内微生物生態系を再構築し、炎症、免疫、代謝状態を改善する可能性を秘めており、骨老化関連疾患を含む様々な腸疾患や非経口疾患に対する新たな治療概念とアプローチを提供する[205]。これまでの研究では、糞便微生物移植(1か月に15回、経口投与)が腸管免疫を調節することで骨免疫を制御し、骨代謝に影響を与えることが示されている。腸内細菌叢は、腸粘膜固有層におけるサイトカインの産生とリンパ球の分化、特にCD4+T細胞のTh17細胞とTreg細胞への分化に影響を与える[206]。糞便微生物移植は、ヌクレオチド結合オリゴマードメインタンパク質(NOD1およびNOD2)受容体やToll様受容体5(TLR5)などのいくつかの受容体を介して、自然免疫を介して腸内細菌叢と骨との関連を媒介することもできる[207]。さらに、糞便微生物移植は腸疾患の治療法としてますます成熟してきているが、骨老化関連疾患の予防と治療への応用は初期段階にある。現在、糞便微生物移植の従来の投与経路は、経鼻投与、胃内視鏡検査、大腸内視鏡検査によるものであり、上記の手術による不快感は被験者のコンプライアンスを大幅に低下させる可能性がある[208]。 我々のこれまでの研究では、ドナー細菌(糞便ドナー:同じ環境で飼育され、同じ週齢と性別の健康なC57BL/6マウス)懸濁液を8週間毎日経口投与すると、過剰な破骨細胞形成が抑制され、卵巣摘出術誘発性骨量減少が予防されることが示されている[35]。いくつかのメタアナリシスでは、糞便微生物叢移植は、潰瘍性大腸炎および過敏性腸症候群に対する潜在的に安全で忍容性が高く効果的な治療法であることが示されている[209,210]。しかし、定期的かつ長期的な糞便微生物叢移植は、骨老化関連疾患を有する宿主の腸内微生物叢の構造と腸粘膜バリア機能を改善し、臨床現場で骨老化関連疾患の予防と治療に効果的な治療法となることが期待される、と考える価値は依然としてある[211]。しかしながら、糞便微生物叢移植は腸内細菌叢の調節や骨老化関連疾患への介入において有望な可能性を示しているものの、臨床応用には対処すべき重要な課題と潜在的なリスクが数多く存在する。糞便微生物叢移植は未知の病原体を伝播する潜在的なリスクを伴う。さらに、移植を受けた患者は胃腸症状を経験する可能性がある。より重篤な副作用としては、腸穿孔、出血、麻酔関連リスクなどが挙げられる[212]。糞便微生物叢移植が宿主の代謝、免疫機能、神経系に及ぼす長期的な影響は依然として不明である。今後の研究では、より安全で標準化された準備および注入プロトコルの確立が必要である。さらに、マルチオミクス技術を用いて、その有効性の根底にある主要な細菌種とメカニズムを特定する必要がある。その安全性と有効性を確認するためには、大規模かつ長期にわたる無作為化比較試験が必要である。さらに、リスクをより制御可能な特定の機能性微生物叢に基づく「精密微生物叢療法」の開発は、骨の健康にとって不可欠である[213]。 |
| 4.4. 身体活動 |
| 身体活動は、安価で簡便な非薬物療法として、腸管-X軸モードに基づき、骨の健康維持と骨老化関連疾患の予防に重要な役割を果たします。これまでの研究では、身体活動は腸内細菌叢とその関連代謝物の安定性を調整することで骨質に影響を与えることが明らかになっており、その原理は複数のレベルに及びます。例えば、1) 骨芽細胞のアポトーシス抑制:身体活動は腸内細菌叢の多様性を促進し、腸粘膜バリア機能を改善し、血中リポ多糖類の含有量を減少させることで、炎症反応と酸化ストレスを調節し、骨芽細胞のアポトーシスを遅らせます。例えば、高頻度サイクリングローラー運動は、腸内細菌叢と抗酸化ストレスの安定性を調整することで、骨芽細胞のアポトーシスを軽減することができます[214]。 2) 破骨細胞の分化の抑制: 身体活動は腸内細菌叢の安定性を向上させ、有益な細菌の数を増加させ、破骨細胞の分化を抑制することができます。例えば、自発的な車輪運動は、フィルミクテス と バクテロイデス の比率を調整することで破骨細胞の分化を抑制することができ、抵抗運動は腸内細菌叢の安定性を向上させ、Treg-Th17 細胞の割合を調整することで破骨細胞の形成を抑制することができます [215]。3) 骨芽細胞の分化の促進: 身体活動は、代謝産物の濃度を調整することで骨芽細胞の分化を促進することができます。例えば、ジョギングは、腸内細菌叢の代謝産物であるエクオールの濃度を調整することで、閉経後の女性の骨量減少を軽減することができます。有酸素運動(トレッドミル、10m/分、傾斜角10°、週5日、8週間、各セッション60分)は、胆汁酸や酪酸などの骨形成因子の分泌を促進することにより、骨芽細胞の分化を促進する可能性がある[216]。4)骨細胞の栄養代謝の調節:身体活動は腸粘膜バリアの防御機構を強化し、体内のミネラル、ビタミン、その他の栄養素の吸収を促進し、骨細胞への栄養供給を強化します。たとえば、抵抗運動は腸内でのカルシウムの吸収を高めるのに有益であり、骨の健康を維持し、骨の老化関連疾患を予防する上で特に重要です[217]。Jia et al. [218]は、膝変形性関節症ラットに対する異なる治療コースの効果を決定し、腸内細菌叢と炎症因子の観点から膝変形性関節症に対する灸の用量反応関係を探求し、灸治療により膝変形性関節症ラットの腸内細菌叢と炎症因子に重要な改善がもたらされ、4週間および6週間の灸治療により、プロバイオティクスの増加と病原性細菌叢の減少、炎症促進因子の減少、抗炎症因子の増強により腸内細菌叢のディスバイオシスを調節できることを示唆した。さらに、機械的負荷は維持に不可欠であるが、骨格の機械的応答性の非常に変動的な性質によって大きく制限される。Wangら[219]は、腸内細菌叢の枯渇により機械的負荷に対する骨格の適応が著しく低下することを発見した。微生物によって産生されたL-シトルリンとそのL-アルギニンへの変換は、骨格の機械的適応の主要な調節因子として同定され、これらの代謝産物の投与は、正常、高齢、および卵巣摘出マウスの骨格の機械的応答性を高めた。さらに、L-アルギニンを介した骨格の機械的適応の増強は、主に骨細胞における一酸化窒素-カルシウム正のフィードバックループの活性化に起因することが示された。加えて、以前の関連レビューでは、骨粗鬆症に代表される骨老化関連疾患における腸内細菌叢とその関連代謝産物に対する身体活動の重要な調節的役割と重要性も明らかにした[12]。 |
| 4.5. 腸内細菌叢関連バイオマーカー |
| 腸管-X軸に沿って、精密なスクリーニングと有効性評価のための腸内細菌叢関連バイオマーカーは、リスク予測から治療モニタリングまでのクローズドループ管理を可能にします[220]。低酪酸産生(低酪酸レベル)、腸管バリア損傷(血清リポ多糖結合タンパク質の上昇)、および骨を介した免疫炎症活性化(高IL-17)は、病理学的プロセスの連続体を構成し、骨代謝異常または骨量減少のリスク増加を示します。さらに、バイオマーカーの動的な変化を追跡することで、治療が標的経路に有効であるかどうかを客観的に評価できます[221]。介入後、特定のプロバイオティクスの増加、酪酸レベル、および短鎖脂肪酸の増加は、腸内細菌叢の機能的リモデリングを確認できます。血清炎症マーカーの低下、骨代謝マーカーの改善、腸管バリアマーカーの正常化は、腸内細菌叢の改善によって媒介される全身性炎症の解消と骨代謝バランスの回復を示している可能性がある[170]。総合的に見ると、腸内細菌叢関連のバイオマーカーは、潜在的な骨量減少のリスクを示し、客観的な有効性評価を提供し、食事調整、プロバイオティクス、薬剤などのさまざまな介入をモニタリングすることができ、最終的には腸内生態系の調節を通じて個別化された骨の健康維持を可能にする。 |
| 5. 現在の骨老化研究における腸管-X軸モデルの課題と改善の方向性 |
| 腸管-X軸モデルは骨老化の分野で大きな可能性を示していますが、まだ初期段階にあり、その本格的な応用には様々な課題が残されています。具体的には、以下の点が挙げられます。1) 因果関係の複雑性:腸内細菌叢と骨の健康との相互作用は、代謝系、免疫系、内分泌系など、複数のレベルとリンクにまたがっています。これらのシステム間の相互作用は複雑で、完全に解明することは困難であり、腸内微小環境の変化と骨老化関連疾患との因果関係を明確にすることは困難です。また、腸内微小環境は個人によって大きく異なるため、結果をより広い集団に直接一般化することは困難です[222,223]。 2) 研究手法の限界: 腸内細菌叢と骨の健康との関連性に関する現在の研究は、主に 16S rRNA ハイスループット シーケンシング、メタゲノミクス、メタボロミクス、プロテオミクス技術に依存しています [224]。しかし、これらの技術的手法には、実用上の限界があります。たとえば、16S rRNA ハイスループット シーケンシングは腸内細菌叢の構成と構造を包括的に分析できますが、その機能的活性を正確に反映することは依然として困難です [225]。メタボロミクスとプロテオミクス技術は、サンプル処理、検出感度、データ解析の課題によって制限されています [226]。 腸内細菌叢と骨の健康の間の相互作用メカニズムをよりよく明らかにするためには、より精密で包括的な研究アプローチを開発する必要があります。3) 臨床応用の難しさ: 腸-X軸モードに関連する基礎研究は大きく進歩していますが、腸内細菌叢と骨の健康の関連性に関する研究結果を臨床応用につなげるには、まだいくつかの困難があります。主な困難は、腸と標的臓器のリンクのメカニズムが不明確であること、さまざまな疾患の異質性が高いこと、個人差が大きいこと、大規模な臨床検証を行うためのさまざまな障壁に集中しています。4) 複雑な相互作用ネットワーク: 腸-X軸モードには、代謝、免疫、内分泌など、複数のシステムと臓器の相互作用が含まれます。これらのシステム間の複雑で多様な相互作用により、骨老化関連疾患における腸-X軸モードを探索する際に、さまざまな要因間の因果関係と相乗効果を正確に分析することが困難になります[227]。一方で、腸内細菌叢の複雑さ、異質性、個人差により、精密な介入が特に困難になります[228]。一方で、腸内細菌叢の特定の不均衡に対する効果的な介入方法はまだ確立されておらず、臨床研究では倫理、感受性、有効性、安全性など様々な要素を十分に考慮する必要があるため、現在の研究は複雑で困難を極めている。 |
| したがって、上記の課題に対応するため、今後の研究は主に次の側面に焦点を当てるべきである。1) さまざまな技術的アプローチ間の連携を強化する: 腸-X軸モードに関する基礎研究を強化し、腸内細菌叢と骨老化関連疾患との間のメカニズムを深く分析する。メタボロミクス、プロテオミクス、空間トランスクリプトミクスなどの高度な技術を使用して、腸内細菌叢の構成、機能、代謝経路、およびこれらの経路が骨老化関連疾患にどのように影響するかを包括的に分析する[229]。2) 精密なモデルの構築: 腸内細菌叢の個体差と複雑さに基づいて精密な動物モデルとin vitroモデルを構築することは有望なアプローチである。遺伝子編集や糞便微生物移植などのいくつかの技術を使用して、異なる個体および骨老化関連疾患状態における腸内細菌叢の変化をシミュレートし、病態生理学的プロセスをより正確に反映する[230]。 3) 学際的協力の強調: 骨老化関連疾患における腸管-X軸モードの研究は、微生物学、整形外科、内分泌学、免疫学、神経科学など、複数の学際的分野にまたがっています。したがって、学際的協力を強調し、異なる分野間のコミュニケーションと統合を促進し、学際的研究チームを編成して研究の困難と課題を共同で克服し、腸管-X軸モードの深化を促進することが不可欠です[231]。4) 個人差と集団特性に焦点を当てる: 腸-X軸モードに対する個人差と集団特性の影響を十分に考慮する必要があります。集団ベースの研究に基づき、年齢、性別、遺伝、生活習慣などの異なるグループの腸内細菌叢データを収集および分析して、腸内細菌叢と骨の健康の間の個人差と集団特性を明らかにすることは、より個別化された精密な介入措置の開発に貢献する可能性があります[232]。5) 高度な手段の開発と合理的な適用: 人工知能に代表される一連の高度な手段が腸-X軸モードの研究で徐々に出現しており、腸内細菌叢と骨老化の分子メカニズムの探索、臨床試験の設計、マルチオミクスデータ解析に強力な支援を提供することが期待されています[233]。したがって、腸-X軸モードの研究のボトルネックに対処するために、研究手段の革新、メカニズムの詳細な探索、統一基準の確立など、いくつかの側面で努力する必要があります。図4は、上記の関連内容をまとめて示しています。 |
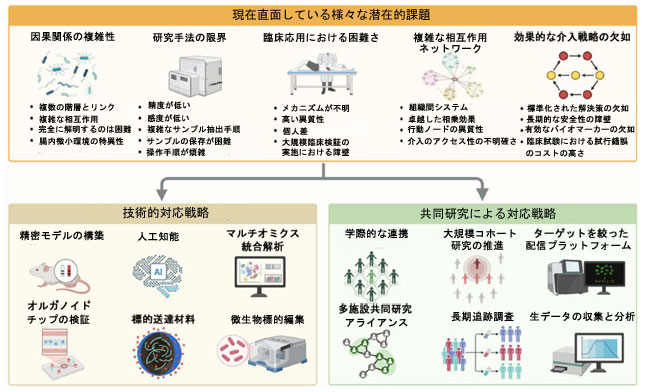 |
| 図4. 現在の骨老化研究における腸管-X軸モードの課題と潜在的な対応戦略 |
| 6. 結論と展望 |
| 腸内細菌叢は、腸内に生息する膨大な微生物群集として、骨老化の発生と進行に重要な役割を果たしています。腸管-X軸の研究は、骨老化関連疾患に関する従来の理解を覆し、骨粗鬆症、変形性関節症、椎間板変性症といった疾患の深層メカニズムの解明と予防に向けた新たな視点と潜在的な戦略を提供しています。この研究分野の今後の発展を見据えると、以下の点に引き続き注視していく必要があります。まず、腸管-骨軸、腸管-関節軸、腸管-椎間板軸が骨老化関連疾患において果たす役割については一定の理解が得られていますが、その具体的な分子メカニズムはまだ完全には解明されていません。今後の研究では、腸内細菌叢とその関連代謝物がシグナル伝達経路を介して関連細胞の生物学的挙動にどのように影響を与えるかに焦点を当てるべきです。一方、腸管X軸に関する現在の研究のほとんどは、動物実験やin vitro細胞実験に基づいており、臨床研究は比較的少ない。今後は、骨老化関連疾患の治療におけるマイクロエコロジー調節の実現可能性と安全性を検証するために、より大規模かつ多施設共同の臨床研究を実施する必要がある。 |
| 現在の腸管-X軸パターンの研究は、技術的および概念的なボトルネックに直面している。技術的には、既存の方法では、腸内細菌叢の空間的不均一性、その動的な遷移、および宿主細胞との局所的な相互作用を正確に解明することが困難である[234]。さらに、動物モデルは、ヒトの腸内細菌叢と老化の全身的な生理学的側面をシミュレートする上で限界がある。概念的には、腸内細菌叢と骨代謝を結びつける因果関係は依然として不明である。したがって、「細菌叢-代謝物-宿主受容体-シグナル伝達経路-骨細胞」軸には、より明確なメカニズム的調査が必要である。さらに、細菌叢と食事、遺伝、免疫、その他の要因との間の多因子的な相互作用の理解は不十分である。今後の取り組みは、腸内細菌叢に基づく骨格老化疾患の標的療法を進展させるために、空間マルチオミクスやオルガノイドなどの新しい技術の開発に焦点を当てるべきである[235]。 |
| さらに、腸内環境調節によって治療された骨老化関連疾患の患者については、疾患の予後を観察するために長期的な追跡調査が必要であり、腸内環境調節が骨、関節、椎間板の構造と機能に及ぼす長期的な影響、および疾患の自然経過を変えることができるかどうかを検証するためにも、さらなる研究が必要です。最終的には、腸-骨軸、腸-関節軸、腸-椎間板軸に対する一般の認識を高め、腸の健康と骨老化関連疾患との関連性についての一般の認識を高めるためのさらなる努力が必要です。健康に関する講演会や科学普及活動などを開催することで、腸内環境調節に関する知識を一般の人々に普及させ、健康的な食事とライフスタイルを推奨することで、骨老化関連疾患の患者により多くの恩恵をもたらすことができます。要約すると、本レビューは、腸-X軸の統合概念を創造的に活用し、腸-骨軸、腸-関節軸、腸-椎間板軸の根底にある共通のパターン化されたメカニズムを探求しています。さらに、この共通パターンが骨老化関連疾患を制御する潜在的なメカニズムを掘り下げ、これらの軸に基づいて骨老化関連疾患に対する治療戦略を将来的に概説する。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、J Orthop Translat. 2026 Feb 23;57:101064.に掲載されたGut microbiota and bone aging: Focusing on the gut-X axis modes.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


